SB203580在电压依赖性钾离子通道阻断剂4-氨基吡啶增强大鼠低氧高二氧化碳性肺血管收缩中的作用*
2013-12-01马迎春陈海娥黄林静何金波王淑君王万铁
马迎春, 陈海娥, 黄林静, 何金波, 王淑君, 陈 丹, 汪 洋,2, 王万铁,2△
(温州医科大学1基础医学院病理生理学教研室,2缺血/再灌注损伤研究所,浙江温州325035;3赤峰上京内分泌专科医院,内蒙古 赤峰024000)
肺动脉平滑肌细胞(pulmonary arterial smooth muscle cells,PASMCs)上钾离子通道功能异常在低氧性肺血管收缩及血管重构中均发挥重要作用[1],其中最重要且研究较多的是电压依赖性钾离子通道。近年来有关丝裂原活化蛋白激酶(mitogen activated protein kinase,MAPK)信号转导通路和低氧之间的关系越来越受到关注,逐渐成为研究的热点。p38 MAPK是MAPK信号家族一重要成员,可被许多应激刺激(包括低氧、活性氧)及某些G蛋白偶联受体激活,引起一系列生物化学反应[2-3]。本室先前研究[4]表明:在急性低氧高二氧化碳条件下,p38 MAPK信号通路抑制剂SB203580能减弱二级肺动脉环的II期持续收缩反应。那么p38 MAPK信号通路在低氧高二氧化碳性肺血管收缩(hypoxia hypercapnia-induced pulmonary vasoconstriction,HHPV)中发挥的作用与钾离子通道是否有关系,目前未见详细报道。本研究采用电压依赖性钾离子通道(voltage-dependent K+channel,KV)阻断剂——4-氨基吡啶(4-aminopyridione,4-AP)及SB203580在急性低氧高二氧化碳条件下孵育SD大鼠离体二级肺动脉环,动态观察血管环收缩张力的变化,探讨KV和p38 MAPK信号通路对急性HHPV的影响。
材料和方法
1 动物和试剂
清洁级雄性SD大鼠由温州医科大学实验动物中心提供[SCXK(浙)2010-0044]。SB203580购自Biosource,DMSO购自上海申工生物技术有限公司,重酒石酸去甲肾上腺素购自上海禾丰制药有限公司,乙酰胆碱(acetylcholine,ACh)和4-AP购自 Sigma。其余均为市售分析纯。
2 大鼠离体肺动脉环灌流模型的复制
SD大鼠36只,体重(300±20)g,随机均分成6组(n=6),按照本室先前报道的方法[4]制备大鼠低氧高二氧化碳性二级肺动脉环灌流模型,并平衡动脉环,检测内皮的完整性。
3 电压依赖性钾离子通道阻断剂4-AP及p38 MAPK信号通路抑制剂SB203580对HHPV的影响
在急性低氧高二氧化碳介质中,分别用4-AP及4-AP和SB203580联合孵育二级肺动脉环20 min,动态观察药物处理对HHPV的影响。所有二级肺动脉环随机分为:(1)常氧组(N组);(2)低氧高二氧化碳组(H组);(3)低氧高二氧化碳+DMSO组(HD组);(4)低氧高二氧化碳 +4-氨基吡啶组(4-AP组);(5)低氧高二氧化碳+SB203580组(SB组);(6)低氧高二氧化碳+4-氨基吡啶+SB203580组(4-AP+SB组)。N组和H组不做药物处理,HD组、4-AP组、SB组和 4-AP+SB组分别用 DMSO(0.05%)、4-AP(10-3mol/L)、SB203580(10-5mol/L)和4-AP(10-3mol/L)+SB203580(10-5mol/L)孵育20 min,然后按照低氧高二氧化碳反应性测定方法(除N组外)检测肺动脉环张力的变化。
4 统计学处理
用SPSS17.0统计软件分析,计量资料均进行正态性检验,数据(张力变化率)以均数 ±标准差(mean±SD)表示,多组样本均数比较进行方差齐性检验和单因素方差分析,方差齐性者两两比较采用LSD法,方差不齐者进行Dunnett's T3检验。以P<0.05为差异有统计学意义。
结 果
1 低氧高二氧化碳对二级肺动脉环张力的直接影响
N组持续通入95%O2+5%CO2混合气体60 min,张力变化率(tension percentage change,P%)未见明显变化,见图1A、表1。H组持续通入92%N2+8%CO2混合气体60 min,其张力曲线呈双相性收缩(biphasic vasoconstriction):即在急性低氧高二氧化碳条件下1~5 min内出现一个短暂、明显的收缩峰(I期快速收缩,phase I vasoconstriction),5 ~15 min此收缩峰表现为较明显的舒张(I期舒张,phase I vasodilation),15~20 min后又出现缓慢、持久的收缩(II期持续收缩,phase II vasoconstriction);H组二级肺动脉环的 P%与常氧组相比,差异显著(P<0.05),见图1B、表1。HD组作为溶剂对照组,与H组相比,二级肺动脉环P%变化不明显(P>0.05),见图1C、表1。
2 4-AP在急性低氧高二氧化碳介质中对二级肺动脉环HHPV的影响
选用4-AP孵育二级肺动脉环时发现,4-AP可增强二级肺动脉环的HHPV,尤其是II期持续收缩,与HD组相比,差异显著(P<0.05或P<0.01),见图1D、表1。
3 SB203580在急性低氧高二氧化碳介质中对二级肺动脉环HHPV的影响
用SB203580孵育二级肺动脉环时发现,SB203580可明显缓解急性低氧高二氧化碳引起的二级肺动脉环II期持续性收缩,但I期快速收缩没有明显变化,与HD组相比,差异显著(P<0.05或P<0.01),见图1E、表 1。
4 4-AP与SB203580联合应用在HHPV中的作用
用4-AP与SB203580联合孵育二级肺动脉环,发现SB203580能减弱4-AP所致的肺动脉环收缩幅度,使血管环张力下降。在急性低氧高二氧化碳介质中,4-AP+SB组I期收缩和I期舒张变化不明显,但收缩峰值较HD组明显下降,II期持续收缩逆转为舒张状态(P<0.05或P<0.01);4-AP+SB组二级肺动脉环II期持续收缩显著缓解,与HD组、4-AP组和SB组相比,均有显著差异(P<0.05或 P<0.01),见图1F、表1。
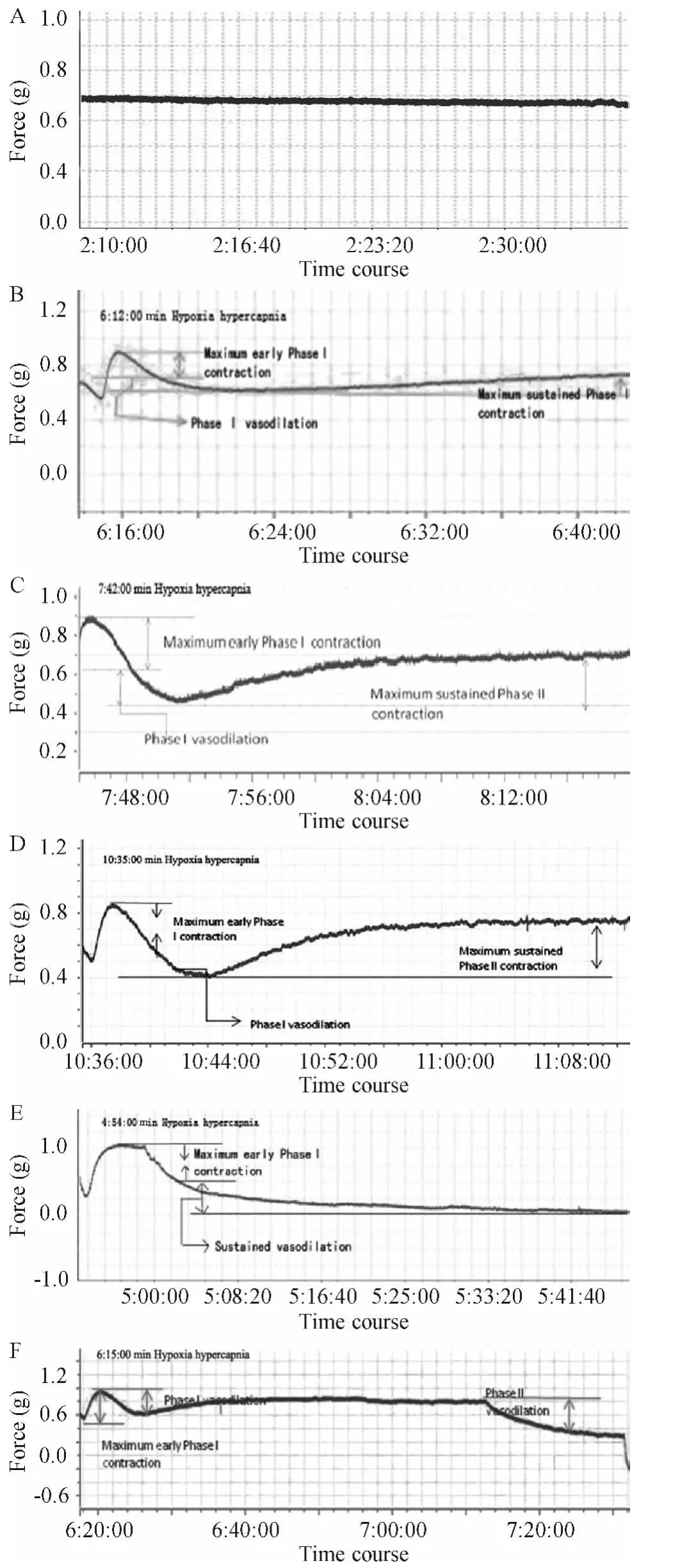
Figure 1.Dynamic changes of the tension of the second-order pulmonary artery rings in the six groups.A:control group;B:hypoxia hypercapnia group;C:hypoxia hypercapnia+DMSO incubation group;D:hypoxia hypercapnia+4-AP group;E:hypoxia hypercapnia+SB203580 incubation group;F:hypoxia hypercapnia+4-AP+SB203580 incubation group.图1 6组二级肺动脉环张力的动态变化
讨 论
低氧性肺血管收缩(hypoxic pulmonary vasoconstriction,HPV)的发生机制与PASMCs膜电位(membrane electricity,Em)变化密切相关。PASMC的张力主要受Em调控,膜去极化可激活L型钙通道(L-type voltage-dependent calcium channels,L-VDC),导致细胞外Ca2+内流,胞质Ca2+浓度升高,触发兴奋收缩偶联机制,引起平滑肌细胞收缩。而膜电位的大小取决于细胞膜上各种离子通道的活性,其中钾通道的作用至关重要。PASMCs上与HPV相关的钾通道主要有以下4种:(1)KV,包括延迟整流性钾通道(delayed rectifier K+channels,KDR)、瞬时外向钾通道(transient out ward K+channels,Kto)及缓慢激活的非失活性钾通道(non-inactivating K+channels,KN);(2)钙激活性钾通道(calcium-activated potassium channels,KCa),KCa通道根据电导值的不同分为高(BKCa)、中(IKCa)、低电导(SKCa)的钙激活钾通道,其中在血管平滑肌上分布广泛的是BKCa;(3)内向整流性钾通道(inward rectifier potassium channels,Kir);(4)ATP敏感性钾离子通道(ATP-sensitive potassium channels,KATP),KATP是由内向整流性孔区(Kir)和磺酰脲受体(sulfonylurea receptor,SUR)组成的八聚体,特异性阻断剂是格列苯脲(glybenclamide,Gly)。还有一种双孔区钾通道(two-pore potassium channels,Kt)正在研究中[5-6]。低氧可使 KV及 Kt受抑制,导致膜发生除极,引起L-VDC开放,Ca2+内流增加,触发兴奋收缩偶联机制[7]。洪志刚等[8]在离体大鼠肺的研究中指出,有些钾离子通道阻断剂可增加低氧状态下肺血管张力进而增强HPV,由此我们可以认为HPV是通过对钾离子通道的直接调控引起细胞膜去极化所致。周敏等[9]的实验结果亦支持肺动脉平滑肌细胞膜上的KV在低氧性肺血管收缩中起重要作用。因此,我们选用KV的阻断剂4-AP孵育急性低氧高二氧化碳介质中的二级肺动脉环,观察其HHPV的张力变化。结果发现经4-AP孵育的血管环HHPV的收缩幅度增强,Ⅱ期持续收缩较明显。我们的实验结果验证了KV与HHPV密切相关,阻断KV可增强肺动脉环HHPV收缩的幅度。这可能是因为肺血管的收缩与其血管平滑肌细胞膜电位变化密切相关,而膜电位的变化又直接调控血管张力的变化。

表1 6组二级肺动脉环张力的动态变化Table 1.The tension percentage changes of the second-order pulmonary artery rings in the six groups(Mean±SD.n=6)
MAPK即丝/苏氨酸蛋白激酶,是一种细胞外信号调节激酶,它参与了细胞生长、发育、分裂、死亡以及细胞间的功能同步等多种生理反应过程。p38 MAPK通路又称为应激激活的MAPK通路,实验中我们用p38 MAPK通路抑制剂SB203580孵育急性低氧高二氧化碳介质中的二级肺动脉环,结果发现SB203580可明显缓解急性低氧高二氧化碳引起的二级肺动脉环II期持续性收缩,但I期快速收缩没有明显变化,这与我们之前的研究结果是一致的[4]。在此基础上,为了进一步研究其与钾离子通道的关系,我们用4-AP与SB203580联合孵育二级肺动脉环,发现在低氧高二氧化碳条件下II期持续收缩明显下降,说明p38 MAPK信号通路可能在钾离子通道受阻断引起的II期持续收缩中发挥着重要的作用。因此我们有理由认为SB203580能够缓解因KV阻断而引起的HHPV。
在急性低氧高二氧化碳的条件下MAPK信号通路被激活,引起肺动脉平滑肌细胞收缩,而在此过程中钾离子通道呈现出受阻断的关闭状态,导致细胞膜去极化而产生细胞收缩。由此我们可以推断MAPK通路与钾离子通道之间可能存在着一定的联系,我们通过抑制 p38 MAPK通路缓解肺动脉的HHPV,而在此过程中钾离子通道可能处于开放状态,从而可以使肺动脉平滑肌细胞膜电位趋于复极化状态,减少钙离子内流,从而缓解其收缩程度。
综上所述,KV阻断剂4-AP可增强HHPV的作用,抑制p38 MAPK通路可以缓解4-AP引起的肺动脉HHPV。p38 MAPK信号通路的参与可能是电压依赖性钾离子通道调节低氧高二氧化碳肺动脉高压形成的重要机制之一,它们之间具体的作用机制尚待进一步研究。
