四氧化三铁磁性纳米微粒表面的氨基化修饰
2013-11-21娄兆文
胡 玮,娄兆文
(湖北大学 化学化工学院,湖北 武汉 430062)
纳米材料, 特别是磁性纳米颗粒,是近年来物理、化学、化工、生物医药、材料科学与工程等领域研究的热点[1-5]. 国内外大量工作集中在磁性纳米颗粒的表面修饰. 通过表面修饰使其功能化,应用于生物技术、医药和环境等众多领域[6]. 共混包埋法不需要进一步对微球表面进行化学处理就可以直接偶联所需的配体,是磁性纳米材料修饰极为有效的一种方法. 目前普遍使用Fe3O4纳米磁流体进行纳米粒子包埋研究,而对于Fe3O4纳米粒子粉体的改性鲜有报道.
3-氨丙基三乙氧基硅烷(APTES)是一种常用的氨基偶联剂,常温下为无色液体,可溶于醇、醚、酯等有机溶剂,也可溶于水,并且容易水解形成硅醇. 在酸性条件下把APTES水解缩聚后接到Fe3O4的表面,反应原理如图1所示.
本文作者利用APTES通过共混包埋法对磁性Fe3O4纳米粒子进行表面修饰,着重探索反应前对于市售Fe3O4粉体进行羟基活化的最佳条件,同时研究了不同的反应溶剂、Fe3O4纳米粒子与APTES质量比(简称投料比)、温度和时间对氨基修饰效果的影响.
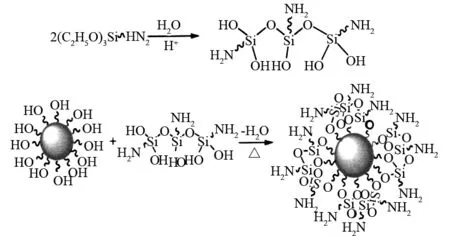
图1 Fe3O4 粒子表面硅烷化示意图Fig.1 Silanized scheme of Fe3O4 particles
1 实验部分
1.1 试剂及仪器
3-氨丙基三乙氧基硅烷(APTES,NH2(CH2)3Si (OC2H5)3), 纳米四氧化三铁(20 nm),购自阿拉丁公司;无水乙醇,无水甲醇,丙酮,冰乙酸均为市售分析纯试剂;试验用水为去离子水.
PE-Spectrum One 型红外光谱仪,KBr 压片; KQ218型超声波清洗仪,昆山市超声仪器有限公司;pHB-5型便携式酸度计,上海仪电科学仪器股份有限公司.
1.2 纳米Fe3O4粉体的表面羟基活化
取750 mg纳米Fe3O4粉体,加入50 mL去离子水后超声分散10 min. 维持60 ℃水浴加热,机械搅拌,N2保护下反应,加入一定量的稀盐酸(0.001 mol·L-1)将反应体系pH调节到4,然后每隔0.5 h测定一次反应体系的pH,及时补加稀盐酸使反应体系的pH维持在4,直到pH不再变化. 选择不同的pH条件和不同的反应温度对活化条件进行探索.
1.3 ATPES表面修饰Fe3O4纳米颗粒
取Fe3O4纳米颗粒750 mg活化后加入100 mL乙醇水溶液(50%), 用冰醋酸调节pH至4,室温下超声分散10 min (40 kHz) , 加入1 mL 硅烷化试剂,N2保护, 60℃水浴加热,机械搅拌反应10 h. 反应完毕依次用去离子水,无水乙醇和无水乙醚洗至无油状悬浮物,35 ℃真空干燥,称重. 同时选择不同的反应介质、温度和时间等条件进行优化.
1.4 氨基含量的测定[7]
电位滴定法是根据滴定过程中,指示电极的电位或pH产生“突变”,从而确定滴定终点的一种分析方法. 具体测定过程如下:取质量为m0功能化的Fe3O4磁性微粒, 加入定量的 HCl(n1) 标准溶液,超声震荡均匀,迅速用已知浓度(c2)的NaOH溶液滴定,记录pH随碱体积(V)变化的数据,做pH随V变化的曲线, 滴定终点时曲线上所对应的V值即为实际消耗碱的体积Ve,计算氨基的含量ω(μmol·g-1),公式如(1)所示.
ω=(n1-c2Ve)/m0
(1)
2 结果与讨论
2.1 不同的pH条件和温度对磁性纳米Fe3O4粉体活化的影响
分散在水溶液中的Fe3O4纳米颗粒比表面积大,裸露在颗粒表面的Fe与O原子易于吸附水溶液中的OH-和H+离子,从而使其表面具有丰富的羟基功能团,即Fe3O4表面金属Fe 原子以Fe-OH 形式存在[8]. 所以在适宜的反应条件下进行磁性纳米Fe3O4粉体表面羟基活化能够增加其包埋的反应位点,本文作者通过改变活化反应时的pH和温度条件,由消耗盐酸或氢氧化钠的量来比较活化程度的大小.
2.1.1 酸性条件下不同pH对磁性纳米Fe3O4粉体活化的影响
维持反应温度为60 ℃,反应体系pH分别为3.0、3.2、3.4、3.6、3.8、4.0. 如图2所示,活化反应基本在1.5 h内均已经完成. 随着反应体系pH的增大纳米粒子活化所消耗盐酸的量逐渐减少(调节溶剂消耗的盐酸量<1%,可以忽略不计). pH为3时盐酸在反应开始后基本无消耗,可以推断Fe3O4粉体在反应一开始即完成活化,但是pH为3.0时产品回收率(77.6%)小于pH为3.2 (85.2%)和3.4 (84.7%)的,并且pH为3.0 时磁性纳米Fe3O4粉体出现了轻微的酸溶解现象,所以pH 3.0不是最佳的酸活化条件,而且酸性活化时若溶剂pH小于3.0 Fe3O4粉体的酸溶解现象会加剧. 不同pH活化后Fe3O4纳米粒子表面-OH平均含量(μmol·g-1)如图3所示.

pH (a)3 (b) 3.2 (c) 3.4 (d) 3.6 (e) 3.8(f) 4.0图2 消耗盐酸的量随反应时间的变化Fig.2 Consumption of hydrochloric acid changingwith reaction time

图3 酸性条件下pH变化对活化的影响Fig.3 Effect of pH change on activation of acidiccondition
2.1.2 碱性条件下不同pH对磁性纳米Fe3O4粉体活化的影响
反应过程中温度为60 ℃,反应体系pH分别用NaOH溶液(0.008 mol·L-1)调节为9.0、9.2、9.4、9.6、9.8、10.0. 如图4所示,活化反应基本在1h内均已经完成. 随着反应体系pH的增大消耗NaOH的量逐渐增加,在pH为9.8时NaOH的消耗量最大,并且活化后Fe3O4纳米粒子表面-OH平均含量最高. 不同pH活化后Fe3O4纳米粒子表面-OH平均含量(μmol·g-1)如图5所示.

图5 碱性条件下pH变化对活化的影响Fig.5 Effect of pH change on activation of alkalinecondition
2.1.3 不同反应温度对磁性纳米Fe3O4粉体活化的影响
选择反应体系pH为3.2、3.4、9.8分别在50 ℃,60 ℃和70 ℃条件下进行活化反应后计算Fe3O4纳米粒子表面-OH平均含量(μmol·g-1),结果如表1所示. 酸性条件下50 ℃比60 ℃活化的效果好,碱性条件下60 ℃活化的Fe3O4纳米粒子表面-OH平均含量较50 ℃略高. 不论是酸性还是碱性条件活化,70 ℃温度都过高,活化后的Fe3O4纳米粒子出现结块现象.

表1 温度变化对活化的影响(μmol·g-1)Table 1 Effect of temperature change on activation

图6 (a)Fe3O4 纳米粒子、(b) Fe3O4/APTES复合粒子的红外光谱图Fig.6 FT-IR spectra of the (a) Fe3O4 nanoparticles, (b) Fe3O4/APTES complex
2.2 功能化磁性Fe3O4纳米粒子的红外光谱分析
与未修饰的Fe3O4纳米粒子相比,Fe3O4/APTES 纳米粒子在2 973 cm-1和2 885 cm-1处有较明显的-CH2及C-H伸缩振动峰,这主要来自于APTES中含有的大量-CH2;在 1 050 cm-1附近的强吸收峰为Si-O-Si的非对称伸缩振动峰,881 cm-1附近的吸收峰为Si-O-Si的对称伸缩振动峰[9];Fe-O键的伸缩振动峰位于587 cm-1,与未修饰的Fe3O4相比,Fe-O吸收峰波数发生了3 cm-1的蓝移. 修饰后样品的Fe-O 吸收峰发生蓝移是由于APTES 与纳米Fe3O4表面发生反应形成Fe-O-Si键,与Fe3O4表面的Fe-O-H相比,Si原子比H原子有更强的电负性,通过静电诱导作用,使得Fe-O 的键力常数增加, Fe-O 基团频率向高波数移动. 以上吸收峰证明了APTES成功的包覆到了Fe3O4纳米粒子表面.
2.3 不同的投料比及不同反应介质对修饰效果的影响
保持反应温度和时间以及反应体系中初始Fe3O4纳米粒子浓度为15 g/L不变,在1∶1的乙醇水体系、1∶1的甲醇水体系、1∶1的丙酮水体系[10]中依次改变投料比,反应后测定Fe3O4/APTES复合粒子表面的-NH2含量(μmol·g-1) ,结果见表2. 由表2可知在三种反应介质中当投料比为3∶8时,复合粒子表面的-NH2含量均达到最高值,并且丙酮水体系中合成的复合粒子-NH2含量要高于乙醇水体系和甲醇水体系,但是从溶剂的价格以及环保角度分析,乙醇水体系是较为理想的选择.

表2 不同投料比和反应介质对-NH2含量(μmol·g-1)的影响Table 2 Amino content changing with different reactant ratio and solvents
2.4 不同活化方式以及不同反应介质对修饰效果的影响
在乙醇水体系和丙酮水体系中分别用之前经过酸性活化、碱性活化和没有活化的磁性Fe3O4纳米粒子进行硅烷化反应,实验结果如表3 所示. 在乙醇水体系中经过活化的Fe3O4纳米粒子包埋效果比没有活化过的Fe3O4纳米粒子要好. 在丙酮水体系中硅烷化的Fe3O4纳米粒子更适合在酸性条件下活化.

表3 不同活化方式和反应介质对-NH2含量(μmol·g-1)的影响Table 3 Amino content changing with different activation method and solvents
2.5 不同反应时间对修饰效果的影响
Fe3O4表面通过硅烷化反应来改性的过程十分复杂. 许多实验参数如反应时间、温度、硅烷浓度都影响着硅烷分子链连接到Fe3O4表面的反应. 在不改变其他参数的情况下研究了不同反应时间对修饰效果的影响,结果如图7 所示. 若反应时间短,氨基含量偏低,当修饰反应在11 h 以上时,氨基含量可达到较高的值.

图7 不同反应时间-NH2含量的不同Fig.7 Amino content changing with different reaction time
2.6 不同反应温度对修饰效果的影响
温度对磁性纳米材料的修饰效果的影响很大(表4). 若温度过低则很难有效修饰;温度过高,会加速Fe3O4的氧化和晶形转变,反应后的产品出现结块的现象. 在70 ℃和80 ℃条件下合成的产品均出现了结块的现象, 因此氨基硅烷化过程应选择60 ℃左右,在低于晶化温度条件下反应.
3 结论
1) 本文通过硅烷化反应将APTES修饰到磁性Fe3O4纳米粒子表面,通过电位滴定法对Fe3O4/APTES复合粒子表面-NH2含量进行了测定.
2) 对于市售磁性Fe3O4纳米粉体进行表面羟基活化确实能够增加硅烷化反应位点. 碱性条件下活化所需时间比酸性活化短,而酸性条件活化后羟基的平均含量更高,硅烷化反应后所得复合粒子表面-NH2含量也更高. 在适宜的酸性或碱性条件下活化均比在中性条件下活化效果好.
3) APTES修饰磁性Fe3O4纳米粒子最佳反应温度为60 ℃,随着反应时间延长复合粒子表面的-NH2含量增加. 在乙醇水体系中Fe3O4纳米粒子与APTES质量比为3∶8是较佳的反应条件. 通过电位滴定法测得,-NH2含量可达1 400±50μmol·g-1.

表4 不同反应温度下产物-NH2的含量Table 4 Amino content changing with different reaction temperature
参考文献:
[1] MOGHIMI S M, HUNTEr A C H, MURRAY J C. Long-circulating and target-specific nanoparticles: theory to practice [J]. Pharm Rev, 2001, 53: 283-318.
[2] 董国君, 张密林, 王桂香.新型智能材料磁致变液的制备、性能评价及应用 [J]. 化工新型材料, 2001, 6: 17-19.
[3] BERRY C C, CURTIS A S G. Functionalisation of magnetic nanoparticles for applications in biomedicine [J]. J Phys D Appl Phys 2003, 36: 198-206.
[4] 王永飞, 李巧玲, 景红霞. 柠檬酸法合成纳米SrFe12O19的工艺分析及磁性研究 [J]. 化工新型材料, 2007, 35: 54-55.
[5] BERRY C C, WELLS S, et al. Dextran and albumin derivatised iron oxide nanoparticles: influence on fibroblasts in vitro [J]. Biomaterials, 2003, 24: 4551-4557.
[6] 冯 斌, 任志强, 屈晶苗, 等. 3-氨丙基三乙氧基硅烷表面修饰的磁性Fe3O4纳米粒子合成与表征 [J]. 化工新型材料, 2008, 36(12): 26-29.
[7] 武汉大学. 分析化学实验 [M]. 第四版. 北京: 高等教育出版社, 2001: 172-177.
[8] SHEN X C, FANG X Z, ZHOU Y H, et al. Synthesis and characterization of 3-aminopropyltriethoxysilane modified superparanlagnetic magnetite nanoparticles [J]. Chem Lett, 2004, 33: 1468-1469.
[9] FENG B, HONG R Y, WANG L S, et al. Synthesis of Fe3O4/APTES/PEG diacid functionalized magnetic nanoparticles for MR imaging [J]. Elsevier, 2008, 328: 52-59.
[10] 严向阳, 刘 端, 崔亚丽. 功能化磁性微粒的合成与表征 [J]. 陕西师范大学学报:自然科学版, 2005, 33(2): 69-73.
