一种二维多孔窗口型膦酸锆材料的合成及其对不同金属离子的吸附性能
2013-11-21莫士净崔纪利王润伟义建军徐庆红
莫士净,崔纪利,刘 亮,王润伟,义建军,徐庆红*
(1. 北京化工大学 化工资源有效利用国家重点实验室,北京 100029;2. 吉林大学 无机合成与制备化学国家重点实验室,吉林 长春 130012;3. 中国石油天然气集团公司 石油化工研究院,北京 100083)
α-Zr(HPO4)2· H2O(α-ZrP)于1964年被成功合成以来[1],磷(膦)酸锆及其衍生物的合成、结构以及性能的研究引起了人们广泛的重视.α-ZrP是一种无机层状结构材料[2-3],其比表面积大、机械强度高、热稳定性好、不溶于水和有机溶剂. 继1978年分子式为Zr(O3PC6H5)2的层状结构苯膦酸锆合成以来[4],磷酸锆层间的有机修饰以及利用有机膦酸直接合成有机膦酸锆类化合物的研究正在迅速开展起来[5-6].
研究发现,有机膦酸锆类化合物仍具有α-ZrP的层状结构,其层间距和材料本身功能取决于R基团的长短和性质. 如果应用有机双膦酸来进行有机膦酸锆的合成,就可能得到具有类分子筛结构的窗口型多孔材料[7]. 由于有机基团结构以及链长的可调变性,可以合成不同孔径大小的新材料[8]. 该类材料不仅可以直接作为催化剂进行酸催化反应,而且还可以用作催化活性中心的载体. 1982年,自首例具有层柱状结构的有机双膦酸锆Zr(O3PC6H4-PO3)2被成功合成以来[9],分子通式为α-Zr(O3PRPO3)0.4(HPO4)2(其中R=Me2H2C6-C6H2Me2)的窗口型有机膦酸锆材料相继被成功合成[10]. 新型膦酸锆的合成将磷酸锆研究扩展到了一个新的领域.
含重金属离子废水具有很强的污染性,其毒性具有较长的持续性. 此类废水的处理常采用化学沉淀、离子交换、电解、吸附、膜分离等方法[11]. 吸附法是利用吸附剂的独特结构去除重金属离子的一种有效方法. 根据机理的不同,重金属离子的吸附可分为交换吸附、物理吸附、化学吸附等. 吸附剂中存在的各种活性基团通过与金属离子形成离子键或共价键,达到吸附效果. 目前使用的吸附剂有活性炭[12-13]、腐植酸树脂[14]等,只有活性炭在实际中应用较多. 但活性炭再生效率低,一般用于电镀废水的预处理. 用腐植酸类物质处理含铬、含镍废水也有成功先例. 微介孔材料磷酸钛[15-16]在处理含有Pb2+、Hg2+、Cd2+等重金属离子废水中有很好的应用,处理后废水中金属离子含量低于污水综合排放标准.
作者分别从初始浓度、温度、初始pH三个方面,以实验室合成的新型二维窗口状材料β-丙氨酸-N,N-双亚甲基膦酸锆(ZrNCP)为吸附剂对不同半径的Mg2+、Zn2+、Mn2+、Cd2+、Pb2+的吸附规律进行深入探究,力求找到主体材料对客体金属离子的吸附规律,为吸附学研究提供一些有参考价值的数据资料.
1 实验部分
1.1 试剂与仪器
β-丙氨酸、亚磷酸、浓盐酸、磷酸、八水合氧氯化锆(ZrOCl2·8H2O)、氢氟酸、甲醛、四水合硝酸锰、六水合硝酸镁、六水合硝酸锌、四水合硝酸镉、硝酸铅等药品均为分析纯,购自北京化学试剂公司.
样品的X射线粉末衍射分析(XRD)在XRD-6000型粉末X射线衍射仪(日本岛津公司)上得到. 通过Vector22型傅立叶红外光谱仪(德国Bruker公司)测定样品的红外光谱(FT-IR). 样品的比表面和孔径分布、比孔容通过AS-1C-VP型比表面-孔径分布测定仪(美国康塔公司)分析. 采用氮气为吸附质,测试样品在200 ℃脱气处理2 h,比表面采用多点BET法得到,孔径分布采用HK法微孔分析得到. 采用日本电子株式会社JEM-2010型高分辨电子显微镜对样品结构进行微观结构表征. 采用日本日立公司S-4700型扫描电子显微镜(SEM)观测样品的形貌特征,所有样品都经喷金处理. 用HCT-2型热分析仪(北京恒久科学仪器厂)对样品的热物理性质进行测试. 样品中的C、H、N元素分析在德国Elementarvario元素分析仪(载气流速为200 mL/min,氧气流速为20 mL/min,燃烧管温度为950 ℃,还原管温度为550 ℃)上进行. 运用日本岛津ICP-7500型等离子体电感耦合光谱仪测定样品中Zr、P的含量. 样品表面的元素组成及状态分析在VG ESCALAB250 型X射线光电子能谱仪(英国Thereto公司)上进行. 测试条件为:辐射光源Al Kα靶 (1 486.6 eV),分析室真空度2×10-9Pa,操作电压25 kV,光斑直径100 μm,内标C1s电子结合能284.8 eV. 用安捷伦4510原子吸收(AAS)光谱仪测定水溶液中金属离子的含量,其中燃气为乙炔气,助燃气为空气,选择适合的分析线、燃助比、燃烧器高度、狭缝宽度以及空心阴极灯工作电流.
1.2 实验过程
1.2.1 β-丙氨酸-N,N-双亚甲基膦酸的合成
将8.2 g(0.1 mol)H3PO3溶于10.0 mL去离子水中,并与4.5 g(0.05 mol)NH2CH2CH2COOH及5.0 mL浓盐酸一起置于三口瓶中搅拌. 当混合物油浴加热至95 ℃时缓慢滴加11.0 mL (0.15 mol)40%甲醛水溶液(10 ~ 15 min内加完),恒温110 ℃并回流90 min. 冷却后采用丙酮析出方法对产物进行粗提纯,然后经碱溶,酸化,最后再用8.0 mol/L的盐酸对所得固体进行重结晶,即得纯净产物β-丙氨酸-N,N-双亚甲基膦酸(ATMPA)(分子式为H2O3PCH2N(CH2CH2COOH) CH2PO3H2). 理论上各元素含量(%)分别为C:21.39;H:4.63;N:4.98;O:45.99;P:22.52. 实测上述各元素含量(%)分别为C:21.66;H:4.69;N:5.05;O:46.21;P:22.38. 合成产物的纯度达到99.37% (以P元素含量计算得到). C5H13O8NP2合成反应机理如下[17]:
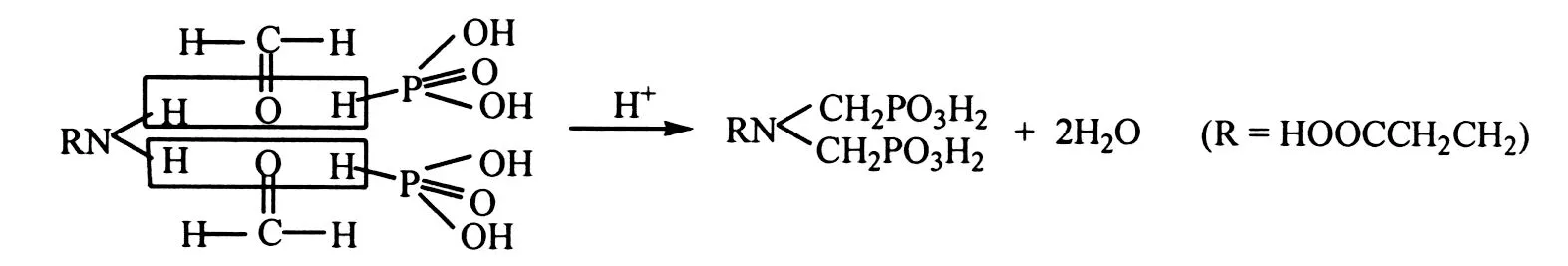
1.2.2 二维窗口有机膦酸锆(ZrNCP)的合成
将有机双膦酸ATMPA(5.3 g)与磷酸(4.0 g)混合溶于40 mL去离子水中;将ZrOCl2· 8H2O (6.1 g)溶于20 mL去离子水中,并按照n(F-)/n(Zr4+)= 8向其滴加6.7 mL HF水溶液配制成[ZrF6]2-溶液. 将上述配制好的有机膦酸水溶液倒入三口瓶中,水浴加热至80 ℃,并在搅拌下向其逐滴加入[ZrF6]2-溶液,直至烧瓶中出现大量的乳白色悬浊液. 混合液继续于80 ℃下回流24 h,然后将其转移至聚四氟乙烯内衬反应釜中,150 ℃下晶化5 d后进行离心分离,洗至溶液接近中性. 固体样品于80 ℃干燥后放置干燥器中备用.
1.2.3 金属离子吸附实验
准确称取一定质量的M(NO3)2(M = Mg2+、Zn2+、Mn2+、Cd2+、Pb2+),溶于去离子水中,配制成一定浓度的M2+溶液,采用火焰原子吸收法分别测定其浓度.
ZrNCP对不同初始浓度M2+的吸附:分别配制初始浓度为50、100、200、300、400、500、600、700、800、900 mg/L的M2+溶液,取其100 mL转移至圆底烧瓶中. 25 ℃恒温搅拌下加入0.1 g 的ZrNCP样品,开始计时. 一定时间t后,取1.0 mL悬浊液稀释到100.0 mL, 经过离心去除沉淀后测定溶液中金属离子的浓度.
ZrNCP在不同反应温度下对M2+的吸附:分别准确量取初始浓度为500 mg/L的M2+溶液100.0 mL转移至三口圆底烧瓶中,水浴加热并回流搅拌,于不同的温度(30、40、50、60、70、80 ℃)下加入ZrNCP样品(0.1 g),开始计时. 一定时间t后, 取1.0 mL 悬浊液稀释到100.0 mL,经过离心去除沉淀后测定溶液中金属离子的浓度.
ZrNCP对不同初始pH的M2+的吸附:分别准确量取初始浓度为500 mg/L的M2+溶液100.0 mL转移至圆底烧瓶中,用1.0 mol/L的HCl调节体系初始pH(pH = 1.0、2.0、3.0、4.0、5.0),25 °C恒温搅拌下加入0.1 g 的ZrNCP样品,开始计时. 一定时间t后, 取1.0 mL 悬浊液稀释到100.0 mL, 经过离心去除沉淀后测定溶液中金属离子的浓度. 实验过程中平衡吸附量的计算公式[18]为
(1)
其中,Qe为吸附剂的平衡吸附量(mmol/g);c0、ce分别为吸附前后溶液中金属离子的浓度(mg/L);V为量取的溶液体积(mL);W为吸附剂的质量(g);M为金属离子的摩尔质量(g/mol).
2 结果与讨论
2.1 合成产物ZrNCP的表征
图1a为ZrNCP的N2吸脱附曲线. 按照IUPAC分类,这些曲线介于Ⅰ和Ⅱ型之间,倾向于Ⅱ型. 从该图可以看出,样品在低相对压力区域(p/p0< 0.03)对气体的吸附量有一个快速增长过程,这是微孔被气体分子填充过程的特征. 由于介孔或外表面多分子层吸附的存在,气体在高相对压力区域(p/p0> 0.8)也有一个吸附量快速增长过程[19]. 由于吸附和脱附行为的不同,样品的脱附曲线具有典型H3型迟滞回线特征[20]. 因此在ZrNCP中存在介于微孔和介孔之间的孔道.
样品的孔分布曲线如图1b所示. 曲线中有一宽度很窄的峰出现在0 ~2 nm之间,还有一稍宽的峰出现在2 ~6 nm之间. 出现在0.72 nm处的峰可能来自于合成材料中孔道的平均高度,这与计算结果相一致;而出现在2.37 nm处的宽峰归属目前尚不清楚,其可能是孔道宽度的表现. BET法计算结果表明,ZrNCP的比表面积为94 m2/g,孔体积为0.282 cm3/g.
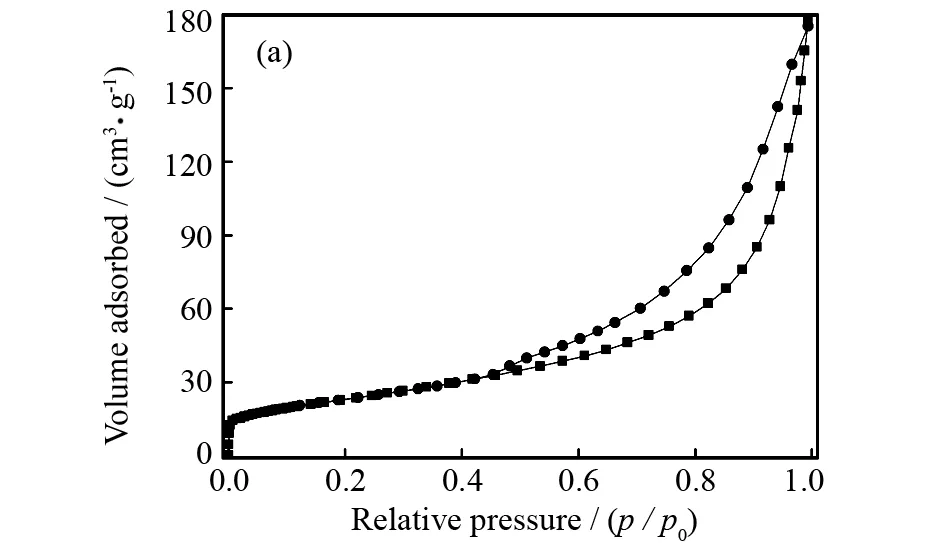

图1 ZrNCP的N2吸脱附曲线及孔分布曲线Fig.1 N2 adsorption-desorption isotherms (a) and pore width distribution curves (b) of ZrNCP
从ZrNCP的TEM图像(图2a)上可以清晰地看到材料中孔道的高度大约为0.7 nm、宽度大约为2.5 nm,这些分布规整的孔道将上下相邻的无机层板紧紧地连接在一起并形成类似窗口状. 材料内部的这种孔结构可能如图3所示. 图2b是ZrNCP的SEM照片. 从图2b 可以看出,合成产物的微形貌呈规整片状. 片层的厚度大约在30~50 nm之间,长度大约在400 nm左右. 与α-ZrP不同的是,这些叶片相互连接在一起,微孔结构则存在于这些叶片内部.

图2 ZrNCP的透射(TEM)电镜(a)和扫描(SEM)电镜(b)照片Fig.2 TEM (a) and SEM (b) images of ZrNCP
ZrNCP的XRD衍射谱图如图4所示. 通常情况下,对于非孔性及层状材料来说,应用布拉格公式2dsinθ=Nλ,物质在广角度范围内衍射峰的d值等于晶体的层间距或者面间距;对于孔材料来说,其在小角度衍射峰d值等于孔径大小. 图4中11.40°处的弱衍射峰对应d值是0.77 nm,与图2 ZrNCP的TEM图像所观察到的孔道高度相吻合.

图3 ZrNCP形成的可能结构Fig.3 Possible structure of ZrNCP
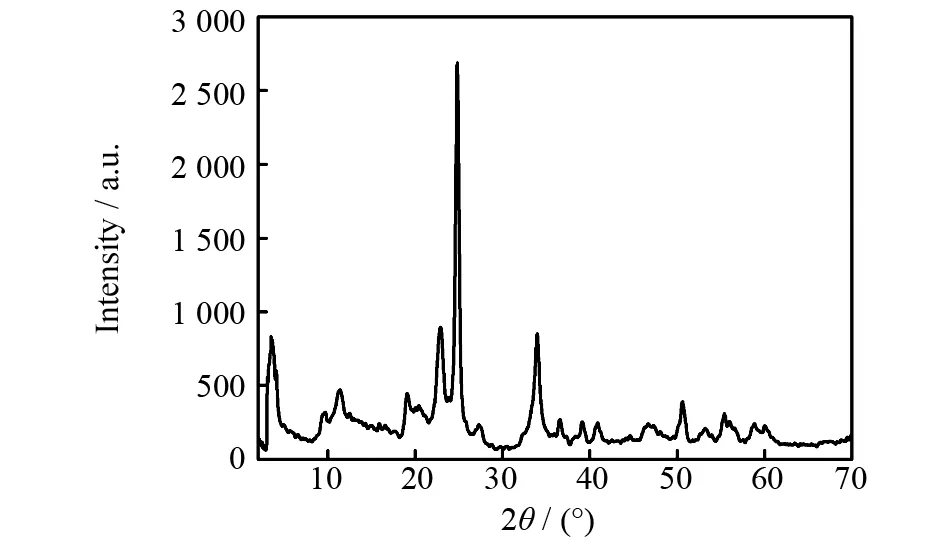
图4 ZrNCP的X射线衍射谱Fig.4 XRD patterns of ZrNCP

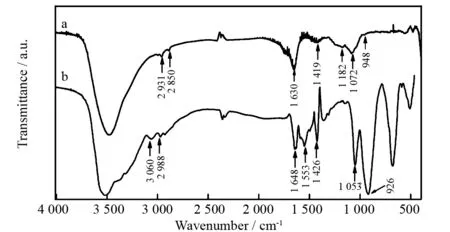
图5 红外波谱分析图(a:ATMPA,b:ZrNCP)Fig.5 FT-IR spectra of ATMPA (a) and ZrNCP (b)
ZrNCP的差热-热重分析如图6所示. 由热重曲线可以看出在350 ℃以前曲线基本上是水平的,因此可以断定合成的材料中基本上没有结晶水. ZrNCP第一失重阶段的温度区间为400 ~ 700 ℃,这一失重过程主要来自于ZrNCP骨架上有机部分的燃烧,这与差热曲线上出现的放热峰(500 ℃左右)相一致. 第二失重阶段温度区间是850 ~ 880 ℃,这一失重主要来自于上一阶段未完全燃烧的有机部分. 整个过程的失重大约为16.0%,这与元素分析所测得有机元素的含量相一致. 元素分析结果表明在ZrNCP中,C、H、N的含量分别为 9.26%,2.56%和4.75%. 由以上分析可看出,ZrNCP骨架在350 ℃以前是稳定的,说明该合成材料的热稳定性还是比较高的. 当温度高于350 ℃后,材料内部结构开始遭到破坏. 当温度加热到880 ℃以上时,该材料基本上没有失重现象了. 按照磷(膦)酸锆类化合物的特点,此时材料的骨架结构已经转化为焦磷酸锆[22](如图7). 图7是900 ℃ 煅烧后ZrNCP的XRD衍射图像,其与标准的焦磷酸锆XRD基本相吻合.
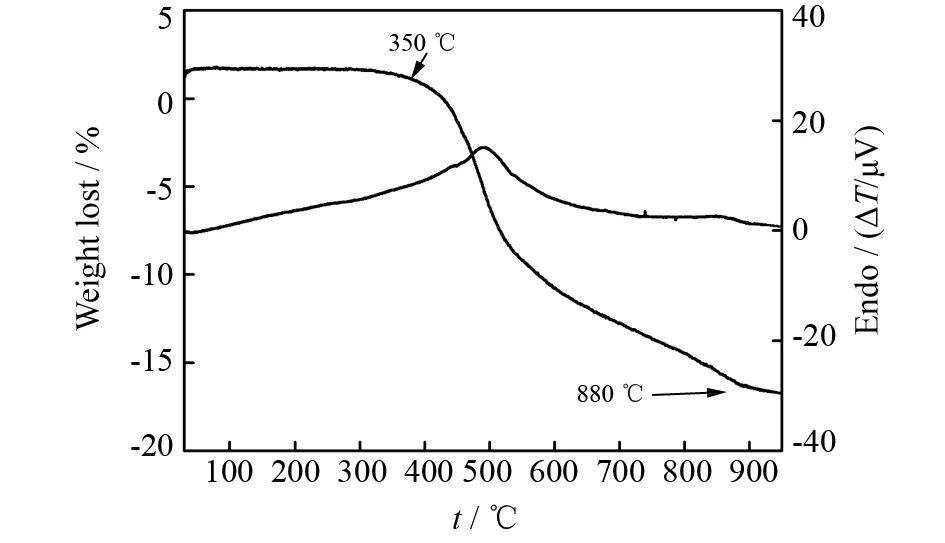
图6 ZrNCP的差热-热重图Fig.6 TG-DSC analysis of ZrNCP

图7 900 ℃煅烧后ZrNCP的XRD衍射图像Fig.7 XRD pattern of ZrNCP calcined under 900 ℃
2.2 ZrNCP对不同半径的金属离子的吸附
为了研究ZrNCP对不同半径金属离子的吸附规律,我们选取了五种不同金属离子,它们分别是Mg2+、Zn2+、Mn2+、Cd2+、Pb2+,其半径分别为0.067、0.073、0.080、0.092、0.120 nm[23]. 我们分别从初始浓度、温度、初始pH三个变量来考察ZrNCP对这五种金属离子的吸附行为. ZrNCP对金属离子的吸附可以分为物理吸附和化学吸附两个过程. 对于轻金属Mg2+来说,由于核外电子结构特点,其不易形成配位键,因此Mg2+的吸附系简单物理吸附,范德华力在吸附过程中起到绝对作用. 而对于其他四种金属离子来说,它们在水溶液中首先与水分子结合形成水合离子[M(H2O)2]2+[18]. 当水合金属离子进入到主体材料孔道中时,与M2+离子弱结合的一个水分子将离去形成[M(H2O)]2+,此时[M(H2O)]2+中的M2+将利用其核外空d轨道与ZrNCP骨架链接的有机链上可配位羰基和亚氨基进行配位,形成稳定的六元环. 为了证明主客体之间这种配位键的形成,作者对主体材料(吸附剂)中的部分元素吸附重金属离子前后X光电子能谱变化进行了仔细分析.
图8是ZrNCP与ZrNCP-M2+(M = Zn,Mn,Cd,Pb)中O1s和N1s的XPS分析图. 吸附剂ZrNCP中O元素1s电子能谱存在两种状态,即EO-H和EO-C,它们分别为531.0 eV和530.1 eV. 由于ZrNCP是在酸性条件下合成的,N元素1s电子能谱也存在两种状态,分别为EN-C和EN→H+,它们的电子结合能分别为401.2 eV和400.1 eV. 由左边曲线可以看出,ZrNCP与金属离子反应后的O1s电子两种状态结合能均发生了明显变化,具体数据如表1所示. 右边曲线显示了吸附前后N1s电子两种状态的电子结合能变化情况,具体数据也列入表1中. 吸附后O1s和N1s电子结合能的变化可能来自于O、N和M2+之间发生的配位作用.
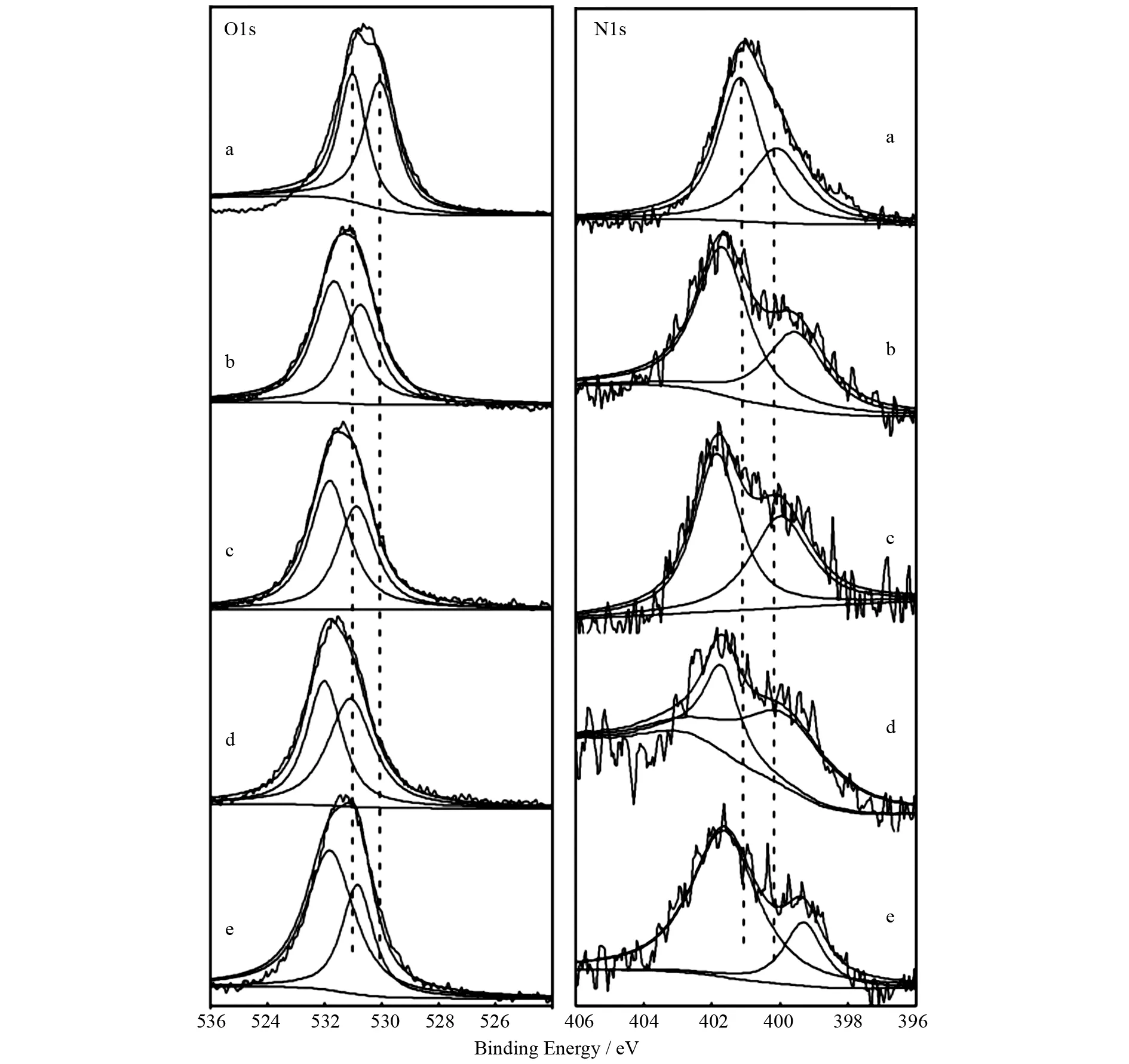
a:ZrNCP;b:ZrNCP/Zn2+;c:ZrNCP/Mn2+;d:ZrNCP/Cd2+;e:ZrNCP/Pb2+图8 吸附剂吸附前后的O1s以及N1s XPS分析Fig.8 The XPS analysis of O1s and N1s in adsorbent before and after adsorptions

ZrNCPZrNCP/Zn2+ZrNCP/Mn2+ZrNCP/Cd2+ZrNCP/Pb2+EO1s(O-H) /eV531.0531.7531.8532.0531.8EO1s(O-C) /eV530.1530.8530.8531.1530.8EN1s(N-C) /eV401.2401.7401.8401.8401.7EN1s(N→H+)/eV400.1399.6400.0400.0399.3
图9是五种金属离子的初始浓度与吸附剂吸附容量之间的关系曲线图. 由图9可知,ZrNCP对金属离子吸附容量随金属离子浓度的增大而增大. 当初始浓度很低时,Qe随c0的增加而迅速增加;当c0增加到一定值时,Qe增加缓慢并最终达到一个稳定值,说明吸附达到平衡. 此时吸附剂对以上五种金属离子的最大吸附容量分别为4.24、1.80、1.42、0.58、0.40 mmol/g,与它们的离子半径大小顺序相反.

图9 初始浓度对吸附容量的影响Fig.9 Effect of different concentrations on the maximum capacity of ZrNCP at equilibrium
五种金属离子(c0= 500 mg/L)的吸附容量随环境温度变化曲线如图10所示. 由图10可知,在30 ~ 50 ℃之间ZrNCP对Mg2+的吸附容量随着温度的升高而增加,在50 ~ 80 ℃之间随着温度的升高而减小. 对于其他金属离子Mn2+、Zn2+、Cd2+、Pb2+来说,温度对Qe的影响基本相同. 在30 ~ 60 ℃间Qe是随着温度的升高而增加的,这可能是由于在相对低的温度区间,分子扩散速率随着温度的升高而增大,使得Qe逐渐增加,但增加的幅度不算太大.Qe在60 ~ 80 ℃温度变化区间随着温度的升高而逐渐减小,温度升高可能破坏吸附剂ZrNCP的活性吸附位点. 从图10还可以看出,五种金属离子Mg2+、Zn2+、Mn2+、Cd2+、Pb2+的最大吸附量Qe分别是11.93、1.54、4.76、1.28 和0.82 mmol/g. 吸附剂对Mg2+吸附量最大,其原因可能是Mg2+的半径远远小于其他金属离子,致使单位质量内Mg2+被吸附的数量较多. Zn2+的最大吸附量Qe值大小与半径大小关系出现反常,可能与锌离子核外电子轨道全充满有关.


图10 温度对吸附容量的影响Fig.10 Effect of temperature on the maximum capacity of ZrNCP at equilibrium

图11 初始pH对吸附容量的影响Fig.11 Effect of initial pH on the maximum capacity of ZrNCP at equilibrium
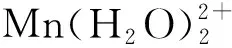
3 结论
我们以β-丙氨酸-N,N-双亚甲基膦酸和八水合氧氯化锆为原料合成了一种新型的二维窗口型膦酸锆材料ZrNCP. 该材料呈现一些规整的叶片状,在这些叶片上大量分布着孔道高度为0.72 nm、宽度为2.37 nm的微介孔,它们共同组成了类似0.72 nm×2.37 nm大小的窗口状. 以新合成的膦酸锆ZrNCP为吸附剂,研究了金属离子半径与它们最大吸附平衡量之间的关系. 从所选取的五种不同半径的金属阳离子Mg2+、Zn2+、Mn2+、Cd2+、Pb2+的吸附实验发现,随着金属阳离子半径的增大,主体材料ZrNCP对金属离子的最大吸附量呈递减趋势. 这一发现为废水中重金属离子的去除提供了必要的实验依据.
参考文献:
[1] CLEARFIELD A, STYNES J. The preparation of crystalline zirconium phosphate and some observations on its ion exchange behaviour[J]. J Inorg Nucl Chem, 1964, 26(1): 117-129.
[2] ALBERTI G. Syntheses, crystalline structure, and ion-exchange properties of insoluble acid salts of tetravalent metals and their salt forms [J]. Acc Chem Res, 1978, 11: 163-170.
[3] CLEARFIELD A, LANDIS A L, MEDINA A S, et al. More on crystalline zirconium phosphates[J]. J Inorg Nucl Chem, 1973, 35(4): 1099-1108.
[4] ALBERTI G, COSTANTINO U. Intercalation chemistry of acid salts of tetravalent metals with layered structure and related materials [M]. Intercalation Chemistry, New York, London: Academic Press, 1982, 147-179.
[5] 马学兵, 傅相锴, 李龙芹, 等. 一些晶态层状有机-无机混合磷酸锆的制备、表征和层间距分析[J].无机化学学报, 2001, 17(1): 124-128.
[6] COSTANTINO U, NOCCHETTI M, MARMOTTINI F, et al. Amino acid derivatives of layered zirconium phosphates-α-zirconiumL-(+)-serinephosphate and zirconiumL-(+)-serinephosphate phosphates[J]. Eur J Inorg Chem, 1998, 10: 1447-1452.
[7] 吴宗斌, 田 鹏, 刘中民, 等. 多孔膦酸盐的研究进展[J].化学进展, 2006,18(9): 1092-1110.
[8] CLEARFIELD A. Organically pillared microporous zirconium phosphonates[J]. Chem Soc Dalton Trans, 2002, 15: 2937-2947.
[9] MARTIN B D, PETER M D. Derivatized lamellar phosphates and phosphonates of M(IV) ions[J]. Inorg Chem, 1981, 20(1): 92-97.
[10] ALBERTI G, MARMOTTINI F, MURCIA MASCAROS S, et al. Computer-generated structural model[J]. Angew Chem Int Ed Engl, 1994, 33: 1594-1597.
[11] 方璐希,喻 鹏,刘灿明. 铝离子和钛离子化学改性MCM-41介孔材料的制备及其对污水中铜离子的吸附性能研究[J]. 化学研究, 2012, 23(1): 29-34.
[12] KADIRVELU K, THAMARAISELVI K, NAMASIVAYAM C. Removal of heavy metals from industrial wastewaters by adsorption onto activated carbon prepared from an agricultural solid waste [J]. Bioresource Technology, 2001, 76: 63-65.
[13] 郑少平, 李卫平. 活性炭吸附去除重金属研究进展[J]. 山西建筑, 2007, 33(14): 153-155.
[14] 罗道成, 刘俊峰. 腐殖酸树脂处理含 Pb2+、Cu2+、Ni2+废水的研究[J]. 环境污染治理技术与设备, 2005, 6(10): 73-76.
[15] ZHANG Xue Jun, MA Tian Yi, YUAN Zhong Yong, Titania phosphonate hybrid porous materials: preparation, photocatalytic activity and heavy metal ion adsorption[J]. J Mater Chem, 2008, 18: 2003-2010.
[16] MA Tian Yi, ZHANG Xue Jun, GAO Song. et al. Ordered macroporous titanium phosphonate materials: synthesis, photocatalytic activity, and heavy metal Ion adsorption[J]. J Phys Chem C: 2008, 112(8): 3090-3096.
[17] 钟 宏. 烷胺双甲基膦酸的合成与性能研究[J]. 有色金属,1994,5: 32-36.
[18] JIA Yun Jie, ZHANG Yue Juan, XU Qing Hong, et al. Studies on adsorptions of metallic ions in water by zirconium glyphosate (ZrGP): behaviors and mechanisms[J]. Applied Surface Science, 2012, 258: 2551-2561.
[19] WU Zong Bin, LIU Zhong Min, TIAN Peng, et al. Template-assisted syntheses of two novel porous zirconium methylphosphonates[J]. Micropor Mesopor Mater, 2005, 81: 175-183.
[20] LEOFANTI G, PADOVANB M, TOZZOLAC G, et al. Surface area and pore texture of catalysts[J]. Catalysis Today,1998, 41: 207-219.
[21] XU Qing Hong, ZHANG Yue Juan, YI Jian Jun, et al. Synthesis and properties of zirconium glyphosate and monochromatic zirconium glyphosate Eu[J]. Micropor Mesopor Mater, 2009, 119: 68-74.
[22] HARRISON D E, MCKINSTRY H A, HUMMEL F A. High-temperature zirconium phosphates[J]. J Am Ceram Soc, 1954, 37: 277-288.
[23] 赵学庄. 阳离子半径的计算[J]. 化学学报, 1980, 38(3): 207-212.
[24] ROSSI M, BAUSCHLICHER C W. The binding energies of one and two water molecules to the first transition row metal positive ions[J]. J Chem Phys, 1990, 92(3): 1876-1878.
[25] RICORDEL S, TAHA S, CISSE I, et al. Heavy metals removal by adsorption onto peanut husks carbon: characterization, kinetic study and modeling[J]. Sep Purif Technol, 2001, 24(3): 389-401.
