几种姜黄素类1,4-戊二烯-3-酮衍生物的合成及结构表征
2013-11-21郭亚宁
郭亚宁
(宝鸡文理学院 化学化工学院,陕西 宝鸡 721013)
姜黄素(curcumin,图1)是姜科植物的根茎中一种具有抗氧化作用的天然化合物,是植物界很稀少的二酮类色素,其分子量小,结构简单,活性广谱,对正常组织细胞毒性小[1-2]. 但由于姜黄素结构中两个羰基之间的活性亚甲基的存在,导致其在pH>6.5时不稳定,抗氧化性降低. 为了得到更加稳定且保持较好生物活性的化合物,研究者在姜黄素结构基础上省略活性亚甲基和一个羰基后,设计、合成了一系列姜黄素衍生物,研究表明其结构稳定性及生物活性均有所提高[3-5].
1,4-戊二烯-3-酮作为天然姜黄素类似物,有广泛的生物活性,有关该类分子设计、合成和生物活性的研究引起了化学及生物学研究者的关注,研究表明这类化合物具有抗癌、抗氧化、消炎、抑制HIV-1 等重要的生物活性[6-9]. 含芳基结构的1,4-戊二烯-3-酮化合物具有高效、低毒、环境友好等特点,受到了广泛的关注. 为了寻找更多的具有生物活性的姜黄素衍生物,作者根据亚结构连接法,在1,4-戊二烯-3-酮结构中引入噻吩基、苯基和呋喃基,设计合成了3类新化合物,1,5-二取代噻吩基-1,4-戊二烯-3-酮类化合物(Ⅰ)、1,5-二取代苯甲基-1,4-戊二烯-3-酮类化合物(Ⅱ)和1,5-二取代呋喃基-1,4-戊二烯-3-酮类化合物(Ⅲ),并对所合成的化合物用1H NMR、13C NMR、IR和元素分析法进行了结构表征.
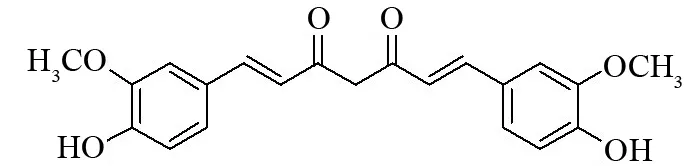
图1 姜黄素的结构式Fig.1 The structure of curcumin
1 实验部分
1.1 仪器与试剂
Bruker AM-400 超导核磁共振仪(瑞士Bruker公司)、Nicolet 170SX FT-IR 红外光谱仪(KBr压片)(上海分析仪器有限公司)、PE-2400元素分析仪(德国PE公司)、X4熔点测定仪(温度计未校正). 3-甲基-2噻吩基甲醛(百灵威科技有限公司)、苯甲醛(百灵威科技有限公司).
1.2 标题化合物的合成
化合物Ⅰa的合成路线如图2所示,化合物Ⅰa的合成步骤为:.
在 500 mL 三口瓶中加入12.79 g(0.10 mol)3-甲基-2-噻吩基甲醛,3.5 g(0.06 mol)丙酮,50 mL乙醇,搅拌数分钟使固体溶解;控制反应温度在 0~5 ℃,然后向其中缓慢滴加8% NaOH溶液120 mL;滴加完毕后继续搅拌,使溶液在室温下继续反应8 h,静置,抽滤,固体用水洗至中性得到浅黄色产物;用无水乙醇重结晶,得纯品. 采用类似方法得到化合物Ib~Ic,Ⅱa~Ⅱc和Ⅲa~Ⅲc.
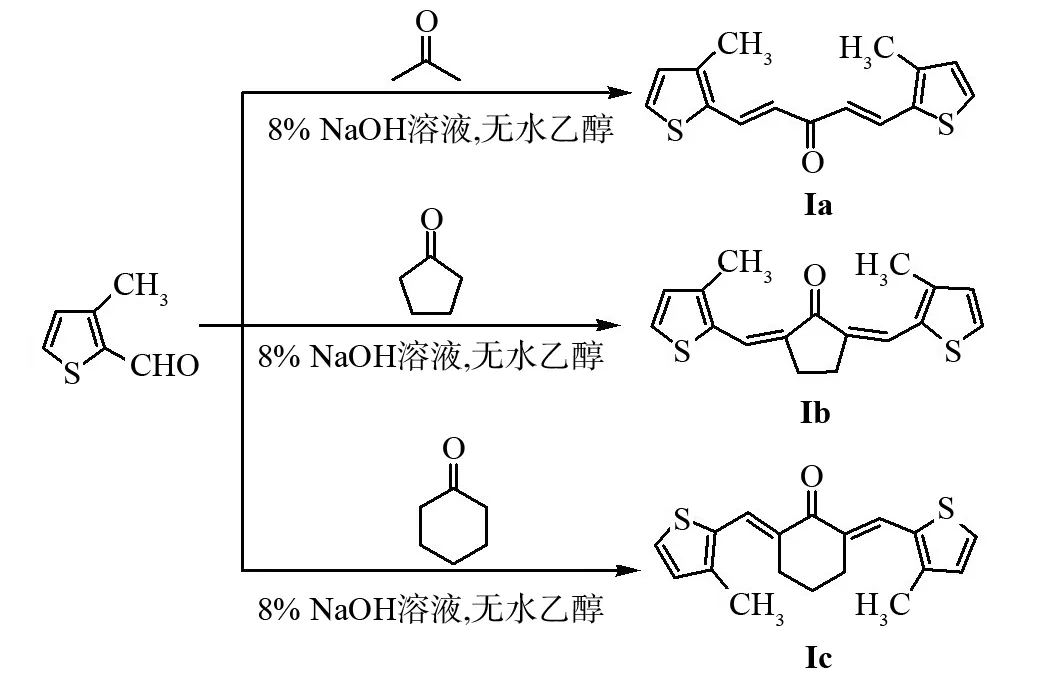
图2 1,5-二噻吩基-1,4-戊二烯-3-酮(Ia~Ic)的合成反应式Fig.2 Synthesis reaction of 1,5-dithienyl-1,4-pentadien-3-one(Ia~Ic)
1,5-二(3′-甲基-2′-噻吩基)-1,4-戊二烯-3-酮(Ia):黄色固体粉末,产率44.7%; mp 140~143 ℃;1H NMR (CDCl3, 400 MHz)δ: 7.66 (d,J=15.8 Hz, 2H, thienyl-CH=), 7.03 (d,J=16.08 Hz, 2H, =CH-C=O), 7.09~7.48 (m, Ar-H), 2.21 (s, 6H, 2CH3);13C NMR (CDCl3,100 MHz)δ: 188.6, 141.7, 139.2, 131.0, 130.4, 126.0, 12.0; IR (KBr,cm-1): 3 145.9, 3 080.3, 3 049.4, 1 665.0, 1 563.3. Anal. calcd for C15H14S2O(%): C 65.69, H 5.11; found(%): C 65.57, H 5.84.
2,5-二(3′-甲基-2′-噻吩基)亚甲基环戊酮(Ib):淡黄色固体粉末,产率42.3%,mp 200~203 ℃;1H NMR (CDCl3, 400 MHz)δ: 6.98 (d,J=16.02 Hz, 2H, thienyl-CH=), 7.07~7.49 (m, Ar-H), 2.20 (s, 6H, 2×CH3), 2.00 (m, 4H of cyclopentanone);13C NMR (CDCl3,100 MHz)δ: 196.6, 149.6, 142.1, 139.2, 131.0, 130.4, 126.0, 35.4, 12.0. Anal. calcd for C17H16S2O(%): C 68.00, H 5.33; found(%): C 68.08, H 5.15.
2,6-二(3′-甲基-2′-噻吩基)亚甲基环己酮(Ic):暗黄色晶体,产率41.5%,mp 98~101 ℃;1H NMR (CDCl3, 400 MHz)δ: 7.38 (d,J=16.30 Hz, 2H, thienyl-CH=), 7.09~7.46 (m, Ar-H), 2.21 (s, 6H, 2×CH3), 1.96 (m, 4H of cyclohexanone), 1.36(m, 2H of cyclohexanone);13C NMR (CDCl3,100 MHz)δ: 186.1, 143.2, 141.5, 139.2, 131.0, 130.4, 126.0, 27.4, 26.7, 12.2. Anal. calcd for C18H18S2O(%): C 68.79, H 5.73; found(%): C 68.55, H 5.87.
化合物Ⅱ及Ⅲ的合成方法同Ia,合成路线如图3和图4所示.
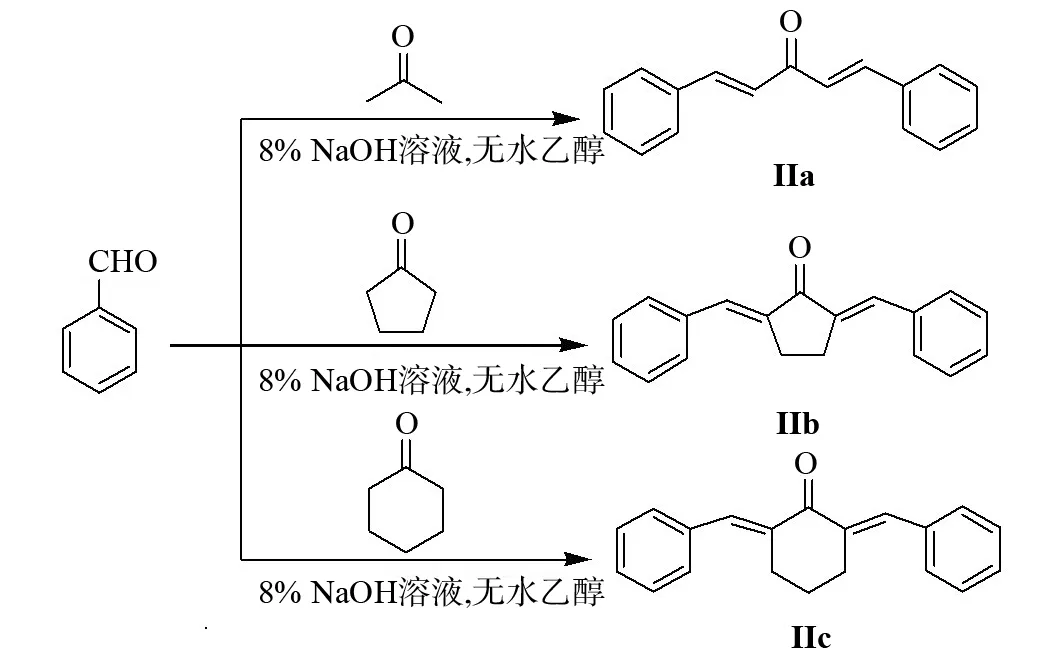
图3 1,5-二苯基-1,4-戊二烯-3-酮(Ⅱa~Ⅱc )的合成反应式Fig.3 Synthesis reaction of 1,5-diphenyl-1,4-pentadien-3-one(Ⅱa~Ⅱc)
1,5-二苯基-1,4-戊二烯-3-酮(Ⅱa):黄色片状晶体,产率47.8%,mp 113~116 ℃;1H NMR (CDCl3, 400 MHz)δ: 7.66 (d,J=7.83 Hz, 2H, phenyl-CH=), 7.03 (d,J=6.7 Hz, 2H, =CH-C=O), 7.14~7.30 (m, Ar-H).13C NMR (CDCl3,100 MHz)δ: 188.6, 152.6, 135.2, 128.7, 128.0, 126.4, 123.4; IR (KBr,cm-1): 3 145.9, 3 080.3, 3 049.4, 1 633.7, 1 563.3. Anal. calcd for C17H14O(%): C 87.18, H 5.98; found(%): C 87.15, H 6.01.
2,5-二苯基亚甲基环戊酮(Ⅱb):淡黄色固体粉末,产率45.6%,mp 188~191 ℃;1H NMR (CDCl3, 400 MHz)δ: 7.38 (d,J=7.75 Hz, 2H, phenyl-CH=), 7.14~7.30 (m, Ar-H), 2.00 (s, 4H of cyclopentanone);13C NMR (CDCl3,100 MHz)δ: 196.6, 146.0, 143.6, 135.2, 128.7, 128.0, 126.4, 29.4; IR (KBr,cm-1): 3 061.0,3 042.1, 2 922.2, 1 635.7, 1 595.1, 1 411.9. Anal. calcd for C19H16O(%): C 87.69, H 6.15; found(%): C 87.71, H 6.11.
2,6-二苯基亚甲基环己酮(Ⅱc):淡黄色晶体,产率38.1%,mp 131~134 ℃;1H NMR (CDCl3, 400 MHz)δ: 7.38 (d,J=7.60 Hz, 2H, phenyl-CH=), 7.14~7.30 (m, Ar-H), 1.96 (m, 4H of cyclohexanone), 1.37(m, 2H of cyclohexanone);13C NMR (CDCl3,100 MHz)δ: 186.1, 145.4, 137.2, 135.2, 128.7, 128.0, 126.4, 27.4, 26.7; IR (KBr,cm-1):3 061.0,3 042.1, 2 922.2, 1 635.7, 1 595.1, 1 411.9. Anal. calcd for C20H18O(%): C 87.59, H 6.57; found(%): C 87.54, H 6.62.
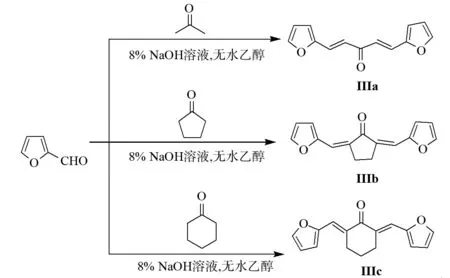
图4 1,5-二呋喃基-1,4-戊二烯-3-酮(Ⅲa~Ⅲc)的合成反应式Fig.4 Synthesis reaction of 1,5-difuryl-1,4-pentadien-3-one(Ⅲa~Ⅲc)
1,5-二呋喃基-1,4-戊二烯-3-酮(Ⅲa):黄色晶体2.0 g,产率47.5%,mp 148~151 ℃;1H NMR (CDCl3, 400 MHz)δ: 7.66 (d,J=15.8 Hz, 2H, furyl-CH=), 7.03 (d,J=16.08 Hz, 2H, =CH-C=O),6.65~7.80 (m, Ar-H);13C NMR (CDCl3,100 MHz)δ: 187.0(-C=O), 150.3, 135.6, 155.3, 145.0, 112.7, 111.8; IR (KBr,cm-1): 3 035.3, 2 997.6, 1 652.7(-C=O), 1 563.3;Anal. calcd for C13H10O3(%): C 72.9, H 4.67; found(%): C 73.5, H 4.63.
2,5-二呋喃基亚甲基环戊酮(Ⅲb):黄色晶体2.3 g,产率47.6%,mp 150~153 ℃;1H NMR (CDCl3, 400 MHz)δ: 6.98 (d,J=16.01 Hz, 2H, furyl-CH=), 6.65~7.80 (m, Ar-H), 2.00 (m, 4H of cyclopentanone);13C NMR (CDCl3,100 MHz)δ: 187.0(-C=O), 149.6, 142.1,155.3, 145.0, 112.7, 111.8, 26.8; IR (KBr,cm-1): 3 120.6, 3 007.3, 1 655.0(-C=O), 1 560.3;Anal. calcd for C15H12O3(%): C 75.00, H 5.00; found(%): C 74.96, H 5.04.
2,6-二呋喃基亚甲基环己酮(Ⅲc):黄色晶体3.4 g,产率40.1%,mp 165~168 ℃;1H NMR (CDCl3, 400 MHz)δ: 7.38 (d,J=15.95 Hz, 2H, furyl-CH=), 6.65~7.80(m, Ar-H), 1.96 (m, 4H of cyclohexanone), 1.37(m, 2H of cyclohexanone);13C NMR (CDCl3,100 MHz)δ: 187.0(-C=O), 141.5,155.3, 150.3, 145.0, 112.7, 111.8, 26.4, 25.0; IR (KBr,cm-1) : 3 010.4, 2 989.5, 1 648.6(-C=O), 1 552.3;Anal. calcd for C16H14O3(%): C 75.59, H 5.51; found(%): C 75.64, H 5.45.
2 结果与讨论
2.1 反应机理的讨论
标题化合物的合成反应属于羟醛缩合反应机理,即亲核加成-消去机理. 以苯甲醛和丙酮的反应为例来进行机理讨论. 首先在碱作用下,丙酮(a)失去弱酸性的α-H形成碳负离子(b),其次此碳负离子(b)与苯甲醛(c)羰基发生亲核加成反应,继而水合形成β-羟基酮(e),最后(e)分子内脱水,生成1,5-二取代苯基-1,4-戊二烯-3-酮(f). 其反应机理见图5.
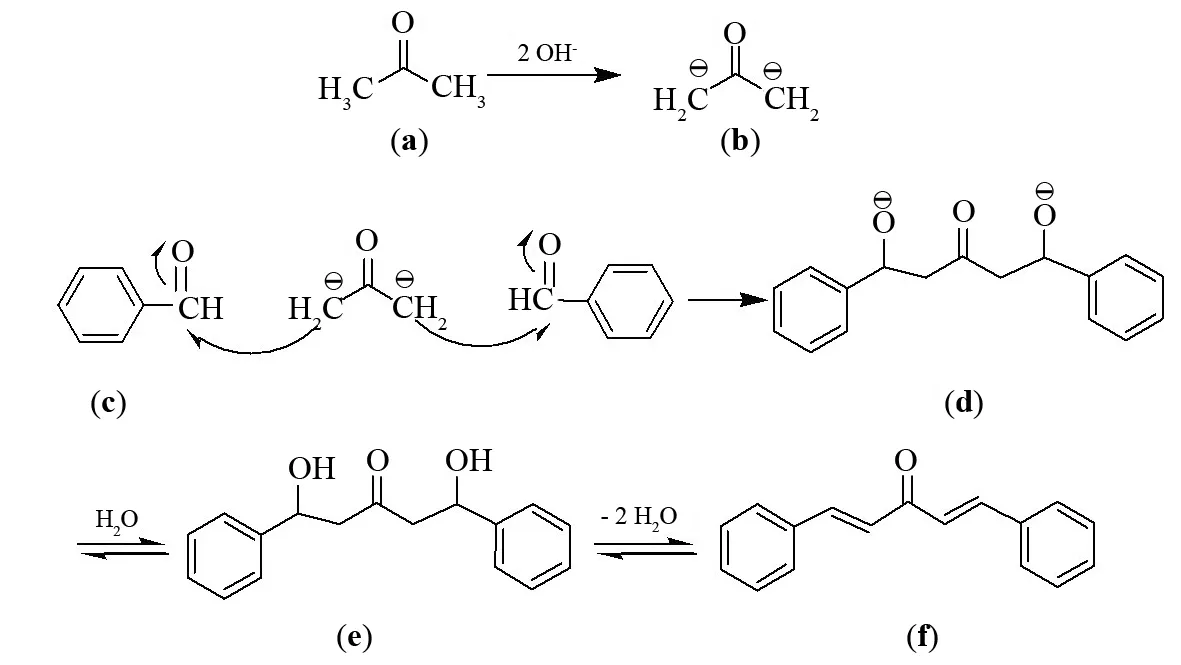
图5 标题化合物的合成反应机理Fig.5 The reaction mechanism of the title compound
2.2 反应条件的讨论
芳醛和含α-H的酮(丙酮、环戊酮和环己酮)在碱催化下,发生羟醛缩合反应. 其过程简便,快速. 只要控制好反应条件,就会得到较高的产率,副产物较少.
以化合物Ⅱa的合成为例采用单因素法对其反应条件进行讨论.
2.2.1 反应时间的选择
取一定量的反应物与溶剂无水乙醇混合,在室温下反应,反应产率随反应时间的变化如图6所示,可以看出,反应时间以8~9 h为宜.
2.2.2 催化剂浓度的选择
取一定量的反应物与溶剂无水乙醇混合,在室温下反应,反应产率随催化剂浓度的变化如图7所示,可以看出,催化剂NaOH的浓度以8%~10%为宜.
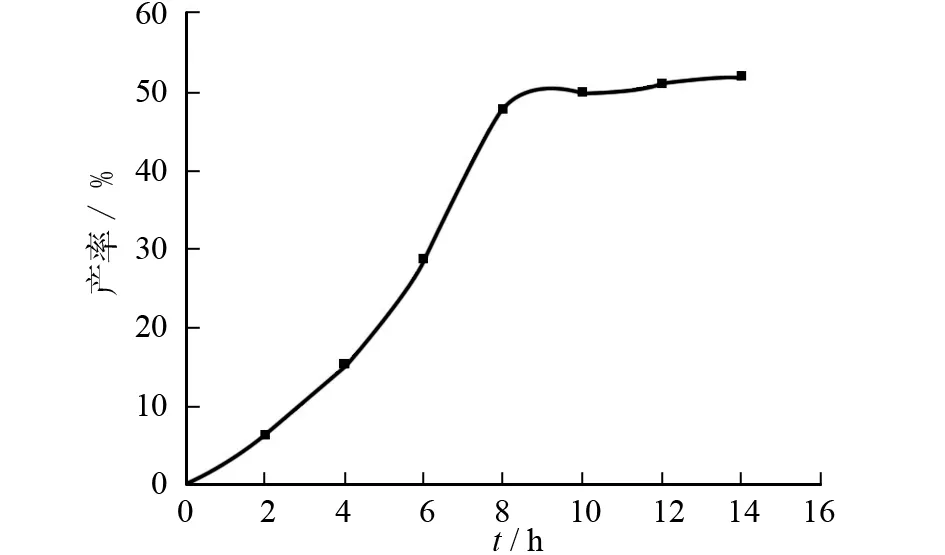
图6 反应时间对Ⅱa产率的影响Fig.6 Effect of reaction time on the yield of Ⅱa
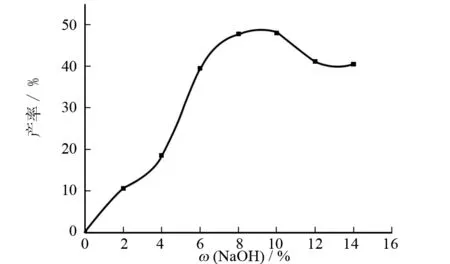
图7 催化剂NaOH浓度对Ⅱa产率的影响Fig.7 Effect of the concentration of catalyst NaOH on the yield of Ⅱa
通过实验对化合物的合成进行探讨,选出较为合适的反应条件为:以无水乙醇为溶剂,8%NaOH溶液为催化剂,分别在室温下反应8 h,收率为38.1%~47.87%. 此反应成败的关键是催化剂的浓度与用量. 碱的浓度太低反应效果不好,碱的浓度太高,会引起芳醛发生歧化反应,导致产率降低.
3 结论
设计合成了3类新的1,5-二芳基-1,4-戊二烯-3-酮类化合物,采用元素分析、IR、1H NMR及13C NMR对其结构进行了表征,并对其反应机理及其反应条件进行了初步探讨,所合成化合物的生物活性有待进一步研究.
参考文献:
[1] 王 牧, 阮余霞, 彭 元, 等. 姜黄素对人肝癌HepG2细胞毒性的分析[J]. 分析测试学报, 2011, 30(2):121-127.
[2] 梁 广, 田吉来, 邵丽丽, 等. 姜黄素的构效关系及以其为先导物的抗肿瘤化合物研究进展[J]. 化学通报, 2008, 4(2):110-117.
[3] 薛海鹏, 李湘洲, 旷春桃. 姜黄素的抗氧化机制及以其为先导物的抗氧化化合物研究进展[J]. 食品科学,2010, 31(07):302-307.
[4] 赵承光, 梁 广, 邵丽丽, 等. 姜黄素类化合物抗炎和细胞保护作用的构效关系研究进展[J]. 中草药, 2008, 39(4):619-622.
[5] 李少博, 胡德禹, 宋宝安, 等. 新型1,5-二苯基-1,4-戊二烯-3-酮肟酯类化合物的合成及其抑菌活性研究[J]. 有机化学, 2008, 28(2):311-316.
[6] 王振宁, 胡德宇, 宋宝安, 等. 1,5-二取代吡唑基-1,4-戊二烯-3-酮类化合物的合成及生物活性研究[J]. 有机化学, 2009, 29(09):1412-1418.
[7] WEBER W M, HUNSAKER L A, ROYBAL C N, et al. Activation of NFKB is inhibited by curcumin and related enones [J]. Bioorg Med Chem, 2006, 14(7):2450-2461.
[8] SELVAM C, JACHAK S M, THILAGAVATHI R, et al. Design, synthesis, biological evaluation and molecular docking of curcumin analogues as antioxidant, cyclooxygenase inhibitory and antiinflammatory agents [J]. Bioorg Med Chem Lett,2005, 15(7):1793-1796.
[9] 黄文待, 黄君成. 研究利用醛-酮缩合反应合成-4-甲氧基查尔酮和1,5-双(4′-甲氧基苯基)-1,4-戊二烯-3-酮[J]. 化学试剂, 1990, 12(3):180-181.
