新型双核Co(Ⅱ)聚合物{[Co2L(MeOH)(H2O)4]n·nH2O}的合成及其晶体结构*
2013-11-19张义东郭晶晶张淑华
杨 莉, 王 娓, 张义东, 郭晶晶, 张淑华, 海 洪
(桂林理工大学 化学与生物工程学院 广西高校应用电化学重点实验室,广西 桂林 541004)
过渡金属聚合物具有明确有序的一维或者多维微观结构以及独特的宏观特性,选取适当的过渡金属离子、配体以及合成方法可调控配位聚合物的结构,进而调控其性质[1~4]。其中,通过选择适宜的配体和金属离子或金属簇,控制影响自组装的各种微妙因素,合成具有新奇拓扑结构的金属-有机超分子,如一维链、梯子、方块、蜂窝等,为开发新型功能材料提供了丰富的研究素材,近十年得到了学术界的广泛重视[5~8]。但是在设计和合成金属有机骨架时,控制维度仍然是一个难题。除了溶剂、温度、金属与配体的配比、模板和平衡电荷的离子外,最终的结构还会受到如氢键和π-π相互作用[9]等因素的微妙影响。尽管配体的空间结构对配合物领域和催化活性金属中心有巨大的影响力,但其影响力在超分子结构方面还没有得到充分的重视[10,11]。而羧酸除了具有多种多样的配位模式可以满足多种金属离子配位能力、模式、配位角度等需要外,还能形成强的氢键[12],使其研究得到迅速发展,在超分子化学的研究中受关注,在分子识别、催化、吸附等方面均有较好的应用[13]。
溶剂热法是近年来发展起来的一种配合物合成新方法,常用来合成一般溶液法难以合成的配位聚合物。本文采用溶剂热法,在甲醇及丁烷四羧酸(H4L)配体体系中,通过配位聚合反应合成了一个新型的配位聚合物[Co2L(MeOH)(H2O)4]n·nH2O(1),其结构经元素分析和单晶X-射线衍射表征。Co(Ⅱ)通过H4L桥联形成一维状结构,通过O-H┈O氢键将每条链连接起来,形成了无限延伸的二维网络结构。1中存在广泛的分子内及分子间氢键其具有超分子网络结构。
1 实验部分
1.1 仪器与试剂
Vario EL Ш型元素分析仪;Bruker Smart CCD型X-射线单晶衍射分析仪。
H4L,国药集团化学试剂有限公司;四水乙酸钴和无水甲醇,汕头市西陇化工厂;其余所用试剂均为分析纯。
1.2 合成
在反应瓶中加入H4L 234 mg(1 mmol)和四水乙酸钴249 mg(1 mmol)的50%甲醇(20 mL)溶液,搅拌下滴加5滴三乙胺,密封搅拌15 min后装入25 mL内衬聚四氟乙烯不锈钢反应釜内(填充度80%),采用程序升温法于160 ℃反应120 h。以10 ℃·h-1降温速率降至室温,出现紫红色块状晶体,抽滤,滤饼用无水甲醇洗涤,于40 ℃恒温真空干燥2 h得紫红色晶体1,收率56%(以Co计); Anal.calcd for C9H19O14Co2: C 23.03, H 4.05; found C 23.14, H 3.97。
1.3 晶体结构测定
将1单晶(0.27 nm×0.18 nm×0.09 nm)置面探衍射仪上作晶体分析,采用单色化的MoKα射线(λ=0.071 073 nm),于293 K以ω-2θ扫描方式在2.51°≤θ≤25.01°收集数据,并进行 Lp 因子校正并做经验吸收校正。晶体结构用直接法解出,全部非氢原子的坐标及各向异性参数经最小二乘修正,用SHELXL-97[14,15]程序以最小二乘法对F2进行修正,氢原子由差值Fourier合成和理论计算得到,所有或部分氢原子的坐标和各向同性温度因子参加结构计算。1的晶体学数据见表1。

表1 1的晶体学参数Table 1 Crystallographic data of 1
2 结果与讨论
1的分子结构见图1,晶胞堆集图见图2,部分键长和键角见表2,氢键键长和键角见表3。
从图1可以看出,1是双核钴层状配位聚合物,根据总的价态, 电荷平衡以及当前典型的Co(Ⅱ)的键长[16,17],每个钴离子的化合价都是+2。在1中,每个Co离子通过H4L的桥联作用连成一条链,其中Co离子都处于畸变的六配位八面体环境中,Co1与四个不同H4L上的羧基氧原子[O1, O3, O5和O7]配位,与水分子上的氧原子(O10)以及甲醇分子中的氧原子(O9)配位,Co1-O键长为0.208 0(9) nm~0.214 3(9) nm, O-Co1-O键角在85.7(4)°~175.6(4)°。 Co2同样具有畸变的六配位八面体几何构型。Co2与三个配位水分子的三个氧原子和两个羧基上的两个氧原子配位,Co2-O的平均键长为0.210 2(11) nm,而O-Co2-O的键角在85.7(4)°~173.1(4)°。每个配位中心CoO可以看作为一个畸变的三角双锥几何构型,其中O3, O5与O10(O6, O2与O13)位于赤道平面上,O1和O7(O2和O11)分别位于两个顶点位置。 O1, O7, O2和O11到平面Co1-O3-O7-O10和Co2-O6-O12-O13的距离相近,分别为0.208 65 nm, 0.210 46 nm, 0.206 46 nm, 0.211 15 nm。作为一个重要的桥联基团[Co1-O9-Co2, 112.1(4)°]在一定程度上增大了1的稳定性。同时,全部的羧基基团都呈现双齿桥连的配位模式,每个Co1和Co2中心通过甲醇分子中的氧原子桥连形成了无限延伸的二维网络结构。1中存在广泛的分子内及分子间氢键使其具有超分子网络结构。
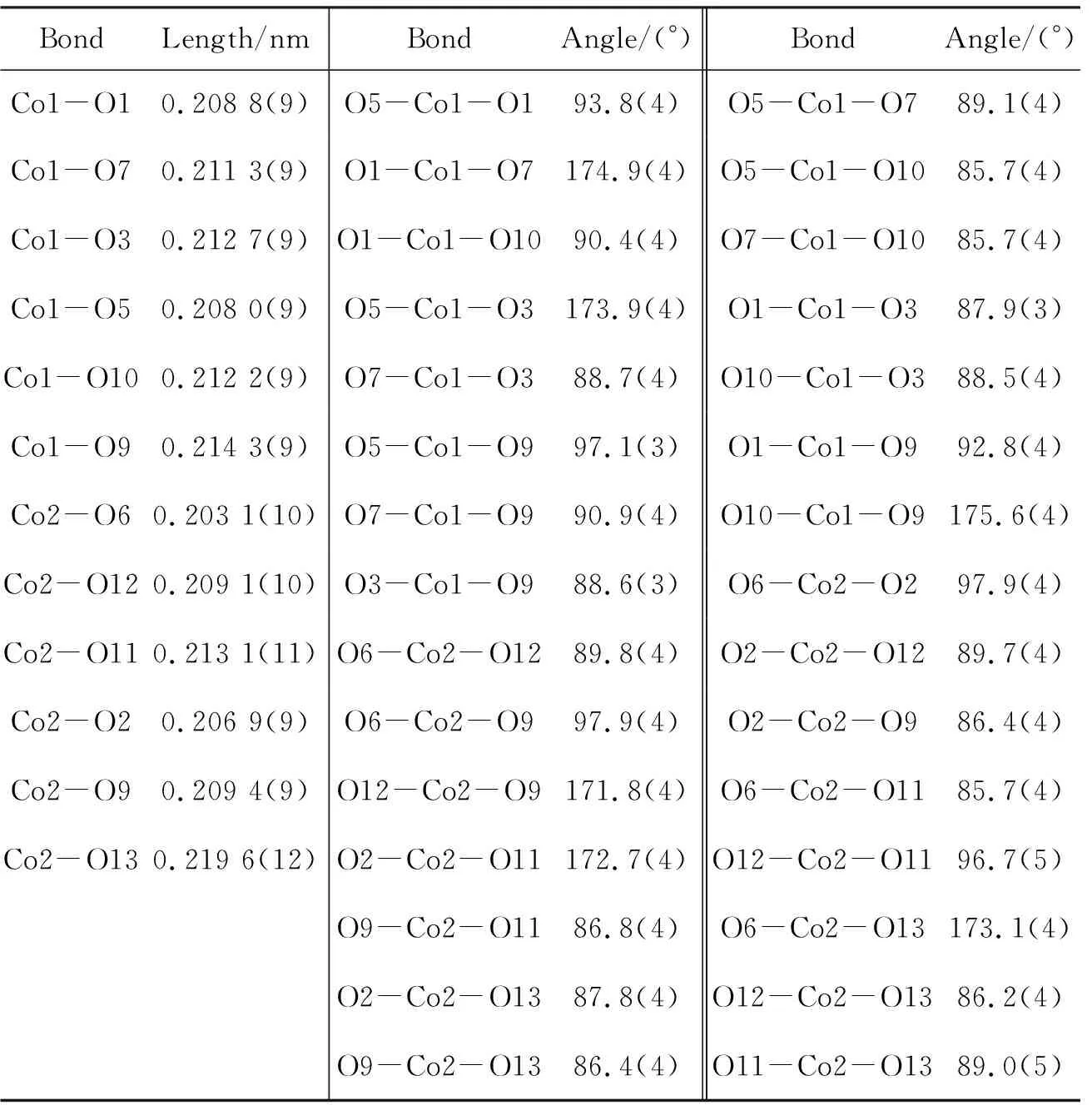
表 2 1的部分键长和键角Table 2 Selection bond lengths and angles of 1
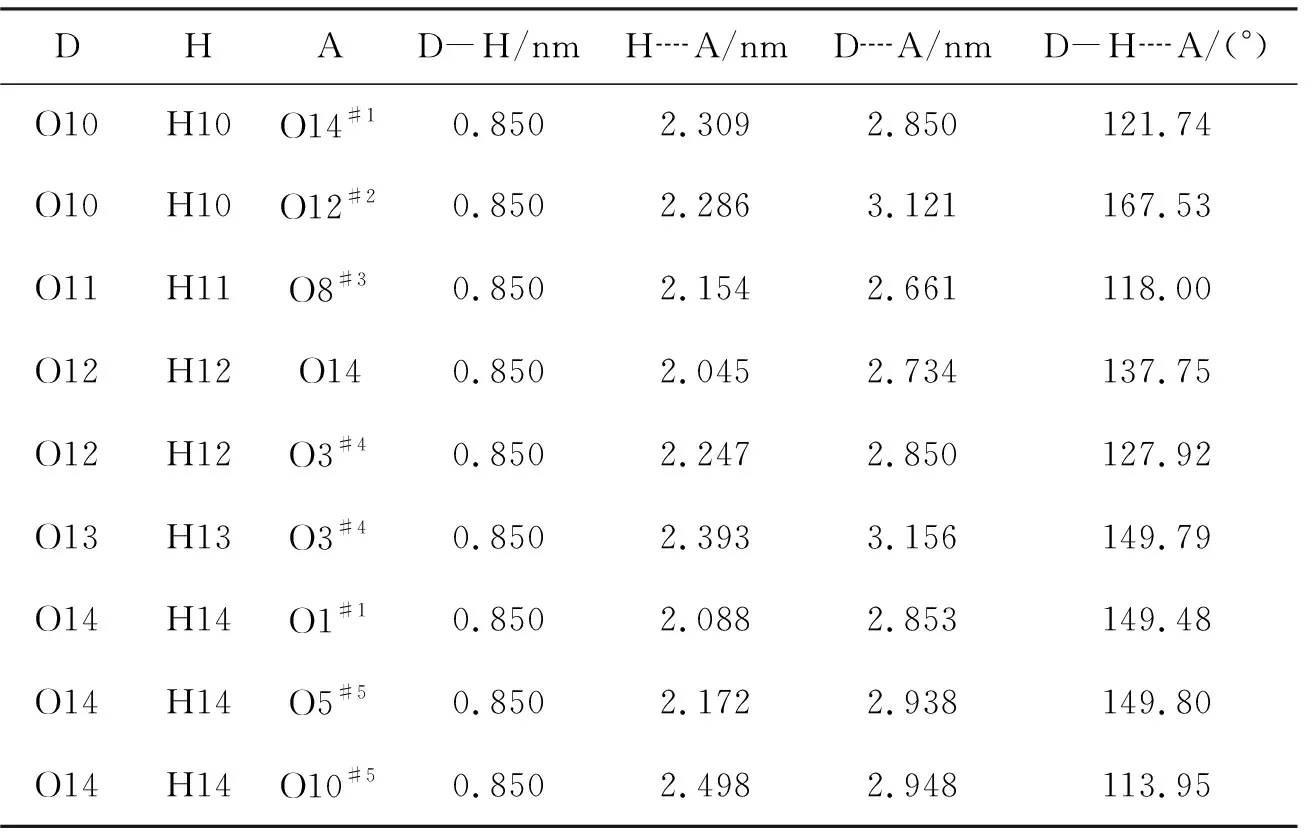
表 3 1的氢键键长和键角Table 3 Hydrogen bond lengths and bond angles of 1
#1-x+1/2, -y+1/2, -z+2;#2x, -y, z+1/2;#3-x, y, -z+3/2;#4x, -y, z-1/2;#5x, -y+1, z-1/2
由图2可见1簇合的堆积情况,离散的簇与簇之间通过大量的分子内与分子间氢键等弱作用相互连接三维网络结构。
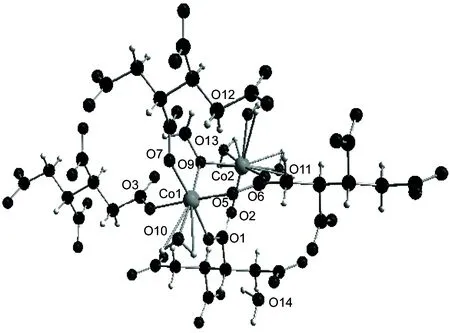
图 1 1的分子结构图Figure 1 Molecular structure of 1
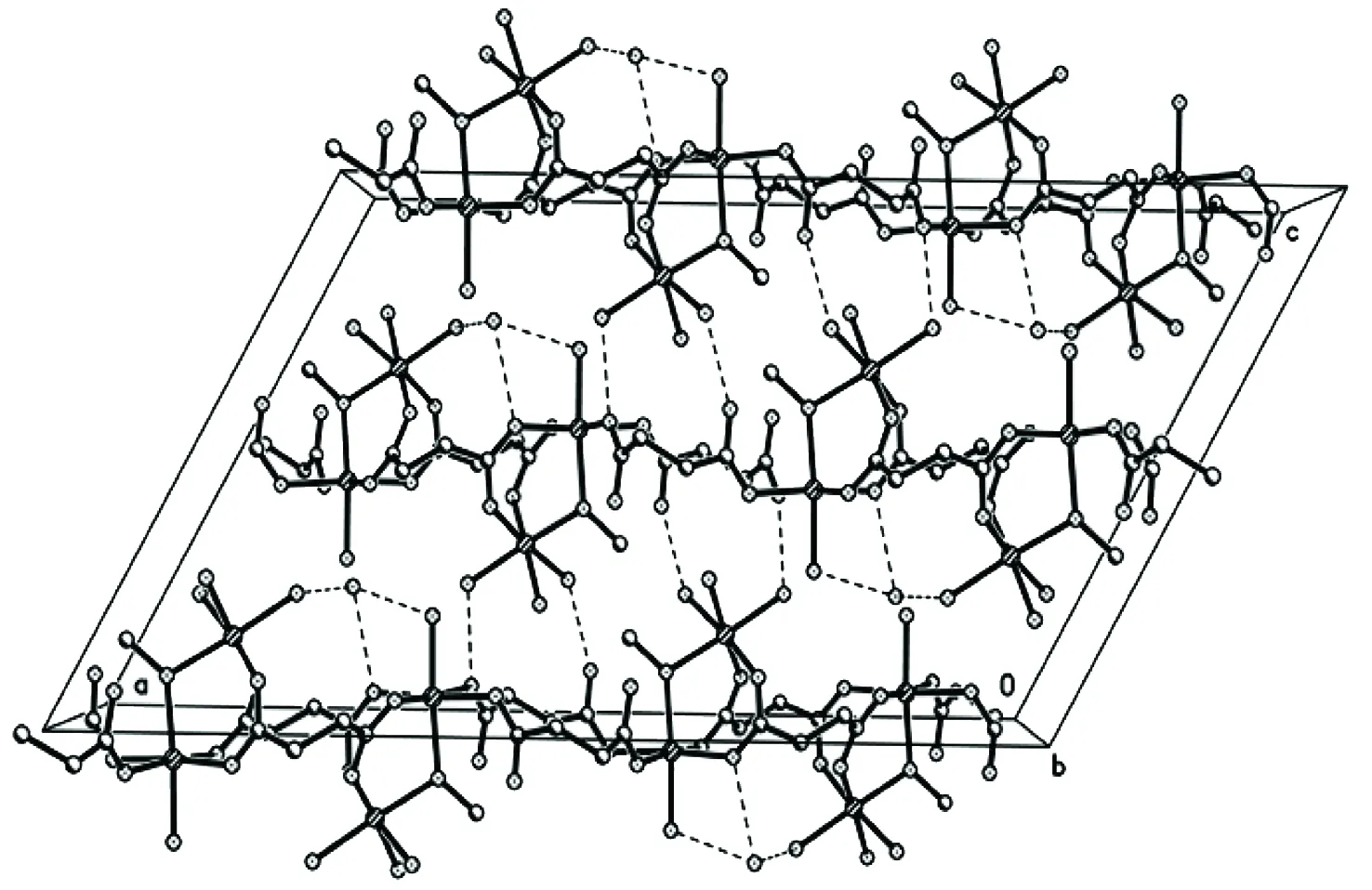
图 2 1沿b轴方向的堆积图Figure 2 The stacking diagram of 1 as viewed along b axis
3 结论
合成了一种新型的具有μ2-OH桥连结构的Co(Ⅱ)配位聚合物[Co2L(MeOH)(H2O)4]n·nH2O。晶体结构分析表明,以每个中心Co(Ⅱ)为中心均形成了六配位的稍微扭曲的八面体几何构型,其通过O-H┈O氢键作用形成了无限延伸的二维网络结构,分子内和分子间的氢键作用,使得配合物堆积形成三维超分子,并增强晶体稳定性。
[1] Mörgenstern B, Steinhäöser S, Hegetschweiler K,etal. Complex formation of vanadium(Ⅳ) with 1,3,5-triamino-1,3,5-trideoxy-cis-inositol and related ligands[J].Inorg Chem,2004,43:3116-3126.
[2] Chiang R K. Synthesis and structure o f a one-dimensional cobalt phosphate (R,S)-(C5H14)Co(HPO4)2[J].J Slid State Chem,2000,153:180-184.
[3] Ye B H, Tong M L, Chen X M. Metal-organicmolecular architectures with 2,2-bipyridyl like and carboxylate ligands[J].Coord Chem Rev,2005,249:545-565.
[4] Sun D F, Ke Y X, Mattox T M,etal. Temperature dependent supramolecular stereoisomerism in porous copper coordination networks based on a design carboxylate ligand[J].Chem Commun,2005,43:5477-5449.
[5] James S L. Metal-organic frameworks[J].Chem Soc Rev,2003,32(5):276-279.
[6] Rowsell J L, Yanhi O M. Straegies for hydrogen storage in metal-organic frameworks[J].Angew Chem Int Ed,2005,44:4670-4673.
[7] Janiak C. Engineering coorination polymers towards applications[J].Dalton Trans,2003,14:2781-2804.
[8] Mäspöch D, Rüiz D, Veciänä J. Old materials with new tricks:Multifunct open-framework materials[J].Chem Soc Rev,2007,36(5):770-818.
[9] Zhao B, Cheng P, Chen X Y,etal. Design and synthesis of3d~4fmetal basedzeo lite-type material is with a 3D nanotubular structure encapsulated water pipe[J].J Am Chem Soc,2004,126:3012-3013.
[10] Zhang J P, Chen X M. Crystal engineering of binarymetal imidazolate and triazolate frameworks[J].Chem Commum,2006,16:1689-1699.
[11] Kim J, Chen B, Reineke T M,etal. Assembly of metal-inorganic frameworks from large organic and inorganic secondary building units:New examples and simplifying principles for complex structures[J].J Am Chem Soc,2001,123:8239-8247.
[12] Yaghi O M, Li H L, Groy T L. Construction of porous solids from hydrogen-bonded metal complexs of 1,3,5-benzenetriearboxylie acid[J].J Am Chem Soc,1996,1118(38):9096-9101.
[13] Marder S R, Sohn J E, Stuchy G D. Materials for nonlinear optics chemical perspectives[J].American Chemical Society,Washington,DC,1992,91:626-634.
[14] SIEMENS. SAINT. Area Detector Control and Integration Software,Siemens Analytiacl X-ray Instruments Inc[M].Madison,WI,USA,1996.
[15] SHELDRICK G M, SADABS. Program for Empirical Absorption Correction of Area Detector Data[K].University of Göttingen:Germany,1996.
[16] Ama T, Ashid M M, Ysui T. Pentaaquatri-mu(3)-hydroxido-tris(iminodiacetato)-mu(3)-oxidotetrahedrocalcium(Ⅱ) tricobalt(Ⅲ)2.54-hydrate[J].Acta Cryst,2010,E66:M483-M484.
[17] Papk J, Lang K, Abboud K A,etal. Self-assembled dinuclear cobalt(Ⅱ)-salen catalyst through hydrogen-bonding and its application to enantioselective nitro-aldol(Henry) reaction[J].J Am Chem Soc,2008,130:16484-16485.
