绵羊红细胞及补体活性对静注人免疫球蛋白(PH4)抗补体活性测定的影响
2013-11-15崔素梅郝清华高红琴山西康宝生物制品股份有限公司长治046000
崔素梅,郝清华,高红琴(山西康宝生物制品股份有限公司,长治 046000)
静注人免疫球蛋白(PH4)是具有多种生物学活性的血液制品,临床上用于治疗原发性免疫球蛋白缺乏或低下症、原发性血小板减少性紫癜、重症感染、新生儿败血症、川崎病等[1],因此具有广泛的应用价值。临床上常用静脉滴注,静注人免疫球蛋白(PH4)可在短时间内大剂量使用,并迅速进入血液循环,因而发挥作用快,但是一般的IVIG大剂量静脉注射会引起严重的副反应[2],这是由于IVIG制品中存在抗补体活性,当抗补体活性(ACA)大于50%时能激活补体系统,释放过敏毒素 C3a,C5a.因此ACA是IVIG中一项极为重要的指标。据文献[3,4]报道,影响ACA的因素很多,这些因素多是生产过程中引起的,本文所讨论的是外在因素,是可以避免的,为此我们对山西康宝生物制品股份有限公司的3批次IVIG,分别用3个不同地方的绵羊红细胞、补体对照活性不同的补体进行抗补体活性测定,考察这两个重要因素对ACA测定结果的影响,为IVIG抗补体活性测定结果的判定提供参考。
1 仪器与试药
1.1 仪器
双光束紫外可见分光光度计(TU-1901双光束紫外可见分光光度计);高级恒温水浴箱(501型,上海市实验仪器总厂);离心机(LDZS-Z型 ,北京医用离心机厂)。
1.2 试剂
钙镁离子贮备液:称取氯化钙1.103 g、氯化镁(MgCl2·6H2O)5.083 g,加纯化水使溶解成 25 ml,4℃保存备用。巴比妥缓冲贮备液:称取氯化钠41.5 g,巴比妥钠 5.096 g,加 900 ml纯化水使溶解,用1 mol/L盐酸调pH至7.3,加2.5 ml镁-钙储备液,再用纯化水稀释至1 000 ml,4℃保存备用。
明胶巴比妥缓冲液(当日配制)(SGVB):称取明胶0.625 g,加水适量煮沸使溶解,加100 ml巴比妥缓冲贮备液,加纯化水稀释至500 ml,临用前新鲜配制。
阿氏液:称取葡萄糖2.05 g,枸橼酸三钠0.8 g,枸橼酸 0.05 g,氯化钠 0.42 g,加蒸馏水溶解至100 ml,pH6.2 装于 250 ml瓶内,经 10 磅蒸汽消毒10 min(放气要快),备用。
绵羊红血球:由绵羊颈静脉无菌采集全血与等体积的阿氏液混合,无菌分装于试管中,4℃保存1周后方可使用。如未污染细菌4周内均可使用。本试验采用北京、西安、长治3个不同地方的绵羊红血球,分别编号为 A、B、C。
溶血素:兔抗羊红血球血清,批号20112222。豚鼠血清(补体),批号 20120119,20120212,20120526,20120721。
待检样品:静注人免疫球蛋白(PH4)(山西康宝生物制品股份有限公司),批号:20120206,20120413,20120726,规格(5%50 ml)。
2 方法与结果
参照文献[5]的方法进行试验。
2.1 制备5%羊红细胞悬液
取绵羊红细胞,用明胶巴比妥缓冲液至少洗3次,2 000 r/min离心5 min,直至上层清液不显红色,弃去上清液后,20倍悬浮于明胶巴比妥缓冲液中,取0.2 ml血球悬液,加入 2.8 ml纯化水中,摇匀,在541 nm波长处测定OD值。根据下述公式,将该溶液OD值调到0.62±0.01,用此法调节的红细胞浓度为1×109/ml。

上式中,Vi为稀释前血球悬液体积,OD为稀释前血球悬液的OD值,Vf为稀释后血球悬液体积。
照上述方法分别将3个地方的绵羊红细胞分别制成5%的羊红细胞悬液。
2.2 溶血素的滴定
稀释溶血素:取0.1 ml溶血素加9.9 ml SGVB为1∶100 稀释。
先取7支试管,从第2管开始分别加入1 ml SCVB,往第1管、2管中各加1 ml 1∶100倍稀释的溶血素,从第2管中取1 ml混合液加入下一管,以此类推一直到第7管,使之分别为100,200,400,800,1 600,3 200,6 400 倍稀释;另外再取 2 支试管即8号管、9号管分别作为空白管和全溶管,按表1分别加入各项试剂。
37℃放置20 min,冰浴15 min之后,在对应的管内分别加入下列试剂。

表1 溶血素的滴定各成分加入量Tab 1 Input volume of each component for hemolysin titration
混匀,37 ℃ 60 min,冰浴3-5 min,2 000 r/min离心5 min,取上清液于541 nm波长处测定吸收值(OD)值,并计算溶血率。
从表3可知,采用不同地方的绵羊红血球,在溶血素稀释倍数相同和补体相同的条件下,溶血率数据明显不同。

表2 溶血素的滴定各成分加入量 (ml)Tab 2 Input volume of each component for hemolysin titration (ml)
根据表3数据,以Y值做纵坐标,Y=每管OD值/全溶管OD值。以不同溶血素稀释度为横坐标,得到饱和曲线。溶血素适宜稀释倍数为曲线的最高点的稀释度的一半,从而求出敏化羊血球所用的稀释度。试验要求最大溶血应在50%-70%范围,否则试验不成立。
由图1可知,A种绵羊红血球最高点稀释度为200,最大溶血率为60.6%,此批绵羊红血球,符合试验要求。溶血素敏化羊血球所用的稀释度为100。

表3 3个不同地方的绵羊红血球溶血素滴定数据Tab 3 Titration data of the sheep red blood cells from three geographical origins
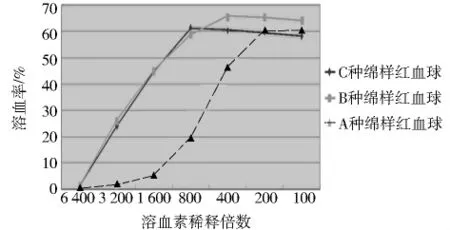
图1 A、B、C三种绵羊红血球不同溶血素稀释度时溶血率Fig 1 Hemolysin dilution of the sheep red blood cells from three geographical origins at different titers
B种绵羊红血球最高点稀释度为400,最大溶血率为65.8%,此批绵羊红血球,符合试验要求。溶血素敏化羊血球所用的稀释度为200。
C种绵羊红血球最高点稀释度为800,最大溶血率为61.4%,此批绵羊红血球,符合试验要求。溶血素敏化羊血球所用的稀释度为400。
2.3 3个地方的绵羊红细胞最适敏化的羊红细胞(EA)的制备
将2.1项下制备的5%的3种绵羊红血球分别量取8 ml,一边轻摇红血球,一边滴入等量的稀释溶血素,37℃放置15 min后,2-8℃保存,6 h内使用。注意红血球不要往溶血素中倒,以免产生溶血。
2.4 滴定补体活性
用明胶巴比妥缓冲液适当稀释补体,一般取500,600,700的稀释倍数,然后按表4滴定补体。
加毕,混匀,37 ℃孵育60 min,0.5 h 摇一次,1 h再摇一次,冰水浴3-5 min,2 000 r/min离心5 min,取上清液于541 nm波长处测量OD值(见表5-7)。

表4 滴定补体活性各成分加入量 (ml)Tab 4 Input volume of each component for complement activity (ml)

表5 A种绵羊红血球滴定补体活性数据Tab 5 The complement activity of the sheep red blood cells of A
表5数据进行双对数回归分析后,可求出直线回归方程的截距(A)、斜率(B)和相关系数(r),补体活性按下式计算,B在0.15-0.40之间表明试验成立,最好的分布范围是0.18-0.30之间。
补体活性=1/X×补体稀释倍数/5,式中:1/X为A值反对数的倒数。
500 稀释倍数:A=-0.226,B=0.188,r=0.998,1/X=1.683,GPC 效价 =1.683 × 500/5=168.3 CH50/ml。
600 稀释倍数:A=-0.142,B=0.207,r=0.999,1/X=1.387,GPC 效价 =1.387 × 600/5=166.4 CH50/ml。
700 稀释倍数:A=-0.074,B=0.208,r=1.000,1/X=1.186,GPC 效价 =1.186 × 700/5=166.0 CH50/ml。
以上三个稀释度的平均效价为:(168.3+166.4+166.0)/3=166.9 CH50/ml。

表6 B种绵羊红血球滴定补体活性数据Tab 6 The complement activity of the sheep red blood cells of B
表6数据双对数回归:500稀释倍数GPC效价=1.928×500/5=192.8 CH50/ml;600 稀释倍数 GPC效价 =1.611 ×600/5=193.3 CH50/ml;700 稀释倍数GPC 效价=1.396 ×700/5=195.4 CH50/ml。以上3个稀释度的平均效价为193.8 CH50/ml。
表7数据双对数回归:500稀释倍数GPC效价=1.816×500/5=181.6 CH50/ml;600 稀释倍数 GPC效价 =1.503 ×600/5=180.4 CH50/ml;700 稀释倍数GPC 效价 =1.294 ×700/5=181.2 CH50/ml。以上三个稀释度的平均效价为181.1 CH50/ml。
从以上A、B、C三种绵羊红血球滴定补体活性数据可知:不同的绵羊红血球滴定相同的补体,得出的补体活性的结果不同。

表7 C种绵羊红血球滴定补体活性数据Tab 7 The complement activity of the sheep red blood cells of C
2.5 抗补体活性测定
根据2.4项下测得的豚鼠血清补体活性,用明胶巴比妥缓冲液稀释至100 CH50/ml,按表8制备培育混合物。

表8 待检样品(20120206)及补体对照加入量的比例Tab 8 Input ratio of samples and complement controls
将表8混合物37℃保温60 min,之后从中取出0.2 ml加入到9.8 ml明胶巴比妥缓冲液中,按滴定补体活性方法测定剩余补体活性。
分别用A、B、C三种绵羊红血球,20120526批补体,测定20120206批IVIG的ACA,按照下列公式计算:待检样品ACA(%)=(a-b)/a×100%,式中,a表示补体对照管剩余补体活性(单位:CH50/ml),b表示待检样品管剩余补体活性(单位:CH50/ml)。待检样品 ACA(%)分别为 25.2%,34.8%和0。
2.6 样品抗补体活性测定
溶血素、绵羊红血球、缓冲液等其他试材料相同,只是补体活性不同,根据2.4项下的方法滴定补体活性
待检样品抗补体活性根据2.5项下的方法测定,结果见表9。
根据表9的测定结果可知,补体活性不同,同一批样品测得的ACA结果差别巨大。
3 讨论
从实验结果可以看出,采集不同地方的绵羊所得到的绵羊红血球,在实验过程中,其他条件相同的情况下,溶血率数据明显不同,因而导致稀释度不同。按这样的结果滴定补体,从而引起补体活性的不同,用以上的结果分别测定同一批样品的ACA值,得到具有较大差别的结果。
在溶血素、绵羊红血球、缓冲液等其他试验材料相同的前提下,根据2.5项的方法测定3批样品中的ACA值,结果表明,补体的活性小于150 CH50/ml,样品ACA易出现假阳性。

表9 不同补体活性测定待检样品的抗补体活性的结果Tab 9 Results of anticomplementary activity of samples
基于在一些特定疾病的预防和治疗上的特殊性,IVIG制品被起来越广泛地用于临床,特别是近10年来临床需求量增加非常快[6]。所以IVIG制品的安全性、有效性十分重要。ACA是制品质量的一项主要指标。为了准确、可靠、及时地检测出数据,为生产提供质量保证,我们应消除实验中的影响因素,在IVIG抗补体活性测定中影响因素很多,需要我们继续探讨,但绵羊红血球和补体的活性是关键因素。
[1] 侯麦花,孙凌云,卢新政.静脉注射用免疫球蛋白的应用及其机制[J].中华风湿病学杂志,2004,8(7):433-435.
[2] 任跃明,程雅琴,倪道明.静脉注射人免疫球蛋白的质量控制[J].中国生物制品学杂志,2005,18(1):73-75.
[3] 刘鹏翰,潘越飞,黎新.静脉注射用免疫球蛋白抗补体活性测定的影响因素探讨[J].药物生物技术,1995,2(4):58-59.
[4] 王宗刚,卢元志,张慧兰.静注人免疫球蛋白抗补体活性测定影响因素的探讨[J].中国医药生物技术,2010,5(3):224-225.
[5] 国家药典委员会.中华人民共和国药典(三部)[M].北京:中国医药科技出版社,2010:附录66-67.
[6] 周海云,江丽君.静注人免疫球蛋白的研究与应用[J].微生物学免疫学进展,2009,37(4):70-73.
