镍(Ⅱ)-吡嗪-2,3-二羧酸配合物的结构及其生物活性
2013-10-30徐晓莹高恩军
焦 韦, 付 虹, 徐晓莹, 高恩军
(1.沈阳化工大学应用化学学院,辽宁沈阳 110142;2.沈阳市无机分子基材料化学(国际)重点实验室,辽宁沈阳 110142)
在过去几年中,配合物的分子结构和生物活性在无机化学领域受到人们更多的关注.镍(Ⅱ)是一种常见的过渡金属,一般具有2种配位形式:四配位和六配位[1-3].镍(Ⅱ)的配位方式取决于配体结构、溶剂和反应条件,其中配体起决定性作用.它不仅可以确定分子结构的复杂性,协调超分子的新颖聚集方式[4-5],还可与 DNA和各种生物活性相互作用[6-10].吡嗪是非常好的桥联配体,金属离子可通过它的轨道重叠达到相互间的电子偶合.因而吡嗪可看做一个潜在的磁交换媒介.羧酸配体也可做为桥联基团为金属提供磁交换作用的途径.然而对于同时将含有这2类基团的吡嗪二羧酸类化合的研究并不常见.本文采用吡嗪-2,3-二羧酸为配体,合成新颖的配合物 Ni[Pyzdc(COO)COOH]2·2H2O 单晶,并通过2个吡嗪-2,3-二羧酸配体以氮原子和氧原子与镍(Ⅱ)离子反式螯合配位.通过X-射线衍射结构分析表明,镍(Ⅱ)形成一个八面体几何形状,通过氢键的弱相互作用使整体结构稳定.应用紫外光谱法和荧光光谱法,初步证实配合物与DNA相互间以插入作用为主.与此同时,又用凝胶电泳法测定配合物对pBR-322质粒DNA的切割能力.
1 实验部分
1.1 试剂和仪器
从商业来源所获得的化学品试剂均为分析纯,不经进一步纯化,直接使用.通过Finnigan EA 1112元素分析仪,Nicolet 470红外光谱仪,Bruker Smart 1000 CCDX射线晶体衍射仪,Shimadzu UV-240紫外-可见分光光度计,Perkin Elmer LS55荧光分光光度计以及JS-380A自动凝胶图像分析仪对配合物的结构、特性以及生物活性进行初步研究.
1.2 配合物的合成
将10 mL浓度为10 mmol/L的硝酸镍水溶液与20 mL浓度为10 mmol/L的吡嗪-2,3-二羧酸水溶液混合,在连续搅拌下,用0.5 mol/L的KOH调节混合溶液pH值为6.3,搅拌8 h后pH值相对稳定为7.52.将该溶液过滤至烧杯中,在室温下放置16 d后有淡绿色晶体析出.
元素分析实测值(%,C12H8N4NiO10计算值):C 33.74(33.76);H 41.86(41.89);N 13.13(13.12).
红外图谱显示(cm-1;s,强峰;m,中峰;w,弱峰):3 404(m);2 360(m);1 636(m);1 609(m);1 438(m);1 395(m);1 129(m);668(m).
2 配合物的晶体结构及弱作用分析
选取尺寸为0.13 mm×0.05 mm×0.08 mm的配合物单晶.在BruckerSmart 1000 CCDX单晶衍射仪上,以经过石墨单色器的Mo-Ka为靶源(λ =0.071 073 nm),在2.84°<2θ<26.02°范围内收集衍射数据.在293 K下,以ω-2θ方式共收集了4 610个衍射数据,其中独立数据1 479个[R(int)=0.0218],-11≤ h ≤ 10,-9≤ k≤9,-12≤ l≤12,R 最终指数(I>2σ(I)):R1=0.036 9,wR2=0.092 8;R 指数(所有数据):R1=0.040 4,wR2=0.095 5.部分配合物键长键角如下:
配合物晶体结构中主要的键长(nm)如下:Ni(1)—N(1):0.204(2)nm;Ni(1)—O(4):0.202(2)nm;Ni(1)—O(5):0.212(2)nm.
配合物晶体结构中主要的键角(°)如下:N(1)—Ni(1)—O(4):79.26(8)°;N(1)—Ni(1)—O(5):91.08(8)°;O(4)—Ni(1)—O(5):90.28(8)°.
从晶体结构(见图1)可以看出,配合物Ni[Pyzdc(COO)COOH]2·2H2O 是由 2个吡嗪-2,3-二羧酸为配体的单核配合物,Ni(Ⅱ)分别与2个Pyzdc配体上的羧酸氧和氮以及2个水分子中的氧形成八面体结构.该分子存在穿过Ni(Ⅱ)的中心对称.配体的羧酸与其Ni(Ⅱ)的距离(Ni(1)—O(4))为0.202(2)nm.C(6)—O(3)的距离为0.126(4)nm、C(6)—O(4)的距离为0.125(4)nm,这两个距离很相近,说明羧酸的3个原子O—C—O之间存在某种程度的共轭使C—O键长发生了平均化.从图2可以看出,每个配合物之间通过C—O…H的氢键作用,形成稳定的一维结构,其中 O(1)—H(5A)、O(2)—H(5A)的距离分别为0.206 nm、0.275 nm.与此同时,在图3中可以看到,通过O(1)与H(5B)之间C—O…H的氢键作用,形成了二维空间结构.其中O(1)—H(5B)之间的距离为0.211 nm.

图1 Ni[Pyzdc(COO)COOH]2·2H2O 的分子结构Fig.1 Molecular structure of Ni[Pyzdc(COO)COOH]2·2H2O
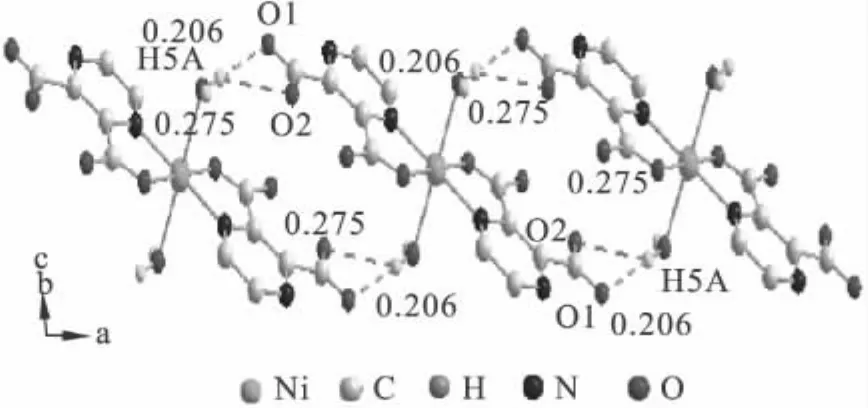
图2 Ni[Pyzdc(COO)COOH]2·2H2O的一维链结构Fig.2 One-dimensional chain structure of Ni[Pyzdc(COO)COOH]2·2H2O
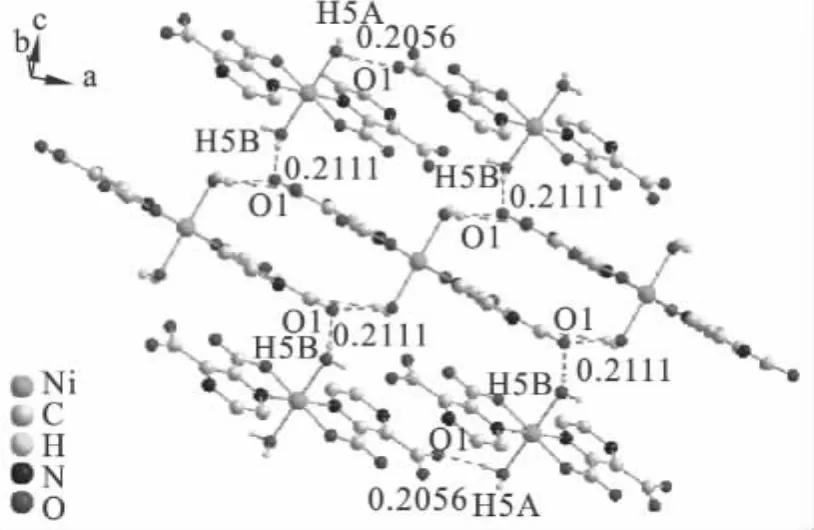
图3 Ni[Pyzdc(COO)COOH]2·2H2O的二维链结构Fig.3 Two-dimensional structure of Ni[Pyzdc(COO)COOH]2·2H2O
3 配合物与DNA作用机理讨论
3.1 配合物与CT-DNA作用的紫外光谱测定
DNA分子在波长为260 nm处具有典型的吸收峰,这是由核酸中有碱基共轭双键存在.在波长为260 nm处,DNA双螺旋分子的吸光度值比DNA分子中各碱基的吸光度值的和要小很多,这种现象被称为“减色效应”.这是由于DNA分子中各碱基平行、紧密的堆叠所引起的.
配合物与CT-DNA(CT-DNA是小牛胸腺DNA)相互作用的紫外光谱如图4所示.由图4可知,在波长为190~360 nm范围内有多个吸收峰.相同浓度 Ni[Pyzdc(COO)COOH]2·2H2O(2.0×10-5mol/L)掺入到不同浓度DNA后,对应285 nm左右的吸光度值逐渐减小,表现为比较明显的减色效应,DNA的最大吸收峰发生蓝移现象.当配合物与DNA碱基对以插入方式结合时,由于配体与碱基的π*空间和π电子轨道发生偶合现象,使能级发生变化,从而导致蓝移现象的产生[11].上述紫外光谱的变化显示配合物中较大的平面芳环配体Pyzdc与DNA以插入方式发生了非共价键作用.
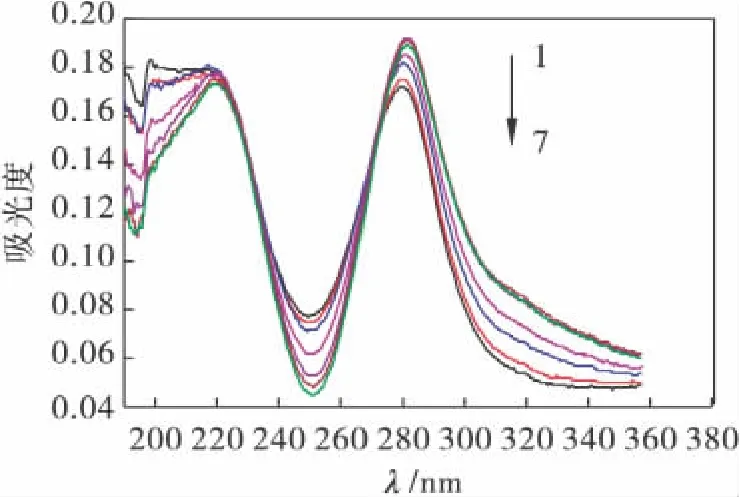
图4 Ni[Pyzdc(COO)COOH]2·2H2O 对CT-DNA的吸收光谱影响Fig.4 Absorption spectrum of the Ni[Pyzdc(COO)COOH]2·2H2O in the absence and presence of increasing amounts DNA
3.2 配合物与DNA-EtBr作用的荧光光谱测定
溴化乙锭(EtBr)是非常重要的平面分子荧光探针[12].EtBr分子平行地嵌插入DNA分子内部,由于EtBr本身具有一定的荧光,而DNA分子没有荧光,当EtBr插入DNA分子之后,增加了EtBr分子的平面刚性,淬灭现象减小,荧光明显增强.
图5为配合物与HeLa-DNA作用的荧光光谱图.由图5可知,随着配合物浓度的增加,DNA-Et-Br体系荧光强度逐渐减弱,并且浓度越大,荧光猝灭现象愈明显.由斯特恩-沃尔默(Stern-Volmer)方程[13]:I0/I=1+Ksqr,其中 r是配合物与DNA浓度的比值,I0和I分别表示不存在和存在淬灭体时的荧光强度,Ksq是斯特恩-沃尔默(Stern-Volmer)淬灭常数.由图6可计算出该混合物的Ksq=0.190 4.实验结果表明:当DNA分子加入到配合物中,发生了π-π堆砌作用,这是由于配合物[Pyzdc(COO)COOH]2·2H2O中较大的疏水平面芳环(Pyzdc)插入到了DNA碱基对中.
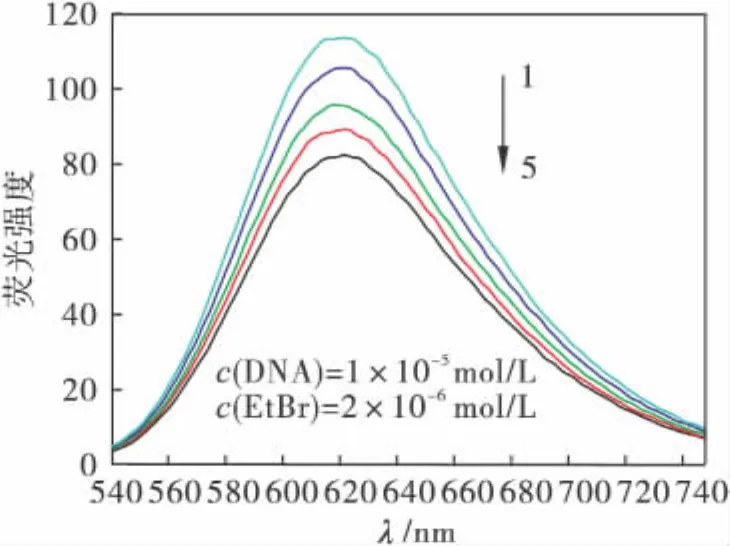
图5 Ni[Pyzdc(COO)COOH]2·2H2O 对DNA-EtBr体系荧光强度的影响Fig.5 Emission spectrum of EB bound to DNA in the presence of Ni[Pyzdc(COO)COOH]2·2H2O
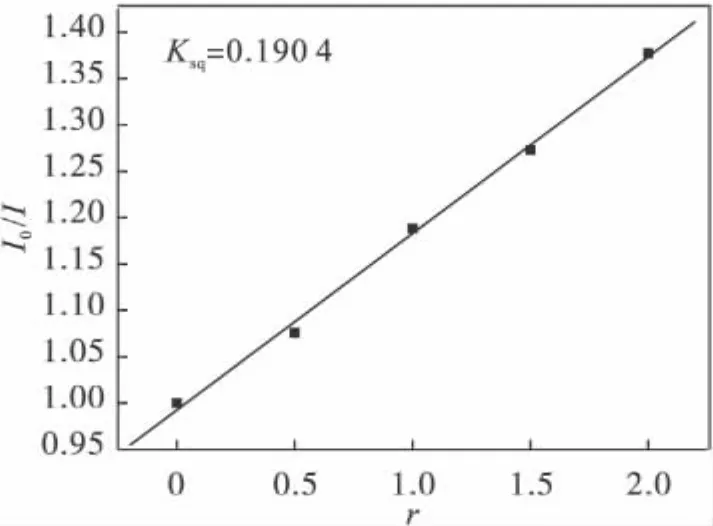
图6 Ni[Pyzdc(COO)COOH]2·2H2O的Stern-volmer图Fig.6 Stern-volmer quenching plots of the Ni[Pyzdc(COO)COOH]2·2H2O
3.3 配合物对pBR322-DNA的切割能力测定
在外电场作用下,带电颗粒如不处于等电状态,将向着与其所带电荷电性相反的电极移动.电泳时,样品在电槽中外电场的作用下发生移动,超螺旋带(FormⅠ)分子质量较小,在电场的作用下迁移速率较大;开环带(FormⅡ)分子质量最大,在电场的作用下迁移速率最小,而线性带(FormⅢ)处于两者之间.实验中,随着配合物浓度增加,FormⅠ解旋慢慢转化为FormⅡ,同时DNA会发生一定降解[14-17].
配合物与pBR322-DNA(0.01 g/L)作用相同时间后断裂结果如图7所示.随着配合物浓度的增加(Lane 0是纯的DNA,Lane 1~3为配合物与DNA在有氧条件下反应2 h的电泳图像,配合物浓度分别为 3.3、6.6、13.2 μmol/L),其对pBR322-DNA切割能力越来越大,即FormⅠ逐渐减少,解旋慢慢转化FormⅡ,即FormⅡ越来越多,但无线性带FormⅢ出现.因此可以看出该配合物对pBR322质粒DNA具有一定的切割能力,这与紫外吸收光谱、荧光光谱实验中得到的结论相吻合.
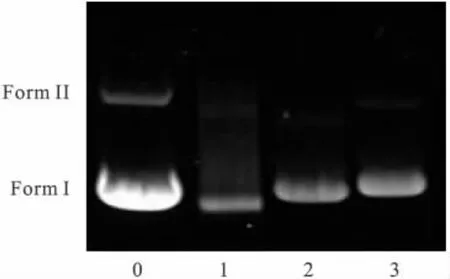
图7 Ni[Pyzdc(COO)COOH]2·2H2O与质粒pBR322-DNA电泳切割图Fig.7 Cleavage of pBR322-DNA in the presence of Ni[Pyzdc(COO)COOH]2·2H2O
4 结论
(1)Ni[Pyzdc(COO)COOH]2·2H2O 单晶为八面体构型,2个吡嗪-2,3-二羧酸配体以氮原子和氧原子与镍(Ⅱ)离子反式螯合配位,2个H2O分子则以氧原子与镍(Ⅱ)离子轴向配位,形成八面体配合物.
(2)配合物分子之间通过氢键弱相互作用形成新颖的超分子结构.紫外光谱和荧光光谱的测定均表明配合物与DNA之间发生了插入作用.在配合物对pBR322-DNA的切割能力测定中可以看出该配合物对pBR322质粒DNA具有一定的切割能力,这与紫外吸收光谱、荧光光谱实验中得到的结论相吻合.
[1] Zhang Y,Zhang Y M,Liu X G,et al.Synthesis and Crystal Structure of the Copper Complex{[Cu(CH3COO)2(bbtz)](H2O)2}n[J].Chinese Journal of Structure Chemistry,2005,24(10):1129-1132.
[2] Datta A,Karan N K,Mitra S,et al.Synthesis and Structural Characterization of a(N,N'-bis[2(S)-pyrrolidylmethyl]-propane-1,3-diamine)Nickel(Ⅱ)Complex[J].Journal of Chemistry Crystal,2003,33(7):579-583.
[3] Gillon B,Mathoniere C,Ruiz E,et al.Spin Densities in a Ferromagnetic Bimetallic Chain Compound:Polarized Neutron Diffraction and DFT Calculations[J].Journal of America Chemistry Society,2002,124(48):14433-14441.
[4] Noro S,Kitaura R,Kondo M,et al.Framework Engineering by Anions and Porous Functionalities of Cu(Ⅱ)/4,4'-bpy Coordination Polymers[J].Journal of America Chemistry Society,2002,124(11):2568-2572.
[5] Devereux M,McCann M,Shea D O,et al.Synthesis,Antimicrobial Activity and Chemotherapeutic Potential of Inorganic Derivatives of 2-(4'-thiazolyl)benzimidazole[thiabendazole]:X-ray Crystal Structures of[Cu(TBZH)2Cl]Cl·H2O·EtOH and TBZH2NO3(TBZH=thiabendazole)[J].Journal of Inorganic Biochemistry,2004,98(6):1023-1031.
[6] Chikira M,Tomizawa Y,Fukita D,et al.DNA-fiber EPR Study of the Orientation of Cu(Ⅱ)Complexes of 1,10-phenanthroline and Its Derivatives Bound to DNA:Mono(phenanthroline)-copper(Ⅱ)and Its Ternary Complexes with Amino Acids[J].Journal of Inorganic Biochemistry,2002,89(3/4):163-173.
[7] Santra B K,Reddy P A N,Neelakanta G,et al.Oxidative Cleavage of DNA by a Dipyridoquinoxaline Copper(Ⅱ)Complex in the Presence of Ascorbic Acid[J].Journal of Inorganic Biochemistry,2002,89(3/4):191-196.
[8] Song Y M,Wang Z H,Lu X Q,et al.Study on the Interactions between CuL2and Morin with DNA[J].Journal of Inorganic Biochemistry,2002,91(3):470-474.
[9] Lemoine P,Viossat B,Morgant G,et al.Synthesis,Crystal Structure,EPR Properties,and Anti-convulsant Activities of Binuclear and Mononuclear 1,10-phenanthroline and Salicylate Ternary Copper(Ⅱ)Complexes[J].Journal of Inorganic Biochemistry,2002,89(1/2):18-28.
[10] Chaviara A T,Cox P J,Repana K H,et al.Copper(Ⅱ)Schiff Base Coordination Compounds of Dien with Heterocyclic Aldehydes and 2-amino-5-methylthiazole:Synthesis,Characterization,Antiproliferative and Antibacterial Studies.Crystal Structure of CudienOOCl2[J].Journal of Inorganic Biochemistry,2004,98(8):1271-1283.
[11]徐宏,邓洪,胡红雨,等.多吡啶钌(Ⅱ)配合物的合成及其与RNA相互作用的光谱学研究[J].高等学校化学学报,2003,24(1):25-27.
[12] Chao H,Mei W J,Huang Q W.DNA Binding Studies ofRuthenium(Ⅱ)ComplexesContaining Asymmetric Tridentate Ligands[J].Journal of Inor-ganic Biochemistry,2002,92(3/4):165-170.
[13] Lakowicz J R,Weber G.Quenching of Fluorescence by Oxygen.A Probe for Structural Fluctuations in Macromolecules[J].Biochemistry,1973,12(21):4161-4170.
[14] Wang X L,Chao H,Li H,et al.DNA Interactions of Cobalt(Ⅲ)Mixed-polypyridyl Omplexes Containing Asymmetric Ligands[J].Journal of Inorganic Biochemistry,2004,98(6):1143-1150.
[15] Holder A A,Swavey S,Brewer K J.Design Aspects for the Development of Mixed-metal Supramolecular Complexes Capable of Visible Light Induced Photocleavage of DNA[J].Inorganic Chemistry,2004,43(1):303-308.
[16] Qian J,Gu W,Liu H,et al.The First Dinuclear Copper(Ⅱ)and Cleavage Reactions by Designed Analogues of Co(Ⅲ)-bleomycin:the Metalated Core is the Primary Determinant of Sequence Specificity[J].Inorganic Chemistry,1996,35(9):2637-2643.
[17] Barton J K,Raphael A L.Photoactivated Stereospecific Cleavage of Double-helical DNA by Cobalt(Ⅲ)Complexes[J].Journal of America Chemistry Society,1984,106(8):2466-2468.
