高铁酸钾去除水中磺胺嘧啶
2013-10-30高乃云祝淑敏杨一琼
马 艳,高乃云,祝淑敏,杨一琼
(同济大学 污染控制与资源化研究国家重点实验室,上海 200092)
近年来,新型污染物——药物和个人护理用品(PPCPs)在水处理领域受到越来越多的关注.PPCPs作为一类与人类生活密切相关的物质,已在环境中大量存在并对人类健康造成一定的威胁.例如,环境中的抗生素可以增加细菌耐药性、抑制细胞生长并对水生态系统造成负面影响[1-3].磺胺类抗生素是畜牧业和水产养殖业中的常用抗菌药物,随着我国畜牧业的快速发展,其作为兽药、渔药的使用量与日俱增并大量排入水体,已是水体中最频繁检出的一类抗生素[4].
高铁酸钾是一种绿色强氧化剂,在酸性条件下的氧化还原电位达到+2.20V,高于其他所有应用于水处理工艺的氧化剂[5].高铁酸钾可以快速杀灭水中微生物,有效去除内分泌干扰物、藻毒素、氯酚等难降解有机物,且不会生成三卤甲烷(THMs)、卤乙酸(HAAs)、溴酸盐等有害副产物,其还原产物Fe(OH)3无毒无害并具有絮凝和吸附功能[6-7].本文以磺胺嘧啶为目标污染物,采用高铁酸钾对其进行氧化去除,研究不同高铁酸钾投加量和不同pH值条件下高铁酸钾对磺胺嘧啶的去除效果,并初步探讨该反应的矿化程度和降解机理,从而为药物类污染水体处理提供一定理论依据和技术支持.
1 材料与方法
1.1 试验材料
高铁酸钾(w>90%)和磺胺嘧啶(w>99%)均购自美国Sigma- Aldrich公司.试验所用缓冲溶液由分析纯的氢氧化钾、磷酸氢二钾、磷酸二氢钾、硼酸钾配制而成.流动相甲酸和乙腈均为色谱级,甲酸溶液由超纯水配制.试验用水均采用去离子水.
1.2 试验方法
高铁酸钾与磺胺嘧啶的反应在150mL的玻璃锥形瓶中进行.反应液pH值由磷酸缓冲溶液调节,在磁力搅拌条件下向反应液中加入一定量的高铁酸钾,在预定的反应时间点取样并加入少量0.1mol·L-1的硫代硫酸钠终止反应.水样以6000r·min-1的转速离心10min后进行测定分析.所有试验在室温(25℃±2℃)下进行.
1.3 磺胺嘧啶分析方法
1.3.1 HPLC分析方法
磺胺嘧啶的浓度采用Waters e2695-2489高效液相色谱仪(紫外检测器)测定,色谱柱为 Waters Bridge C18色谱柱(150mm×4.6mm).流动相采用乙腈和质量分数为0.1%的甲酸溶液,两者的体积比为25∶75;流动相流速0.8mL·min-1,分析时间6min,柱温35℃,检测波长270nm.
1.3.2 LC- MS-MS分析方法
利用高效液相色谱(Waters e2695Separation Module)-质谱(Thermo Finnigan TSQ Quantum)对高铁酸钾氧化磺胺嘧啶所生成的产物进行分析,色谱柱为C18柱(Thermo Basic C18,150mm×2.1 mm),流动相为A(乙腈)与B(质量分数为0.1%的甲酸溶液),采用梯度洗脱模式,0~5min,流动相体积比维持在VA∶VB=1∶99,之后25min A相不断增加直至VA∶VB=80∶20,并维持5min,最后3min流动相体积比返回至VA∶VB=1∶99,检测时间共38min.流动相流速300μL·min-1,柱温35℃ ,进样量为10μL.质谱电离源为加热型电喷雾电离正源(HESI),电喷雾电压为3500V,鞘气压为0.28MPa,辅助气压为0.07MPa,离子传输毛细管温度为270℃.
1.3.3 TOC分析方法
磺胺嘧啶矿化程度采用TOC浓度值来表征,其浓度变化由TOC- VCPH仪(岛津)测定.
2 结果与讨论
2.1 高铁酸钾投加量对磺胺嘧啶去除效果的影响
在磺胺嘧啶初始浓度c0为0.02mmol·L-1,高铁酸钾投加量范围为0.0125~0.1000mmol·L-1,反应液pH值为7.0的条件下,磺胺嘧啶相对浓度(c/c0)随反应时间变化的曲线见图1.随着高铁酸钾投加量的增加,磺胺嘧啶的去除率和反应速率均明显提高.当高铁酸钾投加量为0.0125,0.0250,0.0500,0.1000mmol·L-1时,反应10min后,磺胺嘧啶的去除率分别为29.3%,44.5%,65.2%,86.2%.从结果还可以看出,高铁酸钾投加量增加,单位高铁酸钾去除磺胺嘧啶的能力下降,由0.47mmol·mmol-1下降为0.17mmol·mmol-1,这可能是因为高铁酸钾自身会分解,当其投加量增大时,高铁酸钾自分解加强[8],有效用于氧化磺胺嘧啶的比例降低.

图1 高铁酸钾投加量对磺胺嘧啶去除效果的影响Fig.1 Effect of different potassium ferrate dosages on sulfadiazine removal
2.2 pH值对磺胺嘧啶去除效果的影响
磺胺嘧啶初始浓度为0.02mmol·L-1,pH值范围为5.0~9.0,反应时间为10min,反应液中高铁酸钾投加量为0.0500mmol·L-1,不同pH值时高铁酸钾对磺胺嘧啶的去除效果如图2所示.由图2可知,反应液pH值对高铁酸钾氧化磺胺嘧啶影响很大,在中性和弱酸性条件下,磺胺嘧啶的反应速率及去除率明显高于碱性条件,反应液pH值为7.0时,磺胺嘧啶的去除率最高.这主要是由于pH值的变化会同时影响高铁酸钾的氧化能力和稳定性.高铁酸钾在酸性条件下的氧化电位(E0=2.20V)高于碱性条件(E0=0.72V)[5],反应液pH值升高,高铁酸钾氧化能力下降,反应速率降低,磺胺嘧啶的去除率下降.同时,高铁酸钾溶液稳定性随着pH值的降低而减小,当反应液pH值为5.0~7.0时,Fe(VI)主要以和 H2FeO4存在(见式(1)~(3)),高铁酸钾不稳定,易发生自分解,从而使其对磺胺嘧啶的去除率降低.此外,高铁酸钾氧化磺胺嘧啶在pH=7.0时达到最优效果可能还与磺胺嘧啶本身性质有关,磺胺嘧啶的电离平衡常数pKa值在6.5左右,有研究表明[8-9],离解状态的有机物更易被氧化去除,当pH>6.5时,磺胺嘧啶离解程度较高,更易被高铁酸钾氧化.
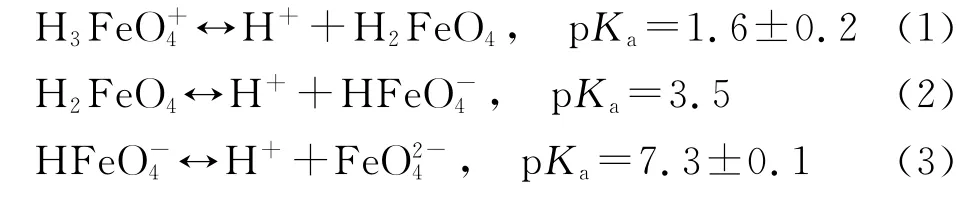

图2 pH值对磺胺嘧啶去除效果的影响Fig.2 Effect of different pH values on sulfadiazine removal
2.3 高铁酸钾对磺胺嘧啶的矿化效果
在反应液pH为7.0,磺胺嘧啶初始浓度为0.02mmol·L-1,高铁酸钾投加量为0.0500 mmol·L-1的条件下,10min内水样TOC相对浓度(TOC/TOC0)的变化如图3所示.随着反应时间的增加,磺胺嘧啶去除率显著上升,但TOC浓度下降不明显,说明高铁酸钾仅将磺胺嘧啶氧化成大分子有机物,反应不彻底,矿化程度较低.这可能是由于磺胺嘧啶结构稳定,不易被氧化降解.曾有研究表明,对于大部分的抗生素,由于分子结构稳定性高,因而很难得到完全矿化[10].在高铁酸钾氧化盐酸四环素的研究中也发现,当盐酸四环素的去除率高于70%时,TOC浓度下降率低于15%[11].
2.4 高铁酸钾氧化磺胺嘧啶产物分析
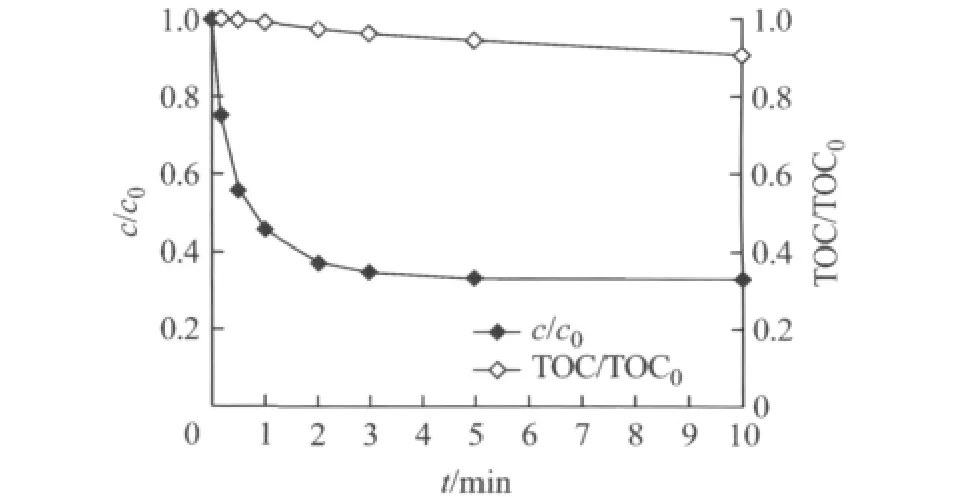
图3 pH=7.0时磺胺嘧啶去除率和TOC变化曲线Fig.3 Sulfadiazine removal and total organic carbon(TOC)reduction with reaction time at pH 7.0
利用LC-HESI-MS-MS对高铁酸钾氧化磺胺嘧啶的产物进行分析,并由此分析与推测可能的氧化反应途径.图4为LC -HESI-MS -MS产物分析质谱图,从图中可以看出,高铁酸钾氧化磺胺嘧啶的产物主要是核质比(m/z)为281的物质.高铁酸钾在氧化磺胺嘧啶过程中,Fe(VI)并不是一步反应生成Fe(III),而是通过单电子转移步骤顺次生成Fe(V),Fe(IV)和 Fe(III)[6,12],磺胺嘧啶的氨基(—NH2)上所带电荷以单电子逐步转移至Fe(VI),生成亚硝基和Fe(III).亚硝基不稳定,易被高铁酸钾氧化,最终生成硝基,主要反应过程见图5.该反应过程与Huang等[13]提出的高铁酸钾氧化苯胺存在的单电子转移反应机理相似.从产物分析结果可以看出,高铁酸钾氧化磺胺嘧啶过程中,主要攻击苯环上的氨基,并没有打开具有稳定结构的嘧啶基团和苯环,磺胺嘧啶仅转化为大分子产物,矿化程度不高,与氧化过程中反应液TOC浓度值下降幅度不大的结果一致.Sharma等[14]在研究高铁酸盐氧化磺胺类抗生素中也发现对于含有苯胺基的磺胺类抗生素,Fe(VI)主要氧化氨基,无法打开苯环,达不到彻底矿化的效果.
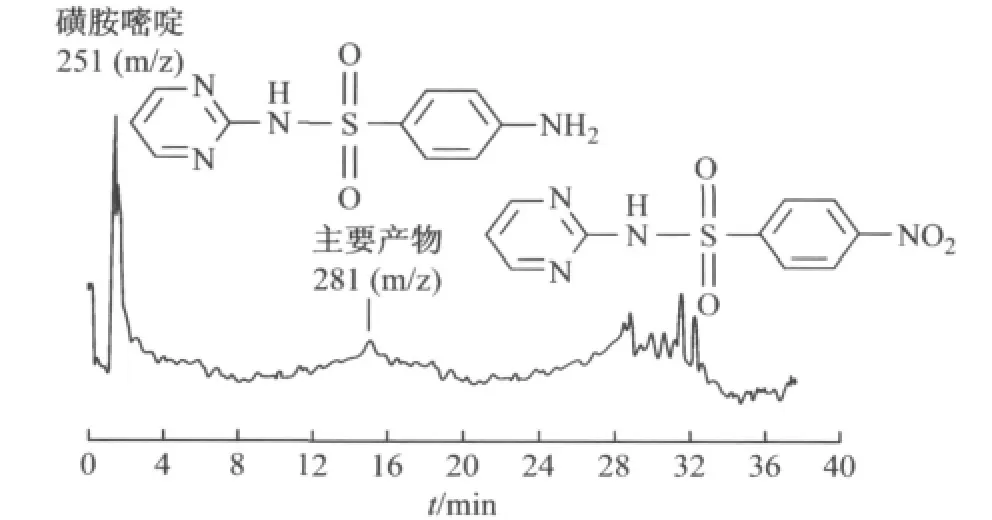
图4 高铁酸钾氧化磺胺嘧啶产物分析的LC-HESI-MSMS图Fig.4 LC-HESI-MS-MS chromatograph of intermediate products of sulfadiazine oxidized by potassium ferrate
3 结论

图5 高铁酸钾氧化磺胺嘧啶的反应途径推断Fig.5 The proposed sulfadiazine degradation pathway by ferrate oxidation
(1)高铁酸钾可以有效地去除水中的磺胺嘧啶.当反应液pH值为7.0,高铁酸钾投加量为0.1000mmol·L-1时,反应10min后0.02mmol·L-1的磺胺嘧啶去除率达到86.2%.
(2)高铁酸钾投加量和反应液pH值对磺胺嘧啶去除效果有显著的影响.磺胺嘧啶的反应速率和去除率随高铁酸钾投加量的增大而提高,但由于投加量增大造成高铁酸钾自分解加强,从而使单位高铁酸钾去除磺胺嘧啶的能力下降.反应液pH值的变化同时会对高铁酸钾的氧化性和稳定性以及磺胺嘧啶的离解程度造成影响.在中性和弱酸性条件下,磺胺嘧啶的去除效果明显高于碱性条件;pH值为7.0时,磺胺嘧啶去除率最高.
(3)反应液TOC浓度值测定以及产物分析结果表明,高铁酸钾对磺胺嘧啶矿化程度不高.反应过程中,通过单电子转移,高铁酸钾主要氧化磺胺嘧啶结构中的氨基,并未打开嘧啶基团和苯环,磺胺嘧啶仅转化为大分子产物,降解不完全.
[1]Pomati F,Castiglioni S,Zuccato E,et al.Effect of a complex mixture of therapeutic drugs at environmental levels on human embryonic cells[J].Environmental Science and Technology,2006,40(7):2442.
[2]Kummerer K.Antibiotics in the aquatic environment:a review—part I[J].Chemosphere,2009,75(4):417.
[3]Kummerer K.Antibiotics in the aquatic environment:a review—part II[J].Chemosphere,2009,75(4):435.
[4]Kolpin D W, Furlong E T, Meyer M T, et al.Pharmaceuticals,hormones,and other organic wastewater contaminants in US streams,1999-2000:a national reconnaissance[J].Environmental Science and Technology,2002,36(6):1202.
[5]Jiang J Q.Research progress in the use of ferrate(VI)for the environmental remediation [J]. Journal of Hazardous Materials,2007,146(3):617.
[6]Sharma V K.Potassium ferrate(VI):an environmentally friendly oxidant[J].Advances in Environmental Research,2002,6(2):143.
[7]马艳,高乃云,楚文海,等.高铁酸钾及其联用技术在水处理中的应用[J].水处理技术,2010,36(1):10.MA Yan,GAO Naiyun,CHU Wenhai,et al.Application of potassium ferrate and hyphenated techniques in water treatment[J].Technology of Water Treatment,2010,36(1):10.
[8]Li C,Li X Z,Graham N.A study of the preparation and reactivity of potassium ferrate[J].Chemosphere,2005,61(4):537.
[9]HoignéJ,Bader H.Rate constants of reactions of ozone with organic and inorganic compounds in water—II:dissociating organic compounds[J].Water Research,1983,17(2):185.
[10]Westerhoff P,Yoon Y,Snyder S,et al.Fate of endocrine disruptor,pharmaceutical,and personal care product chemicals during simulated drinking water treatment processes[J].Environmental Science and Technology,2005,39(17):6649.
[11]马艳,高乃云,李聪.高铁酸钾去除饮用水源中盐酸四环素试验研究[J].土木建筑与环境工程,2010,32(4):108.MA Yan,GAO Naiyun,LI Cong.Removal of tetracycline hydrochloride from drinking water source by potassium ferrate[J].Journal of Civil, Architectural & Environmental Engineering,2010,32(4):108.
[12]Sharma V K.Oxidation of inorganic compounds by ferrate(VI)and ferrate(V):one-electron and two-electron transfer steps[J].Environmental Science and Technology,2010,44(13):5148.
[13]Huang H,Sommerfeld D,Dunn B C,et al.Ferrate(VI)oxidation of aniline[J].Journal of the Chemical Society-Dalton Transactions,2001,8:1301.
[14]Sharma V K,Mishra S K,Nesnas N.Oxidation of sulfonamide antimicrobials by ferrate(VI)[][J].Environmental Science and Technology,2006,40(23):7222.
