鞘内注射氧气联合地塞米松对神经修复效果的临床观察
2013-10-30陈琳黄红云左焕琮
陈琳 黄红云 左焕琮
中枢神经脑和脊髓疾病的后遗症期,是临床常见的治疗难题,常规干预方法有限,严重影响患者的生存质量,给家庭和社会造成很大负担。近年来,基于人脑、脊髓的较大可塑性、内在潜力和可修复性,学者提出细胞移植、神经调控刺激、神经康复训练、鞘内氧气、用药等神经修复学策略,开创了新的探索方向[1-3]。鞘内纯氧联合地塞米松注射是一种临床实用的治疗方案,但目前开展的临床单位较少,研究的病种有限,北京康复医院神经外科近期采用此神经修复方法,治疗脑、脊髓难治性疾病3例,获得一定效果,报告如下。
一、临床资料
1.一般资料:2012年3~12月收治3例患者,其中男2例女1例,年龄44~62岁,中位年龄57.7岁。病种分布:颈髓损伤伴神经病理性疼痛、颅脑损伤后遗症、脑干血肿后遗症各1例。发病至首次治疗时间:2个月至1年10个月,平均11.3个月。
2.治疗方法:术前完成血常规、血型、尿常规、大便常规、凝血机制、肝肾功能、乙肝五项、丙肝抗体、梅毒抗体、艾滋病抗体实验室化验,心电图和胸片检查。术前4 h禁食水,建立静脉通路,多功能生理监护。常规腰椎穿刺,测压力,首先放出12~20 ml脑脊液,缓慢注射过滤氧气10~30 ml +地塞米松5~10 mg +生理盐水8 ml。术后平卧,多功能监护4~6 h。脑脊液常规及生化送检化验。
二、结果
3例患者全部获得功能改善和症状缓解。术后观察,血压一过性升高1例,未予处理,20~30 min后恢复平常水平。无其他不良事件发生。
病例1:患者陈某某,男性,67岁,因外伤后四肢活动不利伴双上肢疼痛2月余于2012年3月7日入院。诊断颈髓损伤伴神经病理性疼痛。患者于2011年12月10日2米高处坠落,臀部及右侧胸部着地,在北京某医院急诊,诊断为右侧肋骨多发性骨折,血气胸。立即手术,4根肋骨切开内固定,右侧胸腔闭式引流,20 d后拔除引流管。受伤后4 d,发现双上肢力量减弱,后双下肢力量减退,呈进行性加重。给予神经营养药物治疗,1个月后病情恶化趋于减慢,但不能站立,双上肢抬举受限。双上臂疼痛剧烈,给予口服洛芬待因缓释片、汉防己甲素片、曲马多缓释片等止痛药物,同时给予局部外用消痛贴、双氯芬酸二乙氨盐乳胶剂等,效果不明显。视觉模拟评分法(visual analogy score,VAS)疼痛评分8分。颈椎MRI(2012年3月2日)显示:颈椎4-5,5-6椎间盘向右后突出;颈椎2-3,3-4,6-7,颈7-胸1椎间盘膨出,脊髓信号稍异常(图1)。
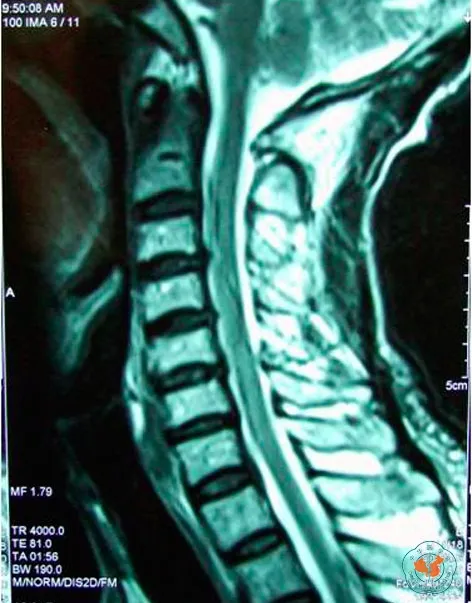
图1 患者颈椎MRI T2WI像
入院查体:神志清,精神欠佳。双上肢:远端肌力0~1级,近端肌力3级,肌张力减低。感觉功能正常。指鼻试验完成困难。轮替试验慢无力。手掌大小鱼际肌、股间肌中度萎缩。双下肢:远端肌力3级,近端肌力3级,肌张力稍高,感觉功能正常,跟膝胫试验完成困难。
治疗经过:2012年3月13日第1次腰椎穿刺,测压力为115 mmH2O,放出12 ml脑脊液,缓慢注射注射鼠神经生长因子(NGF)30 μg +单唾液酸四己糖神经节苷脂(GM1)20 mg +生理盐水8 ml,患者双手、上肢、下肢运动轻度改善,疼痛无缓解,脑脊液常规及生化检查结果正常。2012年4月18日第2次腰椎穿刺,测压力为120 mmH2O,放出15 ml脑脊液,同前注射NGF + GM1。患者病情无明显改善,肢体仍疼痛。脑脊液常规及生化结果正常。2012年6月18日第3次腰椎穿刺,测压力为100 mmH2O。共流出16 ml脑脊液。给予地塞米松5 mg +生理盐水8 ml缓慢鞘内注射,缓慢给予过滤纯氧10 ml。2012年6月21日VAS疼痛评分4分。2013年2月8日随访,双上臂无明显疼痛,未口服及外用止痛药物,VAS疼痛评分0~1分。双上肢由不能抬举过肩,改善可以高举过头部。由轮椅入院,改善为可以双手扶轮椅行走120米,可以自行如厕,生活自理能力较入院时明显改善。
病例2:岳某某,男,44岁。因车祸伤术后意识障碍伴肢体活动障碍4月余于2012年5月9日入院。患者于2012年1月17日发生车祸,伤后昏迷。在北京某急救中心CT显示左额颞部硬膜下血肿伴脑疝,脑挫裂伤,蛛网膜下腔出血,右额颞顶多发颅骨骨折,气颅。胸部CT:双肺挫伤,双侧胸腔积液。急诊行左额颞顶开颅硬脑膜下血肿清除术,去骨瓣减压术,左颞极切除内减压术,耳漏修补术。术中清除血肿60 ml。入ICU期间,复查头颅CT右侧硬膜外下血肿50 ml,中线移位。立即行右侧开颅血肿清除术,去骨瓣减压术,术中清除硬膜外血肿60 ml,硬膜下血肿30 ml。术后1个月气管切开封闭,可无意识睁眼,对疼痛可定位,无言语,左侧上下肢有无意识活动,可经口进食。集尿器收集尿液。患者曾接受高压氧治疗2次,因患者治疗后高热(后证实为肺炎所致),故未继续进行。
入院查体:瘦弱体型,被动体位,无言语,查体不合作。双侧颅骨大面积缺如,脑压正常。睁眼昏迷,无言语。左侧上下肢无意识活动,肌力4级。左侧肢体肌力0级。
入院诊断:颅脑损伤后遗症。
治疗经过:2012年6月5日第1次腰椎穿刺,测压力150 mmH2O,缓慢放出20 ml脑脊液,注入过滤氧气10 ml,脑脊液常规及生化正常。2012年6月18日第2次腰穿,压力为160 mmH2O,放出24 ml脑脊液,给予地塞米松5 mg +生理盐水10 ml缓慢鞘内注射,缓慢给予过滤氧气18 ml,脑脊液化验正常。2012年6月21日第3次腰穿,测压力为150 mmH2O(1 mmH2O=9.80665 Pa),放出 20 ml脑脊液,给予地塞米松10 mg +生理盐水10 ml缓慢鞘内注射,缓慢给予氧气12 ml,脑脊液化验结果正常。2012年6月26日第4次腰穿,测压力为150 mmH2O,放出18 ml脑脊液,地塞米松10 mg +生理盐水10 ml +氧气12 ml缓慢鞘内注射,脑脊液常规及生化结果正常。2012年7月1日第5次腰穿,测压力150 mmH2O,放出18 ml脑脊液,地塞米松10 mg +生理盐水10 ml +氧气20 ml鞘内注射,脑脊液检查正常。2012年7月4日自发言语增加,疼痛刺激后,可闻及“太热了”清晰言语。2012年7月5日第6次腰穿,压力150 mmH2O,放出18 ml脑脊液,给予地塞米松10 mg +生理盐水10 ml +过滤氧气20 ml缓慢鞘内注射,脑脊液常规及生化结果正常。2012年7月10日第7次腰穿,压力120 mmH2O,放出18 ml脑脊液,给予地塞米松10 mg +生理盐水10 ml +过滤氧气30 ml缓慢鞘内注射。2012年7月13日第7次腰穿,压力150 mmH2O,放出18 ml脑脊液,给予地塞米松10 mg +生理盐水10 ml +过滤氧气30 ml鞘内注射。2012年7月17日第8次腰穿,压力135 mmH2O,放出20 ml脑脊液,给予过滤氧气20 ml鞘内注射。2012年7月20日第9次腰穿,压力130 mmH2O,放出30 ml脑脊液,给予过滤氧气30 ml鞘内注射。2012年7月24日第10次腰穿,压力150 mmH2O,放出35 ml脑脊液,给予过滤氧气30 ml鞘内注射。2012年9月6日出院情况:言语及对外反应改善,有时刺激耳垂,发出“疼”的语言,有时刺激后,发出“太热了”的清晰声音,左侧肢体活动改善,左侧上肢肌力5级,下肢活动略改善。
病例3:张某某,女,62岁。因三叉神经痛术后脑出血伴构音不清、呛咳及四肢活动不利1年10个月于2012年7月20日入院。患者于2010年9月15日因三叉神经痛,在北京朝阳区某医院神经外科接受左枕后小切口三叉神经微血管减压术。9月17日上午,头痛、呕吐、颜面水肿、高热达39℃、耳鸣,对症治疗效果差。当日晚9点30分,患者昏迷,急查头颅CT显示脑干血肿约5 ml。急诊行开颅血肿清除。术后昏迷3 d,9月20日可睁眼,不能交流。后中枢神经系统感染、呼吸道感染、泌尿系感染,给予处理,行气管切开,胃造瘘。2010年10月10日病情平稳后,高压氧治疗共88次。2011年1月29日神志完全清醒。住院康复训练,针灸治疗。患者生活完全不能自理,胃造瘘饮食。右口角流涎明显,四肢活动不利,限于卧床和轮椅生活。入院诊断:脑干血肿清除术后。
入院查体:神清,精神差,构音中-重度障碍,吞咽障碍;注意力、记忆力、计算力减退;理解力尚可,可执行指令。右侧额纹浅,右眼睑闭合不全,右侧鼻唇沟浅,示齿口角左偏。舌不能完全伸出,有舌肌萎缩和束颤,咽反射迟钝,流涎明显。左上肢肌力0~1级,右上肢肌力3级;左双下肢肌力0级,右下肢3级。
治疗经过:2012年7月25日腰椎穿刺,测压力为150 mmH2O,放出24 ml脑脊液,给予地塞米松 5 mg +生理盐水6 ml缓慢鞘内注射,缓慢给予过滤纯氧18 ml,脑脊液常规及生化结果正常。术后1 d,言语稍改善,精神改善,反应改善。2012年12月5日第2次腰椎穿刺,测压力129 mmH2O,放出30 ml脑脊液,鞘内过滤氧气20 ml注射,地塞米松5 mg +生理盐水8 ml注射,脑脊液常规及生化结果正常。2012年12月6第2次腰椎穿刺,测压力129 mmH2O,放出30 ml脑脊液,鞘内过滤氧气20 ml注射,地塞米松5 mg +生理盐水8 ml注射,脑脊液常规及生化结果正常,操作过程血压每次上升5~10 mmHg,患者无明显头痛,头晕,2 d后,流涎消失,右侧下肢抬举幅度增加。2012年12月31日出院时,语言改善,流涎消失,反应好转,右侧下肢肌力3 +级。由床转移至轮椅较前容易。
三、讨论
1.疼痛的鞘内注氧及激素治疗
脊髓损伤后疼痛的发生率高达64﹪~82﹪[4],严重者显著影响患者的生活质量。作为中枢痛,脊髓损伤后神经病理性疼痛发病机制复杂,包括影响脊髓伤害性网络结构,异常开启投射到更高级脑中枢痛觉区域、神经组织异位、伤害性感受器致敏、结构恶性重塑、去抑制、神经炎症、神经-皮肤炎性信号传递、脊髓背侧角谷氨酸受体和胶质细胞激活、周围免疫细胞介导的痛觉异常、伤害感受小胶质细胞活化等。新近研究认为,在中枢神经系统中,免疫细胞和分子在神经病理性疼痛过程中发挥着越来越重要的作用,神经损伤后外周的肥大细胞、中性粒细胞、巨噬细胞和T淋巴细胞等免疫细胞所产生的级联炎性反应以及胶质细胞的激活是神经病理性疼痛形成和维持的关键因素。这些免疫细胞通过释放大量炎性介质最终导致疼痛的产生灶性神经炎症,是产生神经病理性疼痛的重要原因[5-6]。
糖皮质激素可通过抑制炎性因子或P物质(SP)产生,改善炎性痛的症状。鞘内注射地塞米松可能通过降低脊髓背角降钙素基因相关肽(CGRP)和P物质,减轻神经病理性痛大鼠的机械痛过敏。动物实验发现,地塞米松在病程早期和晚期均有较明显的治疗作用[7]。
氧对疼痛的作用是最近发现的一个有趣现象。高压氧(HBO)具有增强抗氧化酶活性,减轻或消退神经组织水肿,加速清除自由基的能力,提高血氧含量、产生较多的三磷酸腺苷,促进毛细血管再生,改善微循环的作用。能通过增高一氧化氮(NO)含量激活内源性阿片肽水平,产生镇痛作用。HBO也可通过调节机体免疫系统产生对疾病的治疗作用,如抑制炎症反应,降低白细胞聚集,降低循环中TNF-α,IL-1 以及 IL-6 的分泌[8]。
另有研究提示,鞘内给氧对神经损伤患者神经功能恢复的作用与高压氧相似。鞘内给氧能使脑组织缺氧得以改善,细胞能量代谢得以恢复,同时脑脊液中SOD水平显著升高,从而使机体对自由基的清除能力及细胞对抗脂质过氧化反应的能力得到提高,最终使脑细胞受过氧化损伤程度减轻而达到神经保护作用。由于气体动力作用,鞘内注入氧气可以冲开黏连,改善脑脊液循环,同时,氧气直接向脑脊髓细胞和血管内皮细胞弥散,刺激脑脊髓血管,使部分痉挛的血管功能逐渐恢复,改善微循环,纠正细胞的乏氧状态,这些对促进神经损伤患者神经功能障碍的改善作用,可能更优于高压氧。对推测某些中枢性疼痛的缓解,发挥积极治疗作用[9]。根据以上基础研究的结果,本研究采用鞘内注射纯氧和地塞米松的方法,观察对脊髓损伤后疼痛的效果,随访8个月结果满意,疼痛基本消失。操作中,应注意地塞米松应稀释和缓慢注射,以减少可能的局部刺激及对神经根和脊髓造成新的炎症损伤[10]。
2.颅脑损伤后遗症的鞘内治疗
氧疗,特别是高压氧,是临床治疗颅脑损伤常规手段。颅脑创伤后因机械性创伤破坏脑组织结构,导致脑组织缺血缺氧,进而产生一系列生化和代谢紊乱。早期高压氧能逆转脑缺氧造成的脑细胞轻度损害。改善细胞代谢紊乱,有效地降低缺氧所致的脑脊液内皮素含量升高,逆转缺氧所致的恶性循环。鞘内给氧对颅脑损伤患者神经功能恢复的作用与高压氧相似,且通过对比鞘内给氧与高压氧对颅脑损伤患者神经功能恢复的研究发现,鞘内给氧组神经功能改善更显著,这可能与氧气直接向脑细胞和血管内皮细胞弥散,刺激脑血管,使部分痉挛的脑血管功能逐渐恢复,改善了脑微循环,纠正了脑细胞的乏氧状态和脑细胞代谢异常有关[11]。另外,椎管注氧后可冲开粘连,也进一步改善脑脊液循环;注氧后增加脑干及网状结构激活系统供血量,刺激上行性网状系统的兴奋性,有利于改善醒觉状态,使昏迷患者意识抑制程度减轻[12]。应用大剂量地塞米松既能防治脑伤后继发性炎症病理损害,又可降低血管对γ-受体的敏感性,增强血管β-受体的敏感性,扩张血管,增强损伤局部和周围脑组织中的血流量[13]。鞘内给药则可以减少全身用药的副作用,并能提高局部有效剂量。报告中这例患者,共接受10次治疗,腰穿注射氧气的剂量10~30 ml,地塞米松的剂量为5~10 mg,操作后无不良反应,脑脊液化验结果正常,初步证实安全可行。
3.脑出血后遗症的鞘内疗法
腰穿脑脊液置换鞘内注氧是治疗急性期蛛网膜下腔混血临床常用的方法[14],应用鞘内注射纯氧治疗脑血管疾病及血管性痴呆,亦安全可行,文献报告有一定疗效[15-16]。本例为脑出血慢性期患者,氧气治疗后获得疗效,机制推测:(1)冲开局部粘连。术区出血伴有蛛网膜下腔出血、蛛网膜损伤,蛛网膜和软脑膜炎性变,形成粘连,影响脑脊液循环。(2)改善脑血循环,纠正脑细胞乏氧状态。椎管注氧后,通过血脑脊液屏障和脑脑脊液屏障,氧向血循环弥散,向脑细胞和血管内皮细胞弥散,同时也刺激脑血管,使部分近于麻痹的血管恢复功能,改善了脑循环[17],使得部分处于神经冬眠的可逆细胞恢复[18]。地塞米松作为一种长效激素,具有抗炎、稳定细胞和溶酶体膜等多项保护作用,可以对抗脑出血后的慢性局部炎症,且可以改善神经传导,促进神经修复[19]。
本研究初步显示,氧气配合地塞米松鞘内,方法简单易行,对脑损伤、出血后遗症和脊髓损伤继发的神经痛有一定疗效,值得临床深入研究。与细胞移植联合应用,具有前景。
1 Huang H,Chen L,Sanberg PR. Clinical achievements,obstacles,falsehoods,and future directions of cell-based neurorestoratology[J]. Cell Transplant, 2012, 21,(S1): 3-11.
2 陈琳,黄红云,左焕琮. 疼痛神经修复学:疼痛治疗新思路[J/CD]. 中华临床医师杂志: 电子版, 2011,5(19):5554-5556.
3 陈琳,黄红云,左焕琮. 中枢神经修复术研究现状[J/CD].中华临床医师杂志:电子版,2012,6(24):8198-8201.
4 陈琳,江昭,黄红云,等. 嗅鞘细胞移植治疗脊髓损伤后顽固性神经性疼痛17例报道[J]. 中国康复理论与实践,2010,16(2):146-148.
5 陈琳,黄红云,左焕琮. 细胞移植在疼痛和癫痫神经修复学中的研究概述[J/CD]. 中华细胞与干细胞杂志:电子版,2012,2(3):212-219.
6 Calvo M,Dawes JM,Bennett DL. The role of the immune system in the generation of neuropathic pain [J]. Lancet Neurol, 2012,11(7):629-642.
7 胡进宇,王英伟. 鞘内注射地塞米松对坐骨神经慢性压迫损伤大鼠脊髓背角降钙素基因相关肽和P物质表达的影响[J]. 上海医学,2010,33(6):528-530.
8 韩光,孟凌新,李璐,等. 高压氧对神经病理性痛大鼠的疼痛行为学影响[J]. 中国疼痛医学杂志, 2011,17(6):357-360.
9 高李贵,王卉芳,师蔚,等. 鞘内给氧与高压氧对颅脑损伤患者神经功能恢复的对比研究[J]. 西安交通大学学报( 医学版), 2004,25(5):502-503.
10 Kroin JS,Schaefer RB,Penn RD. Chronic intrathecal administration of dexamethasone sodium phosphate:pharmacokinetics and neurotoxicity in an animal model [J].Neurosurgery, 2000, 46(1):178-182.
11 邹庆贵,周息茂,缪国专,等. 重型脑外伤患者脑脊液内皮素含量变化及高压氧治疗作用[J]. 河北医学,1995,1(6):388-390
12 卫德来. 重型颅脑损伤恢复期椎管注氧的疗效分析[J].陕西医学杂志, 1995,24(3):173.
13 田宇,周建,袁继红.大剂量地塞米松冲击治疗重症颅脑损伤[J].白求恩医科大学学报,1996,(02):177-178.
14 陈博,谢延风,陈文寿,等. 脑脊液置换联合蛛网膜下腔氧气注入治疗蛛网膜下腔出血21例[J]. 陕西医学杂志.2006,35(4): 497-498.
15 龚梅辉. 脑血管病人椎管内给氧术的护理[J]. 护士进修杂志,1991,6(5):36.
16 闫海波,高凤琴,李德香. 鞘内注射纯氧治疗血管性痴呆的临床研究[J]. 山东医学高等专科学校学报. 2008,30(1): 45-48.
17 孙怀彬,程相文,何开毅,等. 椎管高压注氧治疗脑外伤后综合征67 例[J]. 中华神经外科杂志,994,10(2):118-119.
18 陈琳,黄红云,郗海涛,等. 神经修复学理论新思考[J].中国医疗前沿, 2009, 4(23): 10.
19 沈寻,靳文毅,盛森,等. 地塞米松鞘内注射在脑神经微血管减压术后的应用[J]. 中国全科医学,2011,14(3C):972-974.
