重组人5型腺病毒注射液介入途径给药治疗恶性肿瘤的安全性研究
2013-10-25李玉李文刚张素静
李玉 李文刚 张素静
(1.解放军第三零二医院肿瘤放射治疗中心 北京 100039;2.解放军第三零二医院感染性疾病诊疗和研究中心 北京 100039)
重组人5型腺病毒注射液系应用基因工程技术改构人5型腺病毒,删除与病毒复制相关的E1B-55KD基因片段后获得的一种选择性溶瘤病毒,为国家一类抗肿瘤生物制品。非外源基因的载体,是依靠病毒本身特异性地在肿瘤细胞内大量复制裂解杀死肿瘤细胞,从中释放出的子代病毒再进一步感染周围的肿瘤细胞,进而造成肿瘤组织的溶解坏死[1]。同时还具有协同放化疗、特异性免疫等抗肿瘤作用。传统给药途径是瘤内注射,局部药物浓度很高,但扩散受限,对于较大肿瘤需要多部位注射,增加操作次数,且分布不均。因此,我们采用介入手段将微导管插入肿瘤供血动脉,即超-超选择肿瘤供血动脉,随后将重组腺病毒注射液注入肿瘤,可使药物均匀、高浓度地分布于肿瘤组织发挥治疗效果,本文对介入途径给药的临床安全性进行观察,报道如下。
1 资料与方法
1.1 一般资料
自2011年6月至2011年9月间,我科通过介入给药的方式对82例患者给予重组人5型腺病毒注射液进行治疗,其中男57 例,女25 例,年龄31~82 岁,均诊断为恶性肿瘤,其中原发性肝癌56 例,肝转移癌12例,肺癌6例,胰腺癌3 例,前列腺癌2例,喉癌1例,食管癌2例。临床分期为I~Ⅳ期,符合《中国常见恶性肿瘤诊断规范》的标准。82 例患者随机分为3组:观察组35 例,对照组33 例,空白对照组14例。
1.2 治疗方法
治疗组在数字减影血管造影(digital subtraction angiography, DSA)引导下超-超选择肿瘤供血动脉,行碘油栓塞、化疗同时,给予重组人腺病毒注射液(上海三维生物技术有限公司生产,商品名安柯瑞,规格:每支5.0×1011vp/ 0.5 ml。给药方法:直径5 cm以下单发肿瘤1 ml,5 cm以上或多发肿瘤1.5 ml注入肿瘤血供动脉。对照组在介入栓塞化疗同时,采用瘤内注射方式给予重组腺病毒注射液,剂量同治疗组。空白对照组仅给予介入栓塞、化疗。治疗后给予止血、预防感染、水化等常规介入化疗后处理。
1.3 观察指标
治疗结束后监测血压、脉搏、呼吸、体温及足背动脉搏动情况,主要观察发热及其寒战等其他伴随症状,恶心、呕吐、食欲减退等消化道症状,心慌、胸闷、血压波动等循环系统症状以及头晕、过敏反应等发生比例、持续时间以及给予相关处理后恢复情况,1周后复查血常规、生化等指标。
1.4 统计学方法
不良反应持续时间为计量资料,以均数±标准差(x±s)表示,组间计量资料比较采用方差分析。百分比的比较采用x2检验。应用医学统计学软件SPSS 13.0分析,以P<0.05表示差异有统计学意义。
2 结果
观察组与对照组最常见的不良反应包括发热、畏寒、寒战、恶心、呕吐、食欲减退,这些不良反应及其持续时间见表1。
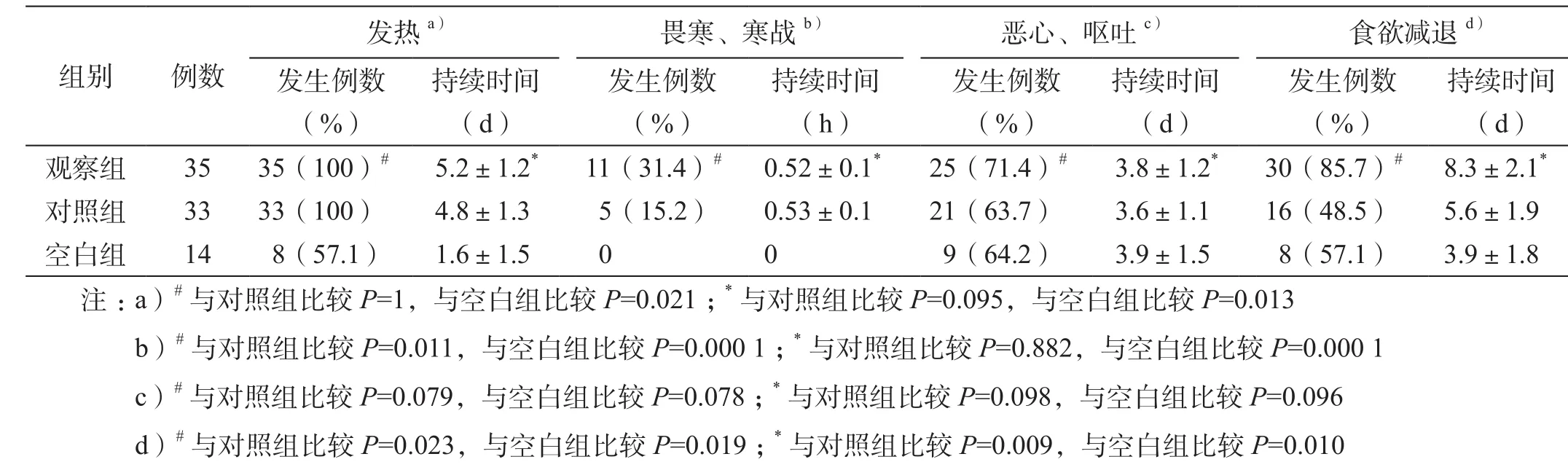
表1 重组人5型腺病毒注射液不同给药途径的不良反应发生比例及持续时间
重组腺病毒注射液通过介入给药后畏寒、寒战、食欲减退的发生率较对照组为高,持续时间略长,差异有统计学意义。其余较少见的不良反应包括头晕、血压升高、胸闷、心慌、过敏反应等,各种不良反应经对症处理后均消失。
3 讨论
重组人5型腺病毒删除了E1B-55KD基因片段,因而在体内一方面能够特异性地在恶性肿瘤细胞内大量复制、裂解肿瘤细胞、破坏肿瘤组织,而在正常细胞内不能复制,不造成破坏,因此,具有选择性溶瘤作用[1,2];另一方面通过改变恶性肿瘤细胞的一系列生物学活性,尤其是能抑制或调节某些与耐药有关的癌基因(如p53、Her-2neu、NF-κB等)的大量表达,以及改变受染细胞膜的物理特性,达到协同放化疗作用[3];再则,溶瘤病毒结合局部加热治疗,可通过特异性抗肿瘤免疫机制,诱导远端抗肿瘤效应[4];刘先军等[5]观察45例肺癌恶性胸腔积液患者,其中23例胸腔灌注重组人5型腺病毒注射液,22例局部灌注顺铂,结果重组人5型腺病毒注射液治疗组有效率明显高于顺铂组,且不良反应两组无明显差异。多项临床研究均表明,重组人5型腺病毒注射液联合化疗药物治疗多种实体瘤疗效显著优于单纯化疗,且不良反应较轻。除部分患者有发热、注射部位疼痛、乏力等反应外,未发现有严重不良反应发生[6,7]。
在肝癌治疗方面,传统治疗模式疗效有限,基因治疗代表肿瘤治疗发展的方向。有关临床试验数据表明,选择性复制型腺病毒联合化疗是一种有效的治疗方案[6-7]。溶瘤病毒传统给药途径是瘤内注射,而大多数肿瘤手术或放疗后复发都是多中心的,所以瘤体内直接注射病毒并不适宜。对于这些晚期肿瘤患者,如期望从溶瘤病毒治疗中获得良好的效果,应考虑局部或血管内注射病毒至肿瘤部位[8]。国内外有关学者经肝动脉注入溶瘤病毒的实验研究表明,溶瘤病毒可明显抑制大鼠移植性肝癌的生长,延长载瘤大鼠的生存期[8]。相关临床试验数据也表明,动脉灌注选择性复制腺病毒进行肿瘤治疗是可行的,并且与化疗联合使用产生的不良反应也是可以耐受的。由此可见,溶瘤病毒和介入治疗技术有机结合起来,有望在肝癌治疗中取得突破。因此,通过介入手段将药物直接注入肿瘤供血动脉可使药物在瘤体内均匀分布,最大限度发挥抑瘤、溶瘤作用。但目前尚无介入途径注射溶瘤病毒的临床研究,其安全性尚未可知。本研究选择多种肿瘤患者,以介入途径注射重组人5型腺病毒注射液与瘤内注射给药和单纯介入化疗对照,观察不良反应的发生率以及持续时间,旨在评价介入给药的安全性。结果发现,介入给药后寒战、畏寒、食欲减退的发生比例以及持续时间高于瘤内注射,发热发生率相似。可能与溶瘤病毒介入给药后部分进入血循环引起机体免疫反应有关,但这些不良反应经对症处理后均完全消失。
本研究仅是小样本研究,从初步结果来看,通过介入手段通过超-超选择肿瘤供血动脉将重组人5型腺病毒注射液注入肿瘤组织是安全的。但真正具指导性的、更有说服力的结果尚需进行长期多中心大样本、随机、对照临床研究。
[1] 徐立辉, 蔡槱佰, 王迪凡. 基因工程腺病毒治疗裸鼠骨肉瘤肺转移的实验研究[J].中华肿瘤防治杂志,2009,16(14): 1066-1068.
[2] Gonzalez R, Huang WY, Finnen R, et al. Adenovirus E1B 55-kilodalton protein is required for both regulation of mRNA export and efficient entry into the late phase of infection in normal human fibroblasts[J]. J Virol, 2006, 80(2): 964-974.
[3] 徐瑞华, 袁中玉, 管忠震, 等. 基因工程腺病毒(H101)逆转A549/DDP细胞对顺铂耐药性的实验研究[J]. 癌症,2005, 24(8): 975-979.
[4] 胡放, 胡晓桦, 余萍, 等. 溶瘤病毒H101结合局部加热治疗对转移肿瘤病灶的远端效应[J]. 癌症, 2006, 25(8): 919-924.
[5] 刘先军, 彭吉霞, 卢进昌, 等.重组人5型腺病毒胸腔灌注治疗肺癌恶性胸腔积液[J]. 临床肺科杂志,2010, 15(11):1539-1540.
[6] Wang Y, Hu F. Clinical trials with oncolytic adenovirus in China [J]. Current Cancer Drug Targets, 2007, 7(3): 659-670.
[7] 周彩存, 徐瑛, 倪健, 等. HIO1溶瘤腺病毒联合长春瑞滨/JlI页铂一线治疗晚期非小细胞肺癌[J]. 肿瘤, 2006,26(7): 613-617.
[8] 熊壮, 王建华. 溶瘤病毒在肝癌介入治疗中的应用[J]. 介入放射学杂志, 2007, 16(3): 206-208.
