室间隔缺损(VSD)介入治疗中封堵器的个体化应用
2013-10-16管丽华周达新葛均波潘文志陈海燕姚豪华孔德红
管丽华 周达新△ 葛均波 张 蕾 潘文志 陈海燕 姚豪华 孔德红
(1复旦大学附属中山医院心内科,2心超科 上海 200032)
室间隔缺损(ventricular septal defect,VSD)是最常见的先天性心脏畸形之一,可导致患者心脏负荷加重,肺动脉压力升高,诱发心力衰竭、心律失常,并易发生感染性心内膜炎。传统的治疗方法是外科开胸直视下行矫正治疗。自1988年Lock等[1]首次报道应用双面伞关闭VSD以来,已有多种装置应用于经导管的VSD介入治疗,特别是1998年Amplatzer发明了肌部VSD封堵器,以及不久后发明的膜周部偏心型VSD封堵器并成功应用于临床。但是美国以及欧洲的部分国家尚未批准该项技术应用于临床,而且国外使用的封堵器形态单一,均为偏心型封堵器。2002年6月开始VSD的介入治疗逐渐在中国各大心脏中心相继开展[2]。
随着病例的积累,对VSD的形态和解剖的认识不断深化,通过左心室造影发现,膜周部VSD形态各异,特别是伴有膜部瘤形成的VSD,有的有多个出口,有的形态呈囊袋状,有的呈手指状,有的呈蜂窝状。我们认为针对不同形态的VSD应有相应的封堵器,如靠近主动脉瓣的VSD应选择偏心VSD封堵器,针对膜部瘤VSD应选择小腰大边等封堵器。这些封堵器的应用,可提高临床手术的成功率、减少并发症的发生。我们根据单中心的经验报道137例VSD介入治疗中封堵器的个体化应用。
资料和方法
研究对象 以2010年1月至2012年2月在复旦大学附属中山医院心血管内科住院并接受介入治疗的VSD患者为研究对象。
入选标准:手术前在门诊或住院经过经胸超声心 动 图 (trans-t horax ultrasonic echocar diogra m,TTE)检查。筛选符合下列标准:(1)膜周部VSD:同时满足年龄≥3岁、体重>10 kg、VSD直径≥3 mm,<14 mm。(2)肌部VSD≥3 mm。(3)外科手术后残余分流。(4)心肌梗死后穿孔,急性心肌梗死后3周以上,或外伤后室间隔穿孔,无外科手术指征。(5)嵴内型VSD,缺损距离肺动脉瓣≥1 mm、直径<6 mm。(6)TTE测得VSD直径≥3 mm,左心室造影显示VSD<3 mm,≥1 mm,如果患者要求介入治疗,给予尝试治疗。
排除标准:(1)曾经发生感染性心内膜炎者。(2)心腔内有赘生物,或存在其他感染性疾病。(3)封堵器安置处有血栓存在,导管插入径路中有静脉血栓形成。(4)左心室造影VSD直径<1 mm。(5)TTE检查,VSD距离主动脉瓣<2 mm。(6)合并其他心脏畸形需外科手术治疗者,如双腔右心室等。(7)主动脉瓣脱垂有遮盖VSD现象者。(8)合并出血性疾病和血小板减少;合并明显的肝肾功能异常。(9)心功能不全(NYHA Ⅳ级),不能耐受操作。(10)重度肺动脉高压伴双向分流,肺动脉高压不能以缺损分流来解释。
疗效判定 VSD介入治疗成功的标志应符合以下条件:(1)无左向右分流。对于膜部瘤患者,在瘤体上可能有多个左向右分流,封堵后可能有少许残余分流,如残余分流细小,对血液动力学无影响,可视为成功。(2)封堵器对主动脉瓣功能无影响。主动脉瓣上造影无新增加的主动脉瓣反流,左心室流出道无新发生的压差。(3)对三尖瓣无影响,封堵后,三尖瓣反流不增加。(4)对右室流出道无影响。右心室流出道无压差 。(5)对传导系统无影响。无新出现的传递阻滞。
围手术期的处理 患者术前1~2天入院检查,排除不宜手术的疾患,签署知情同意书。术前1天开始服用阿司匹林,至术后6个月,儿童每天3~5 mg/kg,成人200 mg/d,阿司匹林过敏或不能耐受者改用氯吡格雷。
手术前30 min使用抗生素,次日继续应用抗生素。术后24 h复查超声心动图(UCG)、复查心电图(ECG),如出现异常可随时监测ECG、UCG,在手术后1、3、6、12个月随访ECG和UCG,必要时行X线检查。
符合条件的VSD患者共137例,其中男性71例,女性66例,年龄3~76岁,平均(31.52±16.13)岁。主要体征:胸骨左缘第2~5肋间收缩期杂音,肺动脉瓣区第二心音增强或亢进分裂,部分患者心前区可触及震颤。
根据UCG检查结果,VSD的类型为:膜周部(peri membraneous VSD,PMVSD)98例,单纯肌部(muscular VSD,MVSD)10例,嵴内型(intracristal VSD,ic VSD)12例,外科修补术后残余分流VSD(residual shunt,RSVSD)11例(7例位于膜部,2例位于肌部,2例为左心室右心房通道),心肌梗死后室间隔穿孔5例,外伤引起的室间隔肌部穿孔1例。其中PMVSD合并心肌致密化不全1例,PMVSD合并卵圆孔未闭(patent foramen ovale,PFO)4例,PMVSD合并动脉导管未闭(patent ductus arteriosus,PDA)2例,MVSD合并继发孔型房间隔缺损(atrial septal defect,ASD)1例,MVSD 合并PFO 1例。
操作方法[2-3]手术在导管室内、在 X线及TTE监护下进行操作,12岁以下患者选择静脉复合麻醉,成人局部浸润麻醉。
左、右心导管检查 左心室及主动脉瓣上造影术,显示VSD部位、形态和大小,观察有无主动脉窦脱垂及主动脉瓣反流。测量心腔内压力、心输出量,计算肺血管阻力和肺-体循环血流比(Qp/Qs)。
VSD介入封堵过程 根据VSD形态选用右冠状动脉造影导管或猪尾巴导管剪切塑形作为指引导管,将导丝从左心室经VSD送至肺动脉或上腔静脉。使用圈套器,套住导丝,由股静脉拉出体外,建立股静脉-右心房-右心室-VSD-左心室-主动脉-股动脉桥。沿导丝轨道将输送鞘管送至主动脉瓣上方,从动脉侧推送指引导管,将输送鞘管压至左心室,达左心室心尖。
将封堵器固定在输送钢丝上,收入短鞘中,排气后将封堵器送至输送鞘管末端,打开封堵器的左心室面的封堵盘,X线监视下回撤输送器,在右心室面打开右心室面的封堵盘,重复左心室和主动脉瓣上造影,检查有无残余分流、主动脉瓣是否有反流;UCG检查心室水平有无残余分流、主动脉瓣和三尖瓣功能状态、右心室流出道;心电图检查传导系统是否有传导阻滞。
封堵器[4]封堵器为上海形状记忆合金材料有限公司、深圳先建科技有限公司、北京华医圣杰科技有限公司生产,由具有形状记忆功能的镍钛合金丝,直径为0.13 mm和医用不锈钢(00Cr18,Mi 13 Mo3)编织而成,其内充填5层聚酯纤维膜。分为左、右心室封堵盘片,两盘片的连接部位为“腰部”;封堵器的形态有对称型封堵器、偏心型封堵器、大小边封堵器、肌部VSD封堵器(图1 A~D)。当封堵器和VSD不相匹配时,可通过输送钢丝收回到输送鞘管内。
封堵器的选择 根据VSD的部位、VSD形态、左向右分流束多少、VSD与主动脉瓣距离、三尖瓣的关系,进行个体化选择VSD封堵器类型和大小。嵴内型VSD紧靠主动脉瓣下,选择0偏心封堵器;膜周部VSD,无膨出瘤的,选择对称型封堵器;膜周部VSD有膨出瘤的,选择大小边封堵器,如左侧封堵器盘片为边3、边4、边5封堵器;心肌梗死后穿孔患者选择肌部室缺封堵器(表1)。

图1 各封堵器形态Fig 1 Different types of occluder

表1 不同部位VSD封堵器的选择Tab 1 Occluder selection accor ding to the different position of VSDs
数据收集及统计学处理 采用SPSS17.0软件对数据进行统计学分析。计量资料数据以表示,非正态分布资料采用平均数、标准差、最大值、最小值描述。两组间用两样本t检验,P<0.05为差异有统计学意义。
结 果
VSD患者临床资料 共有137例患者VSD入组,男性71例(51.5%),女性66例(48.5%),年龄最小3岁,最大76岁,VSD造影类型为(图2~7):PMVSD 98例,MVSD 10例,ic VSD12例,外科修补术后RSVSD 11例(9例位于膜部,2例位于肌部),心肌梗死后室间隔穿孔5例(3例为前壁心肌梗死,1例为前侧壁,1例下壁心肌梗死),外伤导致室间隔穿孔1例。其中MVSD合并继发孔型ASD 1例,MVSD合并PFO 1例,PMVSD合并PFO 4例,PMVSD合并PDA 2例,合并膜部瘤(membranous aneurysm,MA)76例(占PMVSD的77.5%,另5例为VSD修补术后残余分流伴膜部瘤形成);患者VSD直径2~14 mm,平均(4.86±2.36)mm;膜部瘤基底直径7~23 mm,平均(10.68±3.04)mm;所有VSD距主动脉瓣距离1~37 mm,平均(6.14±6.44)mm,距三尖瓣距离3~29 mm,平均(13.77±4.95)mm。

图2 管状VSDFig 2 Tubular VSD
左心室造影显示膜周部的VSD形态多样,有类似管状(图2)、漏斗状(图3)、囊袋蜂窝状(图4)、菜花状(图5)等。左向右分流孔有单孔、多孔(图6)。嵴内型VSD见图7。有2例患者分别使用2个室间隔缺损封堵器,经超声心动图、心动图监测对三尖瓣、主动脉瓣、传导系统均无影响。
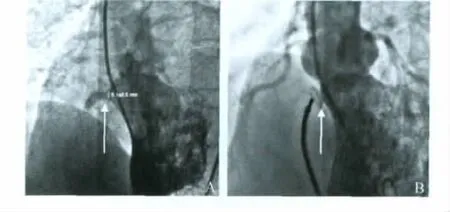
图3 漏斗状VSDFig 3 Funnel VSD
术中心导管测得肺动脉压力>25 mm Hg(1 mmHg=0.133 k Pa,下同)者有9例(6.57%),通过Ficks法计算得肺-体循环血流比(QP/QS)为2.0±0.4(表3)。
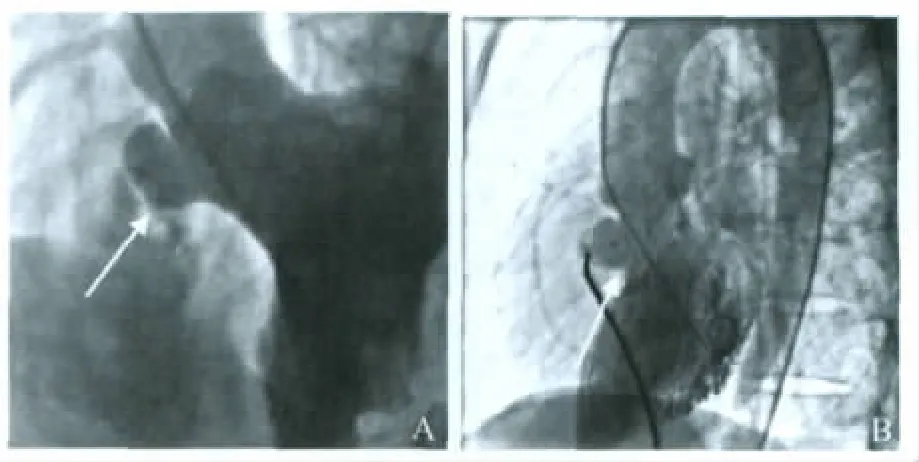
图4 囊袋状VSDFig 4 Cystic VSD

图5 菜花状VSDFig 5 Cystic VSD

图6 多孔状VSDFig 6 Polyporous VSD
VSD封堵疗效 137例患者均符合条件进行左心室造影,124例(90.51%)完成了手术治疗。有102例1次封堵成功,22例患者尝试2~3次后成功(表4),13例未尝试放置封堵器(2例室壁瘤)或尝试失败,失败原因有:伴有主动脉瓣脱垂(1例),无法建立动静脉导丝桥(3例),试封堵后有中到大量残余分流(4例),封堵器发生移位(2例,封堵器的右心室盘片在膜部瘤的瘤体内,误以为在右心室),分流量极小未予封堵1例。膜周部、嵴内型、外科手术后残余分流、心肌梗死后穿孔VSD的成功率分别见表5。
封堵器使用 共使用了126个封堵器,其中2例患者分别使用了2个封堵器。对称型封堵器26个(20.6%),边3 型 18 个 (14.3%),边4 型 44 个(34.9%),边 5 型 13 个 (10.3%),偏 心 型 14 个(11.1%),肌部封堵器使用了11个(8.7%)。

图7 嵴内型VSDFig 7 Intracristal VSD

表3 VSD心导管参数Tab 3 Parameters of cardiac catheterization

表4 VSD封堵技术参数Tab 4 Parameters of VSD occlusion

表5 各类型VSD介入治疗的成功率Tab 5 Success rate of different VSDs
随访 有8例(6.5%)患者在1个月后失访,其余116例随访6~12个月,平均(10.8±2.1)个月。表6是VSD患者封堵治疗前后左心结构和肺动脉收缩压变化数据。左心房前后径(LADap)、左心室舒张末内径(LVDd)、左心室收缩末内径(LVDs)均呈缩小趋势,LADap、LVDd在术后24 h缩小明显,差异有统计学意义(P=0.001及0.002);LVDs在术后24 h有缩小,但差异无统计学意义(P=0.097),而在术后1个月继续缩小,差异有统计学意义(P=0.007);左心室射血分数(LVEF)在术前、术后24 h无明显统计学差异(P=0.402),术后1个月与术前、术后24 h差异也未见统计学意义(P值分别为0.645、0.913)。
VSD患者肺动脉收缩压(PASP)术后24 h较术前有明显下降(P=0.001),但术后1个月未见进一步下降(P=0.820)。
封堵相关并发症 有1例封堵器移位,经导管取出后转外科治疗;造影见残余分流有11例,均为微量至少量,术后24 h有9例微量残余分流,术后1月有3例残余分流。现仍在继续随访1例主动脉瓣返流,术前为中度,术后未见增加。1例股动脉血肿,超声未见假性动脉瘤、动静脉瘘等,术后1月血肿吸收消失。无腱索损伤、右心室流出道狭窄、三尖瓣关闭不全及死亡病例。
表6 VSD患者介入治疗前后左心室结构、功能及肺动脉压力变化Tab 6 Variation of the structure,f unction of left ventricular and the pressure of pul monary artery pressure in VSD patients

表6 VSD患者介入治疗前后左心室结构、功能及肺动脉压力变化Tab 6 Variation of the structure,f unction of left ventricular and the pressure of pul monary artery pressure in VSD patients
?
心律失常 124例成功放置封堵器的病例,有29例(23.4%)术后出现心律失常,分别为Ⅰ度房室传导阻滞(AVB)3例(2.4%),2例术后即刻发生、术后24 h消失,1例术后2天发生、术后1个月随访时消失;2例(1.6%)术后出现左前分支传导阻滞,术后24 h恢复;出现完全性左束支阻滞(CLBBB)2例(1.6%),术中发生、术后2天恢复;IRBBB 6例(4.8%),均术后即刻发生,4例24 h消失,2例术后1个月随访时消失;术后出现CRBBB 7例(5.6%),6例术后24 h恢复、1例术后2天消失;术后即刻发生Ⅰ度 AVB合并 CRBBB 2例(1.6%),术后24 h消失;房性早搏1例,术后1天发生、术后1个月随访仍为房性早搏,术后3个月随访消失;交界性早搏1例,术后1天发生,术后1个月随访消失;阵发性加速性交界性心律5例(4.0%),4例在术后次日发现、1例在术后6个月行心电图发现,1例持续2天消失;2例术后1个月随访消失,1例目前仍未消失,无黑朦、晕厥,随访动态心电图无长间隙。UCG均未见明显心功能受损。其中1例阵发性加速性交界性心律患者在发现后使用甲泼尼龙(60 mg/d)静滴治疗3天后未见恢复,随访至术后复查消失,其余病例未曾使用激素、异丙肾上腺素等药物治疗。仅1例阵发性加速性交界性心律术后1年仍未恢复,总恢复率为96.6% (28/29)。
讨 论
经导管封堵治疗历程和疗效 VSD是最常见的先天性心脏病之一,以往外科手术是VSD的标准治疗方法。但是外科手术需体外循环,损伤大,住院时间长,残余分流发生率为5%,有一定的死亡率和致残率,约2%的患者需要再次手术,医源性房室传导阻滞约1%~8%[5-6]。获得性VSD外科手术治疗死亡和并发症风险更高。
1988年Lock等[1]应用Rashkind双面伞封堵器成功进行了VSD的封堵,为VSD介入治疗之先驱,当时病例主要是肌部VSD,肌部VSD仅占VSD的5%左右,故临床意义不大。之后有Rashkind、Car dioseal双面伞封堵器、Sideris纽扣式补片关闭肌部VSD和部分PMVSD,由于封堵器结构缺陷、移位、残余分流、瓣膜反流、房室传导阻滞(AVB)等并发症的发生率较高,未能推广。
1998年首例心肌梗死后室间隔穿孔经导管封堵治疗获得成功[7]。1998年Amplatzer发明了肌部VSD封堵器,2002年Amplatzer膜周部偏心型VSD封堵器成功应用于临床[8]。但是美国尚未批准此技术用于临床,多数欧洲部分国家也未用于临床。国内于2002年逐渐在临床开展VSD的介入治疗。总体来说,目前此项技术仍然属于探索阶段。
国内报道VSD封堵的技术成功率为93%~97%[2-4,9],本研究的成功率为90.5%,低于我们以往的报道(93.9%),可能与本研究选择的病例有关。
VSD致肺循环血流量增加、左心容量负荷过重,后期可致心腔扩大、肺血管阻力升高。本组病例VSD大小为2~14 mm,肺/体循环血流量比为1.6~2.9,属小~中型VSD,介入治疗后,左向右分流消失,肺循环血流量恢复正常,左心容量负荷得到矫正。本研究中,LADap、LVDd、LVDs均呈缩小趋势,LADap、LVDd在术后24 h缩小明显,(P=0.001及0.002)。LVDs在术后24 h有缩小,但差异无统计学意义(P=0.097),在术后1个月继续缩小,差异有统计学意义(P=0.007)。LVEF在术前、术后24 h差异无明显统计学意义(P=0.402),术后1个月与术前、术后24 h分别相比差异未见统计学意义(P 值分别为0.645、0.913)。VSD患者PASP术后24 h较术前有明显下降(P=0.001),术后1月未进一步下降(P=0.820),这种变化趋势与左心室内径变化趋势相一致,VSD封堵术有利于心脏结构和功能好转。这些均与以往研究相似[10-11]。
VSDO的个体化选择 VSD的分类方法较多,根据UCG检查结果,可将其分为膜周部VSD(MVSD)、肌部 VSD、圆锥部 VSD(包括嵴内型VSD)。MVSD占 VSD的75%,左心室造影可见心脏工作时VSD的生理形态,有别于外科手术修补VSD时的心脏停跳时的静态形态,这种心脏工作时VSD形态,对介入封堵治疗具有重大意义。我们将其分为:管状(Ⅰ)、漏斗状(Ⅱ)、囊袋蜂窝状(Ⅲ)、多出口状 (Ⅳ)、窗型(Ⅴ)5种类型。
VSD周围结构复杂,前有三尖瓣,上方有主动脉瓣,传导束行走在VSD附近,封堵器的选择不当,可致三尖瓣、主动脉瓣反流,严重还可致Ⅲ-AVB。出现这些并发症的原因可能与封堵器选择不当所致。一般认为封堵器腰部过大,可能对传导束产生压迫,以及封堵器的盘片过大可能对束支产生压迫或摩擦导致不同程度的传导阻滞。所以,在选择封堵器时,需要兼顾到上述情况,即个体化选择封堵器。
就封堵器植入术后传导阻滞的发生率情况,国外文献报道总传导阻滞的发生率为3%~31.6%,CRBBB发生率为0%~10.5%,IRBBB的发生率为0%~10.5%,左束支传导阻滞(LBBB)的发生率为0%~8.2%,完全性 AVB(Ⅲ-AVB)的发生率为0%~5.7%,永久起搏器植入率为0%~3.5%[12-13]。而肌部 VSD封堵术后心律异常的情况较少见,但也有高度AVB的报道[14]。国内文献汇总,总传导阻滞发生率为1.9%~30.4%,CAVB发生率为0.5%~7%,永久起搏器植入率为0%~0.4%,CRBBB、IRBBB、LBBB 的 发 生 率 分 别 为0.5%~8.4%、0%~13.1%、0.4%~3.9%[3,15-16]。至于VSD外科修补术后残余分流患者,经导管封堵治疗术后也有高度传导阻滞的报道。
我们根据不同类型的VSD应选择不同的封堵器的理解,封堵器的选择应既能够封堵VSD,又可避免医源性并发症,对三尖瓣、主动脉瓣、传导系统流、流出道不产生影响。管状VSD可选择对称型封堵器,如果分流管长度超过6 mm,应选择大小边的封堵器;漏斗状VSD选择对称的封堵器;囊袋蜂窝状VSD应选择大小边封堵器封堵,一般在囊袋里或蜂窝状的部位有多个出口,需要大小边封堵器。大小边封堵器有边3、边4、边5之分,如果囊袋出口小,或者有多个出口,边5的封堵器可能比较合适。多孔VSD,选择2个腰部小的封堵器,可能比使用一个大的封堵器更合适。
根据以上的认识,我们对98例MVSD进行了介入封堵治疗,成功率为94.9%,未发生三尖瓣、主动脉瓣功能不全,也无Ⅲ-AVB或其他传导阻滞如I-AVB,CRBBB,CLBBB等发生。96.6%患者恢复到封堵前的ECG。
综上所述,经导管封堵治疗VSD,封堵器的个体化选择非常重要,可以减少或避免传导阻滞,避免对三尖瓣、主动脉瓣功能的影响。
经导管封堵治疗VSD、封堵器应个体化选择,不同类型的VSD应选择不同的VSDO,选择合适的VSDO既能够封堵VSD,同时可少发生或避免医源性并发症。
[1] Lock JE,Block PC,Mckay RG,et al.Transcat heter cl osure of ventricular septal def ects[J].Circul ation,1988,78(2):361-368.
[2] 周达新,葛均波,陈灏珠.室间隔缺损封堵治疗的疗效和安全性[J].中华心血管病杂志,2003,31(5):330-333.
[3] Zhou DX,Pan WZ,Guan L H,et al.Transcat heter cl osure of perimembranous and intracristal ventricular septal defects wit h the SHSMA occl uder[J].Cathet Car diovasc Inter vent,2012,79(4):666-674.
[4] 周达新,高伟.结构性心脏病介入诊疗病例解析[M].上海:上海科学技术出版社,2012:226-228.
[5] Roos-Hesselink JW,Meijboom FJ,Spitaels SE,et al.Outcome of patients after surgical closure of ventricular septal defect at young age:longitudinal f ollow-up of 22-34 years[J].Eur Heart J,2004,25(12):1057-1062.
[6] Nygren A,Sunnegärdh J,Ber ggren H,et al.Preoperative evaluation and surger y in isolated ventricular septal defects:a 21 year perspective[J].Heart,2000,83(2):198-204.
[7] Crenshaw BS,Granger CB,Bir nbau m Y,et al.Risk factors,angiographic patterns,and outcomes in patients wit h ventricular septal defect complicating acute myocardial infarction[J].Circul ation,2000,101(1):27-32.
[8] Amin Z,Cao QL,Hijazi ZM,et al.Closure of muscular ventricular septal defects:Transcatheter and hybrid techniques[J].Cathet Car diovasc Inter vent,2008,72(1):102-111.
[9] 胡海波,蒋世良,徐仲英,等.室间隔缺损介入治疗五年临床随访分析[J].中华心血管病杂志,2009,37(7):619-621.
[10] 郑昭芬,蒲晓群,杨天仑,等.室间隔缺损封堵术对心脏重构近、中期的影响[J].中南大学学报:医学版,2007,32(2):320-322.
[11] 胡海波,蒋世良,程飞,等.超声心动图与左心室造影评价室间隔缺损封堵术后左心室功能变化的相关性研究[J].中国介入心脏病学杂志,2005,13(5):293-295.
[12] Car minati M,Butera GI,Chessa MA,et al.Transcat heter closure of congenital ventricular septal defects:results of the eur opean registry[J].Europ Heart J,2007,28(19):2361-2368.
[13] Thanopoulos BD,Tsaousis GS,Karanasios E,et al.Transcat heter closure of peri membranous ventricular septal defects wit h the Amplatzer asy mmetric ventricular septal defect occluder:preli minar y experience in children[J].Heart,2003,89(8):918-922.
[14] Thanopoulos BD,Rigby ML.Outcome of transcat heter closure of muscular ventricular septal defects with t he Amplatzer ventricular septal defect occl uder[J].Heart,2005,91(4):513-516.
[15] 程应樟,李正章,吴险峰,等.国产封堵器封堵嵴内型室间隔缺损:46例回顾封堵过程中选择类型、确定大小、避免损伤的经验[J].中国组织工程研究与临床康复,2010,14(4):740-743.
[16] 朱敏,周爱卿,高伟,等.室间隔缺损介入治疗前后心电图变化的探讨[J].临床儿科杂志,2010,28(5):469-471.
