腹腔镜胆囊切除术中(胆1囊04管次)全切除术的临床研究附例报告*
2013-09-27陈金锁李界明唐晓明田宇剑
陈金锁,李界明,吴 胜,唐晓明,田宇剑,李 伟
(1.安徽医科大学,安徽 合肥,231000;2.解放军第101医院)
腹腔镜胆囊切除术(laparoscopic cholecystectomy,LC)是治疗胆囊良性疾病的“金标准”。但有的患者术后仍出现上腹部疼痛等症状,甚至与胆囊切除前的症状类似,称为胆囊切除术后综合征(post cholecystectomy syndrome,PCS)[1]。导致 PCS 的原因很多,包括胆囊管残留过长及由此引发的炎症、再生结石等重要原因[2]。因此,LC术中行胆囊管次全切除是必要的。2012年2月1日至3月31日我们对腹腔镜下胆囊管次全切除的安全性、可行性及对PCS发生的影响进行了初步探讨。现报道如下。
1 资料与方法
1.1 临床资料 本组104例患者中男43例,女61例;平均(56.09±16.43)岁。胆囊结石伴慢性胆囊炎79例(萎缩性胆囊炎5例);胆囊结石伴急性胆囊炎21例(合并胆囊管结石4例);胆囊息肉4例。术前常规行磁共振胰胆管造影(magnetic resonance cholangiopancreatography,MRCP),排除胆总管结石;电子胃镜(90例)及上消化道造影(14例)检查,排除胃十二指肠溃疡等疾病。术前常规行MRCP,88例(84.6%)胆囊管显示清晰。根据黄志强教授对胆囊管的分型[3],其中胆囊管汇入呈角型(正常型)58例(65.9%),平行型19例(21.5%),螺旋型11例(13.0%)。
1.2 手术方法 全麻下由同一位术者(通讯作者)行3孔或4孔法LC。首先检查胆囊炎症情况及胆管间的解剖关系。靠近胆囊壶腹部分离出胆囊管。于胆囊三角区膜状分离纤维脂肪组织,分离出胆囊动脉并结扎,视胆囊炎症顺行、逆行或顺逆结合法剥离胆囊。最后逐渐分离胆囊管至胆囊管根部。放松对胆囊管的牵拉,于胆囊管根部用可吸收夹夹闭并切断,见图1~图6。炎症较重、渗出较多的患者,于小网膜孔放置腹腔引流管。
1.3 随访 门诊随访5~6个月,随访时常规行肝功及B超检查。
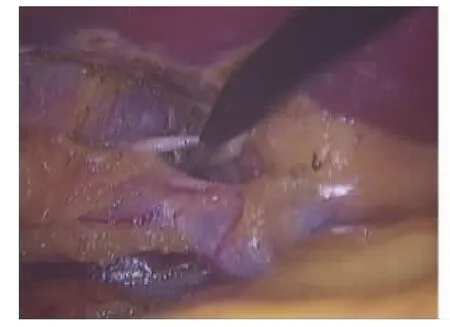
图1 分离、结扎并离断胆囊动脉
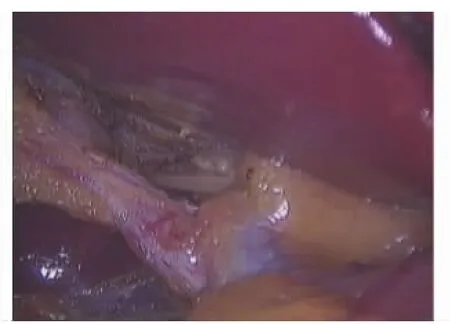
图2 分离胆囊管至根部
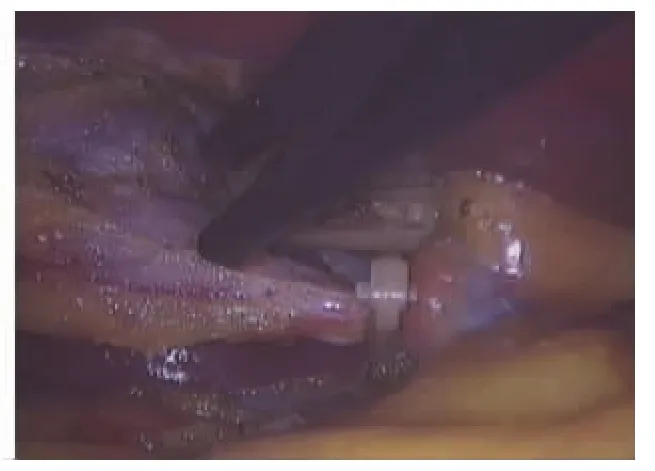
图3 于根部结扎胆囊管
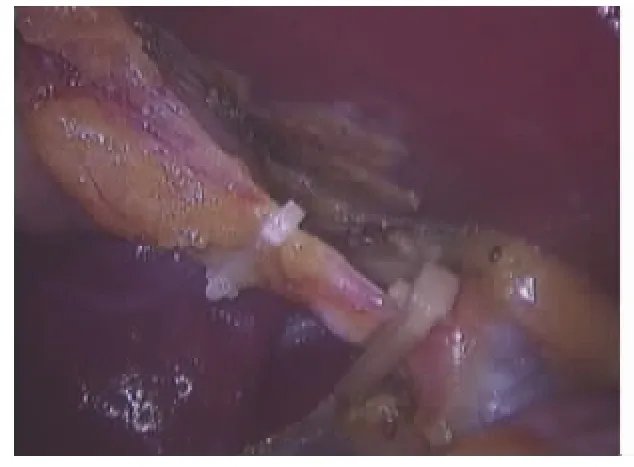
图4 分别结扎胆囊管根部及远端
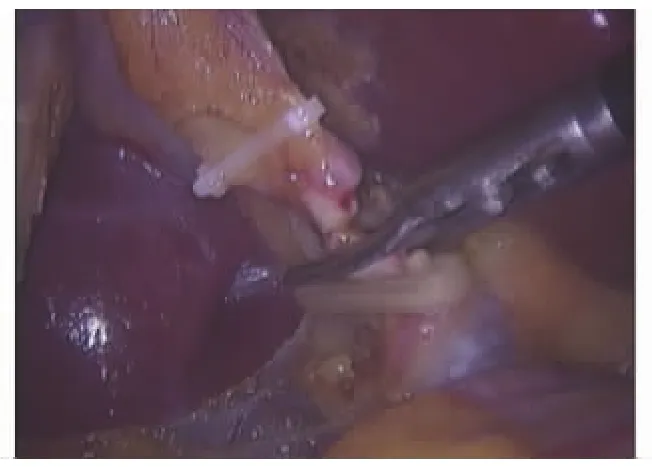
图5 胆囊管近完全切除

图6 切除胆囊管及胆囊动脉后
2 结果
2.1 手术结果 本组LC均获成功,无一例中转开腹。术中97例(93.3%)胆囊管成功分离至汇合部,7例(6.7%)未能分离至汇合部。合并胆囊管结石4例。手术时间平均(46.37±14.62)min,无出血、胆漏、胆管损伤、腹腔感染等并发症发生及围手术期死亡病例。术中13例(急性胆囊炎9例,慢性胆囊炎4例)放置腹腔引流管,术后2~3 d拔除。4例患者术后第1天出现低热,2~3 d后体温恢复正常,术后平均住院(3.29±0.67)d。
2.2 随访结果 门诊随访5~6个月并复查,均进行体检、肝功能及彩色超声检查,胆总管轻度扩张(直径8~10 mm)17例,未发现腹痛、黄疸、肝功能明显异常、胆管明显扩张及胆总管残留结石等。
3 讨论
1950年Primbam首次提出了PCS的概念,即胆囊切除术后患者出现或重新出现与术前相似症状。其发病因素是多方面的,包括胆系内原因及胆系外原因。胆系内原因包括胆总管结石、胆管损伤致胆漏或胆管良性狭窄、残留胆囊管、残留小胆囊、Oddi括约肌功能障碍、胆道蛔虫症等;胆系外原因术前多已存在,包括胃溃疡、十二指肠溃疡、食管裂孔疝、肠易激综合征、慢性胰腺炎及慢性肝炎等[1]。术前常规检查包括胸片、B超、MRCP、胃镜、钡餐及肝功生化检查等,基本可排除术前胆系内、外因素的干扰。尽管LC具有患者创伤小、出血少、康复快等优点,但文献报道[4],LC术后 PCS发生率仍较高,可达5% ~47%。
由于没有开腹胆囊切除术的空间感与直接手感,LC时,术者担心发生胆管损伤,本着“宁伤胆囊,不伤胆管”的原则,沿胆囊壶腹分离,并近胆囊颈部切断胆囊管,这样易残留较长的胆囊管。文献报道[2],胆囊管残留过长容易导致胆囊管残株炎,甚至形成结石,导致PCS;甚至有胆囊管残株癌变的报道[5-6]。因此,我们认为行 LC时应尽量切除胆囊管。我们的体会是,次全切除胆囊管的关键在于完全分离出胆囊管。术前根据MRCP结果充分了解患者肝外胆管的解剖变异情况,做到心中有数。术中操作时应尽量先分离并结扎胆囊动脉,解除胆囊动脉对胆囊管的牵拉作用,为下一步处理胆囊管提供足够的空间。对于不同类型的胆囊管应采取不同的分离方法。
黄志强院士[3]将胆囊管汇入胆总管分为三种类型:角型(正常型)、平行型、螺旋型。我们体会,对于角型汇入,胆囊管容易分离,不易残留较多;对于胆囊管与肝总管并排走行的平行型,又分为两种:一是胆囊管与肝总管间存在间隙,腹腔镜下可仔细分离并切除胆囊管;另一种是胆囊管与肝总管间为共同管壁、无间隙,不能强行分离,以免损伤胆管。约17%的患者胆囊管呈螺旋型汇入肝总管内侧壁。按胆囊管与肝总管的前后关系又分为旋前螺旋汇入型与旋后螺旋汇入型。完全分离这两种变异胆囊管较困难。术前MRCP提示胆囊管为此种变异类型时,术者分离胆囊管时应格外细心。如发现术中胆囊三角区粘连较重,分离困难时,应果断中转手术,不可为追求完全解剖胆囊管而强行分离,以免造成胆管损伤等严重后果。本组7例未成功次全切除胆囊管,均保留胆囊管0.3~0.5 cm。其中平行型胆囊管低位汇入肝总管2例,胆囊管螺旋型汇入肝总管1例。
本组中另有4例未能将胆囊管清晰分离至汇合部,原因有:(1)胆囊三角区炎症重、解剖不清(3例)。胆囊三角区炎症严重时,正常胆系结构与胆囊三角区内纤维脂肪组织间无间隙,无法分辨;此时不宜过分追求胆囊管的完全分离,以免损伤肝管。(2)胆囊动脉出血(1例)。胆囊急性炎症时多伴有新生毛细血管,分离时创面易渗血,此时一般出血量不大,只要及时吸尽渗血即可。无意中损伤胆囊动脉,出血较迅猛,狭小的术野很快模糊,此时切不可盲目钳夹动脉断端或试图电凝止血,否则极易导致医源性胆管狭窄,甚至胆漏。此时正确的做法是:用吸引器吸引,并用纱布条蘸尽积血后压迫出血端片刻,明确出血端后钳夹止血。对于断端回缩无法明确出血点而持续出血的患者应及时中转开腹。
胆囊切除时胆囊管残留长度一直无定论。为避免、减少医源性胆管损伤与狭窄,国内外学者普遍认为胆囊管残留0.3~0.5 cm为宜。理论上,残留胆囊管越短越好。我们体会,清晰显示胆囊管与肝总管汇合部后,可用可吸收夹于胆囊管根部夹闭胆囊管,达到胆囊管的次全切除。本组97例完成胆囊管次全切除,成功率93.3%。由于分离胆囊管至肝总管汇合部,可清晰看到胆囊管、肝总管、胆总管,不会因盲目钳夹而导致胆管损伤、横断或医源性狭窄。术后随访5~6个月,本组未发生明显上腹部疼痛等PCS症状,也未出现黄疸、胆管明显扩张等胆管受压及胆总管、胆囊管残留结石情况。但本组资料仅为回顾性单项研究,无同中心常规LC术后PCS发生率的对比;术后仅随访5~6个月,更长期的临床效果尚待观察与随访。
总之,LC术中仔细解剖胆囊三角区,分离胆囊管至清晰见到胆囊管与肝总管的汇合部,仔细操作,次全切除胆囊管是安全、可行的,可避免因胆囊管残留过长及胆囊管残留结石引发的PCS。
[1]Schofer JM.Biliary causes of postcholecystectomy syndrome[J].J Emerg Med,2010,39(4):406-410.
[2]龚昭,周程,闵凯.胆囊切除术后综合征[J].医学综述,2006,12(15):946-947.
[3]黄志强.黄志强胆道外科手术学[M].北京:人民军医出版社,1995:15.
[4]Bisgaard T,Rosenberg J,Kehlet H.From acute to chronic pain after laparoscopic cholecystectomy:a prospective follow-up analysis[J].Scand J Gastroenterol,2005,40(11):1358-1364.
[5]Gabata T,Matsui O,Sanada J,et al.Cystic duct remnant carcinoma with widespread invasion along the extrahepatic bile duct wall:dynamic CT findings[J].Abdom Imaging,2003,28(1):79-82.
[6]Noji T,Kondo S,Hirano S,et al.Carcinoma of the cystic duct remnant with direct colonic invasion[J].Int J Gastrointest Cancer,2003,34(2-3):117-120.
