某混合铜矿生物浸出铜的试验研究
2013-09-27胡杰华谢洪珍董博文朱莞烨范道焱
胡杰华,谢洪珍,董博文,朱莞烨,范道焱
(厦门紫金矿冶技术有限公司,福建 厦门 361101)
细菌浸出是借助某些细菌的催化作用,直接或间接地氧化含铜硫化物,使铜浸出[1]。低品位铜矿的细菌堆浸能耗低、工艺简单、投资少、环境污染小、适应性强,但浸出周期长、浸出速率慢[2-3]。细菌浸出过程既有细菌生长繁殖和生物化学反应,又有浸出剂和矿物的化学反应。由于细菌生长繁殖速度比矿物化学浸出反应慢得多,所以细菌的生长状况是整个细菌浸出过程的制约环节。金属矿物的浸出速度与浸出介质中细菌的浓度成正比,要取得矿物浸出的高速度,须保持细菌生长繁殖的高速度,而做到这一点的重要条件就是提供细菌生长所必需的足够营养物质[4-5]。一般矿石中都含有镁、钾、铁等无机盐,需要补充的主要有氮、磷元素,因此,研究细菌浸出过程中铁、氮、磷元素的浓度变化对细菌活性及金属浸出率的影响很有意义。
1 试验部分
1.1 试验矿样
试验矿样取自黑龙江某铜矿,其中主要有用矿物为氧化铜、斑铜矿、黄铜矿,脉石矿物为石英、斜长石、绢云母、绿泥石等。矿石呈土状及皮壳状。矿石多元素和铜物相分析结果见表1、2。铜平均品位为0.32%,属低品位混合铜矿。

表1 混合铜矿多元素分析结果 %
混合铜矿理论耗酸量为109.4kg/t。-200目占90%的矿石加入自来水,搅拌,用硫酸调矿浆pH至2.0,并稳定6h,实际耗酸量为46.83 kg/t。矿石实际酸耗量低于理论酸耗量。
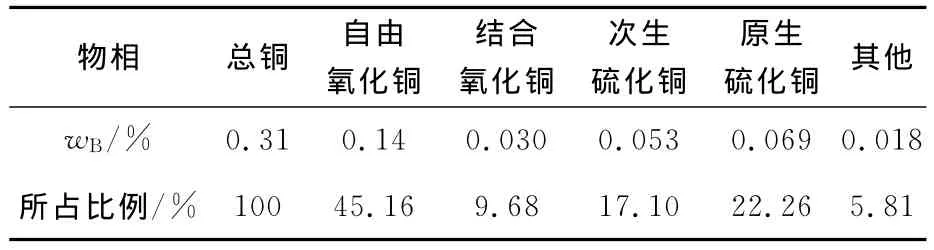
表2 混合铜矿物相分析结果 %
矿石中的铜以氧化铜为主,次生硫化铜占17.10%,原生硫化铜占22.26%,矿石氧化率为54.84%,为典型的混合矿。结合氧化铜因与脉石矿物之间有致密的包裹关系和共生关系,较难与浸出剂发生反应;而原生硫化铜因化学键结构牢固,不易被外力破坏,较难被氧化。
1.2 试验方法及药剂
1.2.1 试验方法
摇瓶浸出试验:摇瓶浸出试验在恒温振荡器中进行。取120mL 9K培养基于150mL锥形瓶中,按20%接种量加入菌液30mL,调初始pH至1.8,摇瓶振荡至电位升至530mV,加入一定量矿石,控制体系pH维持在1.8左右。室温下振荡一段时间后,过滤,渣、液分别送分析。
3L半连续浸出试验:在室温和一定pH条件下培养菌液,当电位达到600mV后分批次加入磨细后的矿样,使最终矿浆浓度为10%。氧化过程中,用碳酸钠或硫酸调整体系pH为2.0。当电位稳定且大于600mV一段时间后,取样。每次取样300mL,过滤,返回滤液270mL,补加矿样30g,并用自来水补足所差液量,继续搅拌。
柱浸试验:将破碎至一定粒度的矿石装入直径为200mm的柱中,先用6g/L硫酸溶液喷淋至浸出液pH稳定在2.0以下,再用菌液循环喷淋,每天测Eh、pH,并补水至指定刻度,维持总液量不变。每周取样并补充相同体积的9K培养基,检测浸出液pH、Eh及Cu、Fe、N、P、H2SO4浓度,判断细菌的生长状况、铜浸出速率、浸出周期和最终浸出率。模拟现场条件,采用6g/L硫酸溶液循环喷淋,当浸出液pH>1.5时,换新的6 g/L硫酸溶液,持续喷淋。
1.2.2 分析方法
水样中的金属离子用日本HITACHI公司生产的原子吸收分光光度计测定,氨氮用UV-5200比色测定,总磷用美国PE公司的电感耦合等离子体发射光谱仪测定;渣样中的铜用原子吸收分光光度计测定,铁用滴定法测定。
2 试验结果与讨论
2.1 摇瓶浸出试验
摇瓶浸出试验分有菌浸出和无菌浸出。细菌浸出试验条件:室温,矿石粒度-200目占90%,用9K培养基培养细菌,矿浆总浓度10%,体系pH控制在1.8。硫酸浸出条件为:室温,矿石粒度-200目占90%,液固体积质量比3∶1,酸液一次性加入,搅拌反应6d。试验结果见表3、4。
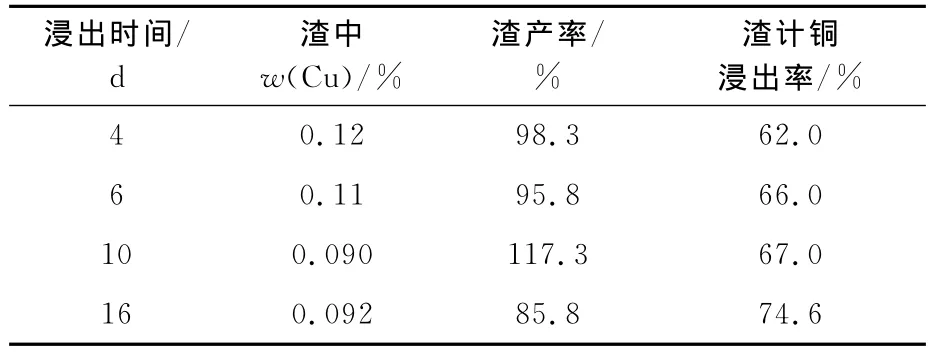
表3 混合矿细菌摇瓶浸出试验结果

表4 无菌硫酸直接摇瓶浸出试验结果
可以看出:与硫酸直接浸出相比,引入细菌后,体系pH需控制在1.8,即硫酸用量约为1g/L,铜浸出率即有不同程度提高;当矿浆浓度为10%、细菌浸出6d后,渣计铜浸出率达66.0%,随浸出时间延长,铜浸出率还有进一步提高。而无菌浸出6d,硫酸用量为30~80kg/t矿,渣计铜浸出率最高仅为57.5%。
2.2 3L模拟半连续浸出试验
试验条件:室温,矿石粒度-200目占90%,用9K培养基培养菌液,矿浆浓度为10%。从第35d开始,只取样、加矿石和自来水,不添加营养物质,考察Fe、N、P的浓度变化及对生物活性的影响。试验结果见表5。

表5 氧化时间对铜浸出的影响
连续取样12次,尾渣中w(Cu)/%基本稳定在0.075%以下,铜浸出率最高可达85.3%。氧化浸出10d,铜浸出率为71.6%,高于摇瓶浸出10d时的67.0%,说明搅拌浸出有利于提高细菌活性。
浸出35~84d,Fe、N、P质量浓度变化趋势如图1所示。
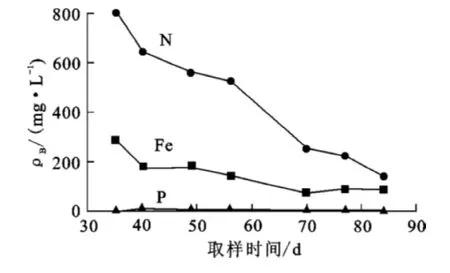
图1 pH为2.0条件下,Fe、N、P质量浓度与氧化时间的关系
随矿样质量增加,菌液中Fe、NH+4、∑P质量浓度逐步降低,且其浓度越高,越快被消耗,但铜浸出率维持在80%左右。说明菌液对Fe、N、P的要求并不高,Fe维持在100mg/L,∑P为5 mg/L,NH4为200mg/L,菌液仍保持较高活性。实际浸出过程可根据需要补充N和P。
2.3 柱浸试验
矿石破碎至-15mm占90%,均匀装入有机玻璃柱中,再用6g/L硫酸溶液反复渗洗中和碱性脉石矿物,同时浸出铜。当浸出液pH连续24 h恒定在2.0以下时,接种菌液。液计浸出率及Fe、N、P质量浓度变化分别如图2、3所示。

图2 液计铜浸出率变化曲线
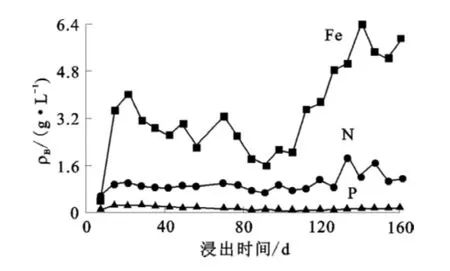
图3 柱浸过程中,Fe、N、P质量浓度变化曲线
第1周,硫酸直接滴淋,中和脉石矿物并浸出部分氧化铜。待浸出液pH稳定在2.0以下时,加菌液滴淋。第1周硫酸耗量为10.1kg/t矿,铜浸出率为29.97%。
细菌浸出前10周,每周铜浸出率均超过1%,Fe质量浓度维持在2~4g/L,NH+4-N质量浓度保持在0.8~1.0g/L之间,而∑P质量浓度不断降低。说明矿样在堆浸时有必要适当补充P元素。
细菌浸出11~16周,浸出液中Fe、P质量浓度持续走低,铁质量浓度为1.5~2.6g/L,∑P质量浓度继续降低至17mg/L。铜浸出速率放缓,平均每周浸出率约为0.40%。故从第16周开始,每天每公斤矿石补加9K培养基0.585mL,经过一段时间的适应,第19周铜浸出速率略微提高,但随培养基添加量的累积,从第21周起,铜浸出速率再次放缓。说明营养物质并非越多越好。
第23周,停止滴淋菌液,用pH=2.0的酸性水继续滴淋2d后卸柱,柱浸渣表面覆盖一层粉状绿色物质,推测是铜的复盐沉淀或铁矾沉淀。为了考察沉淀物的可溶解性,对氧化渣继续进行酸洗试验。将柱浸渣用pH=2.0的稀硫酸溶液在1mm筛子上洗矿筛分,分为+1mm部分和-1mm部分。分析结果见表6、7。

表6 柱浸渣分析结果
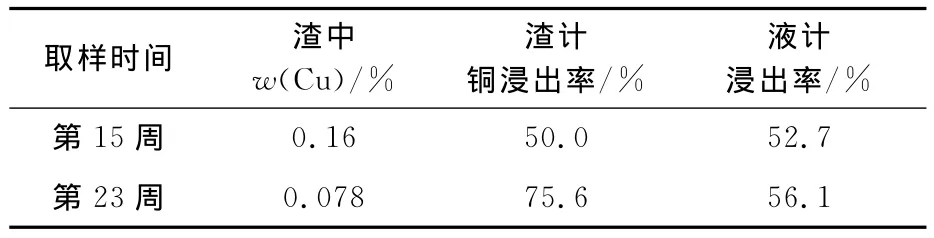
表7 柱浸表面浸出渣分析结果
第23周,表面取样渣计铜浸出率为75.6%,卸柱后整柱缩分取样渣计铜浸出率为59.1%。卸柱后重新用pH=2.0的硫酸溶液洗涤,渣计铜浸出率为71.0%,液计累计铜浸出率为56.1%。生物氧化柱表面取样与卸柱后尾渣缩分取样铜浸出率的差别可能是由于生物氧化柱pH控制在2.0左右,部分铜浸出后在柱下端析出造成的。细粒级矿石铜品位较高,进一步证明了部分铜以复盐形式沉淀析出。用pH=2.0的稀硫酸洗涤后,尾渣平均品位降至0.104%,铜总浸出率提高到71.0%,说明部分浸出的铜在柱下端析出且析出物较易溶于稀酸中。
3 结论
某低品位混合铜矿可以用细菌浸出方式有效回收铜。体系中,Fe质量浓度维持在2~4g/L,NH+4-N质量浓度保持在0.8~1.0g/L之间,∑P质量浓度保持在5~200mg/L之间比较适宜,细菌活性良好。
矿石粒度15mm,柱浸23周,细菌浸出渣计铜浸出率达到71.0%。
生物氧化后,柱表面取样与卸柱后尾渣缩分取样的铜浸出率有差别,可能是由于生物氧化后,浸出的部分铜在柱下端析出造成的。用pH=2.0稀硫酸洗涤后,铜浸出率提高,说明析出物较易溶于稀酸。
[1]董铁广,华一新.黄铜矿湿法冶金研究进展[J].有色矿冶,2009,25(3):28-31.
[2]袁明华,李德,普仓凤.低品位硫化铜矿的细菌冶金[M].北京:冶金工业出版社,2008:71-75.
[3]张冬艳,张通.硫化铜矿的细菌浸出试验研究[J].湿法冶金,1996(2):23-26.
[4]赖绍师,覃文庆,杨聪仁,等.低品位硫化铜矿的细菌浸出[J].中国有色金属学报,2011,21(6):1473-1479
[5]《浸矿技术》编委会.浸矿技术[M].北京:原子能出版社,1994:431-441.
