县区级医院应用PS治疗新生儿呼吸窘迫综合征的临床研究
2013-09-25李玉莲高德玉刘再亮贺志龙刘建华
李玉莲,高德玉,刘再亮,贺志龙,王 芳,刘建华
(甘肃省武威市凉州医院小儿重症医学科,武威 733000)
新生儿呼吸窘迫综合征(neonatal respiratory distress,NRDS)的病因很多,其中最重要的是由于缺乏肺表面活性物质(pulmonary surfactant,PS)引起,主要发生在早产儿。临床以进行性呼吸困难为主要表现,以出现嗜伊红透明膜和肺不张为病理特征,又称肺透明膜病(hyaline membrane disease,HMD)。NRDS是早产儿常见的危重并发症,也是早产儿死亡的主要原因之一[1]。自上世纪80年代国外由于应用肺表面活性物质使NRDS患儿病死率下降50%,气胸、支气管肺发育不良等严重并发症的发病率也明显降低[2]。上世纪90年代,国内也开始应用该技术。我院地处甘肃省西部,经济不发达,医疗卫生条件相对较差,自2010年9月至2012年3月应用PS治疗23例NRDS,取得了满意的治疗效果,现报道如下。
1 资料与方法
1.1 一般资料 选择2010年9月至2012年3月在我院新生儿重症监护病房收住的新生儿呼吸窘迫综合征患儿为研究对象。应用PS治疗者23例为观察组,选择同期非使用PS治疗者23例为对照组。观察组男16,女7 例,胎龄(30.87 ±2.91)周,体质量(1.76 ±0.78)kg,Apgar评分 1 min、5 min 分别为7.42 ±0.89、6.65 ±1.75;对照组男16,女7 例,胎龄(30.76 ±3.01)周,体质量(1.68 ±0.96)kg,Apgar评分1 min、5 min 分别为7.45 ±1.43、7.72 ±1.32。两组患儿在胎龄、出生体质量、性别及Apgar评分方面比较,差异均无统计学意义(P>0.05),具有可比性。
1.2 NRDS诊断标准与剔除标准 符合《实用新生儿学》的诊断依据[3]:①出生0~24 h的新生儿;②出生0~12 h后出现呼吸困难、呼吸急促、青紫、呼气性呻吟,并进行性加重;③胸部X线检查符合RDS诊断标准;④均需机械通气,吸入氧浓度(FiO2)>0.5或平均气道压(MAP)>8cmH2O。剔除标准:①青紫性先天性心脏病;②先天性膈疝;③食道气道瘘;④先天性气道、肺发育畸形或缺陷;⑤遗传代谢病。
1.3 治疗方法 两组患儿均接受呼吸机及常规治疗。呼吸机采用压力控制/间歇指令控制模式。观察组给予PS物质(固尔苏,意大利凯西制药公司生产,避光保存在2~8℃)。使用前将药缓慢升温至37℃,轻轻上下转动使药液均匀,然后用5 ml注射器完全抽取药液。应用前充分吸痰、清理气道、禁食。用最小号胃管量取长度(患儿所用气管插管的长度+1~2 cm),将此胃管与装有固尔苏的注射器连接好,将此胃管缓缓送入气管插管末端,外留1~2 cm,缓慢注药,速度不要太快(注药时间5~10 s),以免药液呛出或堵塞气道,每次注入总量的1/3,然后连注射器一起拔出胃管,加压给氧2~3 min(频率40~60次/min)。按平卧位、右侧卧位、左侧卧位顺序分3次注入。药物总剂量100~200 mg/kg。给药后4~6 h禁止吸痰。对照组除未应用PS物质其他常规治疗同治疗组。
1.4 观察指标 观察两组患儿治疗前及治疗后6 h的血气分析、机械通气时间、氧疗时间、监护室住院时间及并发症,并在24 h后观察胸部X线表现。
1.5 统计学方法 采用SPSS 11.0统计软件包,计量资料以±s表示,两组间均数比较采用完全随机设计的t检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组患儿治疗前后血气分析比较(表1) 两组患儿治疗前PaO2、pH、PCO2比较,差异均无统计学意义(P>0.05)。观察组治疗后PaO2、pH比对照组升高,PCO2比对照组降低,差异有统计学意义(P<0.05)。

表1 观察组与对照组治疗前后血气分析比较
2.2 两组患儿胸部X线表现 观察组应用PS后12 h,床旁胸部X线片可见肺充气情况好转,24 h后肺透亮度明显增加,肺膨胀良好,72 h胸部X线完全恢复正常21例(91.7%);对照组72 h胸部X线仅有13例(56.5%)完全恢复正常。
2.3 两组患儿疗效比较(表2) 观察组患儿的机械通气时间、氧疗时间、住院时间及病死率均低于对照组,差异有统计学意义(P均<0.05)。
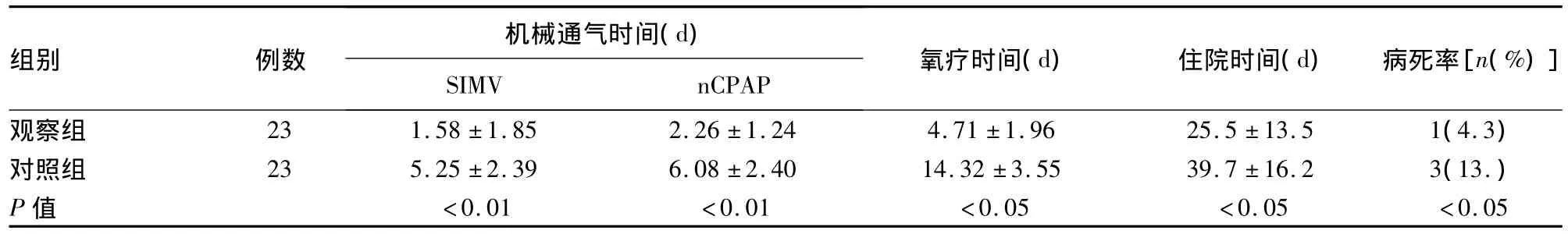
表2 观察组与对照组患儿临床疗效比较
2.4 两组患儿并发症比较 观察组患儿并发肺炎3例,无肺气漏、肺出血、肺不张及视网膜病等并发症的发生。对照组患儿发生肺气漏、肺不张、肺炎各3例,肺出血1例。
3 讨论
胎儿在胎龄22~24周时肺Ⅱ型细胞已能产生PS,但量不多,且极少转移至肺泡表面。随着胎龄的增长,PS的合成逐渐增加,因此胎龄愈小肺中PS的量越少,NRDS的发生率也就越高。胎龄24~30周时肾上腺皮质激素对促进肺成熟的作用最大,此时是产前预防的最佳阶段,胎龄35周以后是PS迅速进入肺泡表面的阶段。早产儿出生后肺仍迅速发育,生后72~96 h产生的PS一般能够维持正常呼吸,因此只要在PS缺乏阶段加以补充,使早产儿渡过难关,可提高存活率[3]。另外低氧、酸中毒(如围生期窒息)、高胰岛素血症(糖尿病母亲所生的新生儿)、剖宫产儿也影响肺的发育,PS的分泌也偏低,成为诱发 NRDS的原因[4]。这部分新生儿发生NRDS时也需要补充PS物质。RDS为早产儿死亡的主要原因,对所有可能发生RDS的患儿尽早使用肺表面活性物质在发达国家已经成为常规治疗[5]。我区由于经济发展的限制,医疗技术相对落后,部分高危早产儿未能接受或未能及时接受肺表面活性物质治疗而导致RDS发生,病死率增高本文结果表明,观察组使用PS 6 h后 PaO2、pH比对照组升高,PCO2比对照组降低,用药后24~72 h胸部X线也较对照组明显改善,从而缩短呼吸机使用时间、氧疗时间和住院时间,此与周晓光等[6]报道一致;观察组死亡率也较对照组明显降低。故应用PS替代疗法是针对NRDS病因的特效治疗,可显著提高早产儿存活率,缩短呼吸机使用时间、氧疗时间和住院时间,从而节省住院费用,因此总住院费用并不高于不用PS物质者,值得在县区级医院应用。
[1]杨树杰,易海英,王艳华,等.早期持续正压通气联合肺表面活性物质治疗早产儿肺透明膜病疗效评价[J].中国新生儿科杂志,2008,23(4):239-240.
[2]Narang A,Kurnar P,Dutta S,et al.Surfactant therapy for hyaline membrane disease:the Chandigarh experience[J].Indian Pediatr,2001,38(6):640-646.
[3]金汉珍,黄德珉,官系吉,主编.实用新生儿学[M].第3版.北京:人民卫生出版社,2002:421-428.
[4]赵祥文,主编.儿科急救医学[M].第3版.北京:人民卫生出版社,2010:276-279.
[5]袁 琳,陈 超.欧洲新生儿呼吸窘迫综合征防治指南2010版(译文)[J].中华儿科杂志,2011,49(1):27-33.
[6]周晓光,罗先琼,杨琳琳.肺表面活性物质治疗新生儿呼吸窘迫综合征的临床对照研究[J].中华儿科杂志,2000,38(8):490-493.
