羊毛角蛋白/羟甲基纤维素钠共混载药膜的制备及体外释药性能
2013-09-14曾春慧刘春光贾若琨
曾春慧,刘春光,贾若琨
(东北电力大学化学工程学院,吉林 吉林 132012)
我国羊毛资源丰富,每年废弃毛数量巨大,造成环境污染及资源浪费[1]。溶解废旧羊毛提取的角蛋白具有生物相容性、可降解性等优良特性[2-3],可作为天然高分子医用材料[4-5]。奥硝唑作为一种临床常用药物,直接用药在体内维持治疗时间短,见效慢[6]。本文以实验室自行提取的羊毛角蛋白为原料[7],与羟甲基纤维素钠溶液共混添加模型药物奥硝唑制备共混载药膜,并考察其体外释药性能。实验中提取的羊毛角蛋白是断裂羊毛分子二硫键,但主链仍保持完整的以α-螺旋结构为主的大分子量角蛋白分子,截留分子量在(8000-14000)以上,主链分子结构中含有大量的碱性和酸性侧基,且每个肽链两端有α-氨基和α-羧基,羟甲基纤维素钠(CMCNa)是一种水溶性纤维素醚,简化分子式为:Cell-O-CH2-COONa,分子中含有大量羟基、醚氧、羰基可与羊毛角蛋白分子中氨基、羧基形成氢键和离子键的特殊相互作用,从而阻止角蛋白分子内形成氢键,起到改变角蛋白分子结构的作用,使其分子链构象改变,从而改变其结晶态,直接有效地改善角蛋白膜的物理力学性能,以达到使用要求,并且两物质的侧链可以相互连接渗透,使二者均相成膜,趋于稳定。优化处方后制备的角蛋白高分子药物控释膜材[8],使药物在要求时间内以一定速度在体内缓慢释放,提高药物疗效及生物利用率,降低毒副作用,为药物载体开发利用提供试验基础。
1 实验部分
1.1 实验材料与仪器
羊毛角蛋白:自制;羟甲基纤维素钠和戊二醛:天津市瑞金特化学品有限公司;奥硝唑:(医用级)天津市华东制药厂;所有仪器:天津工业大学分析测试中心。
1.2 羊毛角蛋白/CMCNa共混载药膜的制备
羊毛角蛋白:羟甲基纤维素钠原料配比选取6040和5050(质量比),变性剂戊二醛用量0.1%,0.2%,37℃反应1 h。以上优选处方制备的共混膜拉伸强度适宜(25-30 N/mm),断裂伸长率大(20-35%),含水率(12-15%),透气率(80-85%)可作为载药膜的制备条件。将羊毛角蛋白和羟甲基纤维素钠溶液加入变性剂混合均匀后,分别加入5%和10%的奥硝唑溶液,充分搅拌,待其完全溶解稳定静止后,倾倒在玻璃板上自然流延,观察其共混溶液呈透明淡黄色,无尘粒堆积,原料物质以溶液状态均相混合,药物分散状态良好,经37℃烘干1小时,常温48小时后刮膜。
1.3 体外释药性能测试[9-10]
采用动态膜透析法,将载药膜封入透析袋中,置于200 mlpH=7.4的磷酸盐缓冲液中,温度(37℃)转速 100 r/min 恒温振荡,间隔一段时间,分别于1、2、3、4、5、6、7、8、10、12、14、18、24 h 定时从袋外缓冲液中取5 ml,同时补充等量介质溶液,用紫外分光光度计在药物最大吸收波长318 nm下测定释放液的吸光度,对照模型药物奥硝唑标准曲线,计算释药量和释药百分率。
1.4 贮存试验
将制备的共混载药膜保存在锥型瓶内,密封口,于37℃ 相对湿度75%条件下贮存6个月,检查外观、形态,测定其药物含量。
1.5 电镜测试
取膜样品,经离子溅射仪喷金,利用扫描电镜测试,观察载药膜表面及断面形貌。
2 结果与讨论
2.1 载药膜形貌
由图1和2 SEM照片可以看出共混载药膜断面比较致密、均匀,表面无明显大的裂纹与孔洞,成膜效果良好,已达到分子结合水平,共混组分相容性良好,药物分散状态均匀无颗粒凝结。膜的表面出现细小纹路,可能是由于测试过程中温度偏高以及膜具有一定的含水率未进行脱气处理所致。

图1 载药膜表面形态电镜照片
图2 载药膜断面形态电镜照片
2.2 原料配比的影响
药物的释放分为三个层次,首先是共混膜表层的药物分子快速释放到外界,所以从图3看出在起始1-3 h,两种配比的释药百分率即达到60-70%,药物突释。之后是分散在膜材料分子骨架之间的药物缓慢扩散到缓冲液中4-10 h,6小时的缓释效应。最后是埋裹在共混膜分子内部的药物几乎难以释放,在10-24 h释药百分率基本持平在93-95%。由图3可知角蛋白/CMCNa质量比6040时释药百分率大于质量比5050,角蛋白含量高,排列紧密的大分子链段及螺旋结构占主导,药物分子难以进入分子内部,所以分散在非晶区和膜材表面的药物占多数,后者羟甲基纤维素钠含量增加与角蛋白分子及变性剂形成氢键数目增加,阻止角蛋白分子内的氢键形成,所以药物分子相对分散在氢键及交联网状结构等分子骨架中较多,释放程度趋于缓慢,但配比5050的膜材吸水率溶失率偏高,强度下降。故选择6040配比最佳,兼顾药物缓释效应及优良性能。
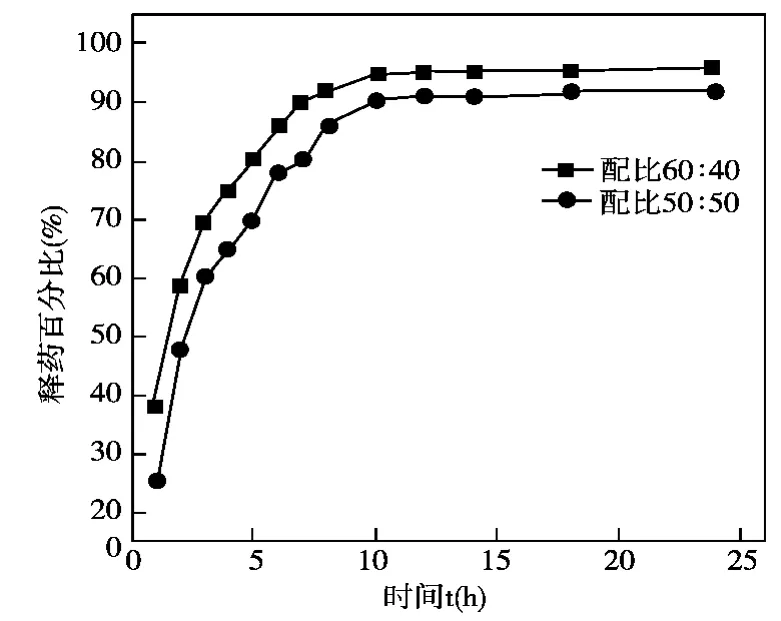
图3 原料配比对释药性能的影响
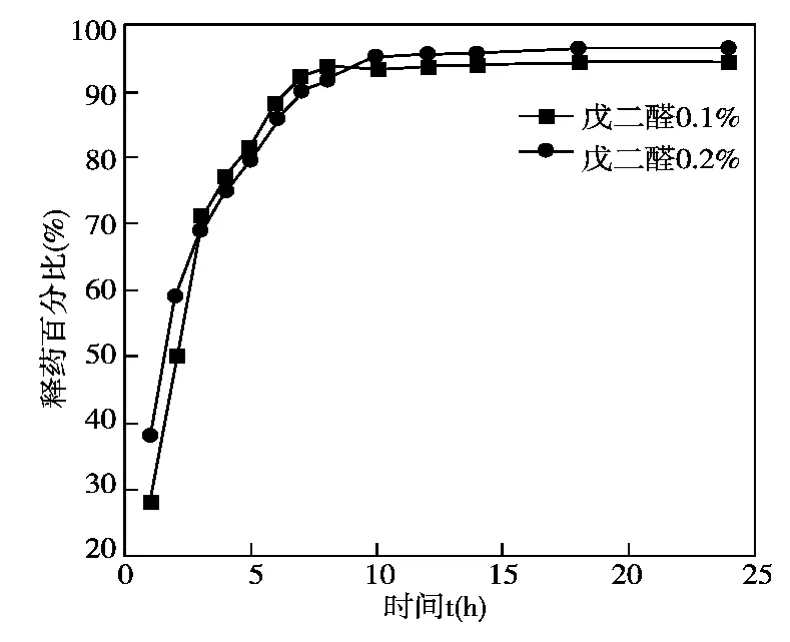
图4 变性剂用量对释药性能的影响
2.3 变性剂用量的影响
共混组分中加入变性剂戊二醛,起交联作用,改善膜的力学性能。每个戊二醛分子中含有2个醛基(—CHO),与角蛋白分子中的氨基(—NH2)发生交联反应,其实质是亲核加成反应之后再脱去一分子水形成C=N构造的化合物,导致角蛋白分子间形成交联网状结构,使肽链链段排列更加紧密。由图4可知起始阶段0.2%戊二醛载药膜突释效果强于0.1%戊二醛载药膜,戊二醛用量多,使角蛋白分子间交联结构增多,肽链链段紧密程度增加,所以较多的药物分子在角蛋白分子紧密链段之外和膜表面,开始阶段释药百分率较高,而在3小时之后0.1%戊二醛载药膜释药百分率略高于0.2%载药膜,由于戊二醛含量偏小,使角蛋白分子结构中亲水基团数目相对较多,而且角蛋白分子中链段排列不是特别紧密,缓冲液逐渐进入分子内部,更多的分子骨架中的药物分子溶于水中,扩散程度加快。选择0.1%戊二醛为最佳用量,保证药物缓释作用并且膜材的柔韧性和弹性优于0.2%戊二醛载药膜。
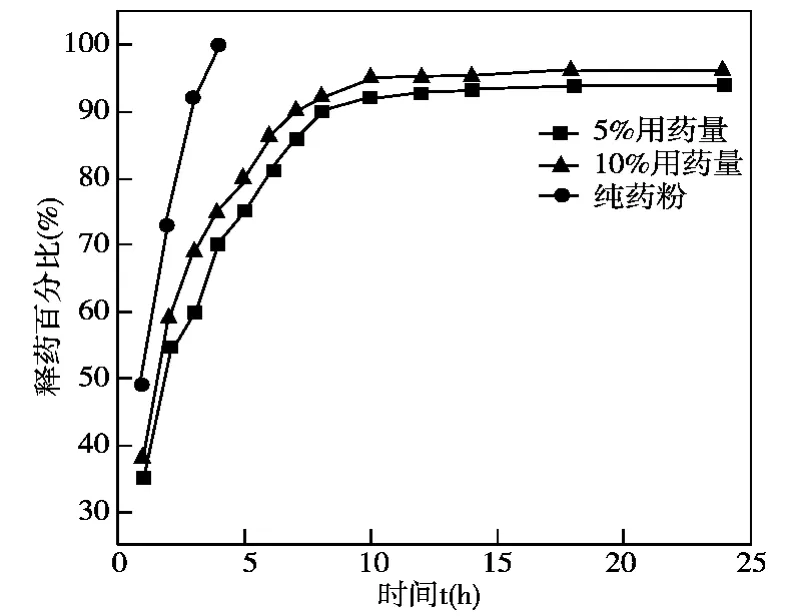
图5 药物用量对释药性能的影响

图6 pH值对释药性能的影响
2.4 奥硝唑用药量的影响
由图5可以看出纯药粉在4小时释放完全,达100%,释药速度快。10%用药量载药膜释药百分率高于5%用药量载药膜,因为用药量大,分散在膜表面、分子非晶区、分子骨架中的药量都相对高,所以在整个药物释放阶段释药百分率都较高。但无论5%或10%的载药膜都具有缓释效果,相比纯药粉可以释药10小时以上,更好的发挥药物疗效。
2.5 pH值的影响
由图6可以看出,载药膜释药百分率在pH=3.8时明显低于pH=7.4,在24小时仅释放40%左右,而在pH=7.4时可达95%,可以得出载药膜的释药性能具有pH敏感性,pH=3.8是羊毛角蛋白的等电点,溶解性能最低,不利于药物释放,所以不同的pH值对释药性影响较大。
2.6 贮存试验结果
六月后检查载药膜外观形态均无变化,测定载药量与释药百分率基本不变,波动2-5%。
3 结 论
本试验优化处方制备共混载药膜,在开始阶段药物出现突释效应,随之持续缓慢释放,释药时间在10 h左右,释药百分率达95%,不仅使药物迅速达到有效浓度并维持较长时间,而且可以降低体循环中药物浓度,提高药物治疗指数与用药安全,载药膜具有明显的pH值敏感性,在37℃条件下保存6个月状态稳定,为临床应用创造条件。
[1]汤燕伟,于伟东.羊毛溶液和角蛋白膜的实用制备技术与基本问题[J].膜科学与技术,2007,27(2):80-84.
[2]Li J S,Li Y,Li L,et al.Preparation and biodegradation of electrospun PLLA/keratin nonwoven fibrous membrane[J].Polym.Degrad.Stab.,2009,94(10):1800 -1807.
[3]Aluigi A,Vineis C,Ceria A.Composite biomaterials from fibre wastes:Characterization of wool-cellulose acetate blends.Composites[J].Composites Part A,2008,39(1):126 -132.
[4]张华林.羊毛角蛋白作为骨组织工程支架材料的研究进展[J].国际口腔医学杂志,2007,34(3):220-222.
[5]Reichl S.Films based on human hair keratin as substrates for cell culture and tissue engineering[J].Biomater.,2009,30(36):6854 -6866.
[6]Aluigi A,Vineis C,Varesano A,et al.Structure and properties of keratin/PEO blend nanofibres[J].Eur.Polym.J.,2008,44(8):2465 -2475.
[7]曾春慧.还原法与金属盐法结合溶解废旧羊毛[J].纺织学报,2011,32(11):12-16.
[8]翟延飞,谭福能.羟丙基壳聚糖-聚乙烯醇凝胶的制备与释药性能[J].济南大学学报,2009,23(2):170-175.
[9]徐倩.丝素/羧甲基壳聚糖共混及其双层复合载药膜的制备与性能研究[D].天津:天津工业大学,2008.
[10]韩永涛,黄桂华,席延卫等.阿奇霉素聚乳酸微球的制备及其体外释药特性的研究[J].山东大学学报,2006,44(8):853-856.
