顶空气相色谱法测定一次性使用无菌导尿管中环氧乙烷残留量
2013-09-14王刚林
张 成,王刚林
(1.陕西省医疗器械检测中心,陕西 西安 710075; 2.重庆医疗器械质量检验中心,重庆 401147)
作为临床上广泛使用的医疗器械,一次性使用无菌导尿管生产的原料主要有天然乳胶、硅橡胶和聚氯乙烯(PVC)等,很适合使用环氧乙烷灭菌。环氧乙烷是一种可刺激身体表面并引起强烈反应的易燃和易爆有毒气体,沸点为10.8℃,室温条件下很容易挥发成气体,进入人体可致突变,对胎儿产生毒性致畸,对睾丸功能也有不良影响,并能损伤体内器官。因此,对环氧乙烷的残留量必须严加控制。本试验中建立了一次性使用无菌导尿管中环氧乙烷残留量的测定方法[1],旨在确保产品的质量和安全性。
1 仪器与材料
Agilent 6890 N型气相色谱仪及工作站,Agilent G 1888型全自动顶空进样器,FID检测器(美国安捷伦科技有限公司);SPB-3型全自动空气源(北京中惠普分析技术研究所);SIMS 50000个人型纯水器(美国Millipore公司);氮气(纯度为99.999%)、氢气(纯度为99.999%)均购自四川梅塞尔气体产品有限公司西安分公司;BP 211D型分析天平(德国Sartorius公司);20 mL顶空瓶(美国安捷伦科技有限公司)。环氧乙烷对照品(规格为5 mL/支,含量为99.4%,批号为350001-201002,购自中国食品药品检定研究院;一次性使用无菌导尿管(批号分别为20100612,201010F3,200912H3,湛江市事丰实业有限公司),规格分别为双腔气囊标准型12 Fr(5~10 mL)、双腔气囊标准型14 Fr(5~10 mL)、双腔气囊标准型16 Fr(30 mL)。
2 方法与结果
2.1 色谱条件与系统适用性试验
色谱柱:P/N Agilent 19091 J-413 HP-5毛细管柱(30.0 m ×320 μm,0.25 μm)[1];柱温:80 ℃;进样口温度:150 ℃;载气:氮气(99.999%);流速:1.2 mL/min;分流比:5 ∶1;氢气流速:40 mL/min;空气流速:450 mL/min;尾吹气流速:40 mL/min。自动顶空进样器参数:平衡温度80℃;定量环温度90℃;传输线温度100℃;气相循环时间5 min;平衡时间8 min;加压时间0.05 min,进样时间1 min。在此条件下,理论塔板数按环氧乙烷峰计算为145 000,色谱图见图1。
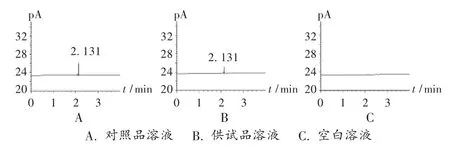
图1 高效液相色谱图
2.2 溶液制备
取一外部干燥的50 mL容量瓶,加超纯水约30 mL,精密称重。精密移取环氧乙烷对照品0.6 mL,迅速加入瓶中,摇匀,精密称重(两次称重之差即为溶液中所含环氧乙烷的质量),用超纯水稀释至刻度,摇匀,即得对照品贮备溶液(质量浓度为87.23 g/L)。精密移取对照品贮备溶液2 mL,稀释至100 mL,得质量浓度为1 744.6 μg/mL 稀释溶液,精密移取该溶液 5 mL,稀释至 50 mL,得质量浓度为174.46 μg/mL稀释溶液,再精密移取该稀释溶液0.3,0.6,1.2,2.4,4.8,9.6 mL,分别置 100 mL 容量瓶中,稀释至刻度,作为系列对照品溶液(质量浓度分别为 0.523 9,1.046 8,2.093 5,4.187 0,8.374 1,16.748 2 μg/mL)。取一次性使用无菌导尿管1 g,精密称定,剪碎,放入20 mL顶空瓶中,精密加入超纯水5 mL,作为供试品溶液。
2.3 方法学考察
线性关系考察:取系列对照品溶液,顶空瓶加样5 mL,按拟订的色谱条件测定环氧乙烷峰面积,以对照品峰面积为纵坐标(Y),对照品溶液质量浓度为横坐标(X)、绘制工作曲线,回归方程为Y=0.462 8X-0.048 39,r=0.999 97(n=6)。结果表明,环氧乙烷质量浓度在 0.523 4 ~16.748 2 μg/mL 范围内与峰面积呈良好的线性关系。
精密度试验:取质量浓度为4.187 0 μg/mL的同一对照品溶液,重复进样6次,测定环氧乙烷峰面积。结果的RSD=2.0%(n=6),表明仪器的精密度良好。
重复性试验:取样品适量,依法制备供试品溶液,平行6份,测定环氧乙烷残留量。结果残留量为 3.126 5 μg/g,RSD=2.3%(n=6),表明方法的重复性良好。
加样回收试验:取已测知含量的样品约0.5 g,精密称定,放入20 mL顶空瓶中,平行6份,分别加入质量浓度为1.0468 μg/mL环氧乙烷对照品溶液2 mL,加入超纯水补足5 mL。按拟订的色谱条件测定,计算回收率。结果见表1。

表1 环氧乙烷加样回收试验结果(n=6)
2.4 样品含量测定
取3批样品,依法制备供试品溶液,按拟订的色谱条件分别测定。结果批号为20100612,201010F3,200912H3的3批样品中环氧乙烷残留量分别为 3.13,3.10,2.85 μg/g(n=3)。
3 讨论
3.1 环氧乙烷残留量测定的国家标准
现行有效的国家标准GB 15980-1995《一次性使用医疗用品卫生标准》[2]、GB 15979-2002《一次性使用卫生用品卫生标准》[3]中对于环氧乙烷残留量的测定方法是采用填充柱和液体直接进样的方式。而 GB/T 16886.7-2001《医疗器械生物学评价第 7部分:环氧乙烷灭菌残留量》[4]及 GB/T 14233.1-2008《医用输液、输血、注射器具检验方法第1部分:化学分析方法》[5]作为医疗器械行业目前广泛引用的两个标准,其中对于环氧乙烷残留量的测定方法仅规定了一个指导性方法。为此,参照上述国家标准对一次性使用无菌导尿管的环氧乙烷残留量检测方法进行了较详细的考察。采用顶空进样毛细管气相色谱法测定,3批样品的检测结果均符合现行标准的规定(环氧乙烷残留量应不超过10 μg/g)。此方法快速简便、结果准确、可靠、重现性好,可作为一次性使用无菌导尿管环氧乙烷残留量的检测方法。
3.2 气相色谱及顶空条件
本试验中所采用的方法是顶空毛细管气相色谱法,对60,70,80,90℃等毛细管柱温温度进行了考察,结果当柱温为80℃时,环氧乙烷的峰形较好、灵敏度高;对顶空条件也进行了考察,在同样的测定条件下比较了60,70,80,90℃等顶空平衡温度,结果80℃和90℃时环氧乙烷峰面积积分值较大且相当,说明80℃时环氧乙烷逸出较完全,故选择顶空平衡温度为80℃;对5,8,10 min顶空平衡时间进行比较,结果平衡时间选择8 min时,环氧乙烷的灵敏度较高,可以满足实际要求。
[1]国家药典委员会.中华人民共和国药典(二部)[M].北京:化学工业出版社,2010:附录ⅤD.
[2]GB 15980-1995,一次性使用医疗用品卫生标准[S].
[3]GB 15979-2002,一次性使用卫生用品卫生标准[S].
[4]GB/T 16886.7-2001,医疗器械生物学评价 第7部分:环氧乙烷灭菌残留量[S].
[5]GB/T 14233.1-2008,医用输液、输血、注射器具检验方法 第1部分:化学分析方法[S].
