柱前衍生-高效液相色谱法快速测定含乳饮料中的甜蜜素
2013-09-07何晓玲福建省晋江市质量计量检测所
何晓玲 / 福建省晋江市质量计量检测所
0 引言
甜蜜素(Sodium cyclamate)化学名称为环己基氨基磺酸钠,分子结构式为C6H11NHSO3Na,是一种人工合成的甜味剂,味道清甜,甜度为蔗糖的40~50倍,为无营养甜味剂。作为人工合成甜味剂,甜蜜素被广泛应用于食品行业,如饮料、蜜饯、糕点等食品中。由于有研究表明甜蜜素可能在肠菌作用下分解为有慢性毒性的环己胺,可能导致膀胱癌,所以美国、英国、加拿大、日本等国禁止使用甜蜜素作为食品添加剂,我国对甜蜜素的使用也有强制限量的规定[1]。
目前已建立的食品中甜蜜素检测方法主要有:气相色谱法[2,3]、比色法[4]、薄层层析法[5]、高效液相色谱法[6]、气质联用法[7]、液质联用法[8]等。比色法和薄层层析法操作较为繁琐且灵敏度不高,已基本不使用;气相色谱法的衍生产物不稳定,易分解,且保存条件苛刻;气质联用法和液质联用法操作简单、检出限低,但仪器昂贵,不适合作为基层检验机构日常快速检测使用方法;近年来液相色谱法检测甜蜜素日益受到研究人员的关注并进行了相关报道,其衍生产物常温下性质稳定,灵敏度高,检出限低,仪器要求不高,检测过程简单方便,目前尚未见有关含乳饮料基质中甜蜜素检测方法的报道。本文通过优化含乳饮料中甜蜜素液相检测方法的前处理过程,建立了柱前衍生-高效液相色谱法分离检测含乳饮料中甜蜜素的方法。
1 实验部分
1.1 仪器
2695高效液相色谱仪(美国waters公司),配有2998 PDA检测器、四元泵、在线真空脱气机、柱温箱、自动进样器;320R离心机(德国Hettich公司);AXL阿修罗实验室超纯水机;0.45μm尼龙滤膜(津腾)。
1.2 试剂
甲醇,乙腈(HPLC级,沃凯);其余试剂均为分析纯,实验用水为超纯水。正己烷(国药集团化学试剂有限公司);乙酸铅溶液(22 g/L),次氯酸钠溶液(1 : 1),硫酸溶液(1 : 1);碳酸氢钠溶液(10%),氯化钠(西陇化工股份有限公司)。
甜蜜素标准物质(纯度99.8%,北京上立方联合化工技术研究院)。
1.3 色谱分析条件
色谱柱:Waters SunFire C18 (4.6 mm×250 mm,5 μm);流动相:甲醇:水= 85 : 15;检测波长:311 nm;流速:1.0 mL/min;柱温:35 ℃;进样量:10 μL。
1.4 样品处理
称取混匀后的含乳饮料样品10 g,缓慢加入3.0 mL乙酸铅溶液,摇匀,静置30 min,6 000 rpm离心15 min后过滤,取上清液加入1.0 mL硫酸溶液,摇匀后加入2.0 mL次氯酸钠溶液,振摇2 min,加入2 g氯化钠和5.0 mL正己烷,振摇2 min后静置分层,取正己烷层加入20.0 mL碳酸氢钠溶液充分振摇,取正己烷层经0.45 μm膜过滤后进液相色谱进行分析。
1.5 标准溶液制备
1.5.1 标准储备液
准确称取甜蜜素标准品100.0 mg溶于超纯水并定容至100.0 mL容量瓶中,作为标准储备液,浓度为1.0 mg/mL,临用前用超纯水稀释。
1.5.2 标准工作溶液
使用前用超纯水稀释为0.01 mg/mL、0.02 mg/mL、0.05 mg/mL、0.10 mg/mL、0.20 mg/mL、0.50 mg/mL的标准工作溶液。
1.5.3 标准工作曲线测定
分别吸取10.0 mL甜蜜素标准工作溶液,加入1.0 mL硫酸溶液,摇匀后加入2.0 mL次氯酸钠溶液,振摇2 min,加入2 g氯化钠和5.0 mL正己烷,振摇2 min后静置分层,取正己烷层加入20.0 mL碳酸氢钠溶液充分振摇,分层后取正己烷层经0.45 μm膜过滤后进液相色谱进行分析。
2 结果与分析
2.1 样品预处理方式选择
甜蜜素稳定性好,对热、光、空气、酸、碱均稳定,不溶于乙醇、乙醚、苯和氯仿等,在水中的溶解度大,能达到200 g/kg。本实验的样品基质是蛋白质、固形物,食品添加剂丰富的含乳饮料,蛋白质的大量存在影响衍生产物的萃取过程,产生大量难以消解的泡沫,萃取分层困难,所以在前处理方法中重点考察甜蜜素与蛋白质、固形物等的分离。
本实验选取乙酸铅溶液、三氯乙酸溶液对样液进行预处理,6 000 rpm离心15 min取上清,三氯乙酸溶液沉淀效果不佳,故排除。考察含乳饮料加标,经乙酸铅溶液前处理后,离心取上清液,按1.5.3 加入1.0 mL硫酸溶液等步骤进行检测,选取乙酸铅溶液作为样品中蛋白质及其他大分子极性物质沉淀剂。其沉淀效果好、速度快、不影响目标产物回收率。
2.2 衍生化方法的优化
衍生效率直接影响方法的回收率和精密度,故本实验着重对甜蜜素的柱前衍生方法进行了优化,主要考察衍生处理中的pH、衍生剂加入量、正己烷加入量、氯化钠加入量、碳酸氢钠加入量等参数对于衍生效果的影响。
2.2.1 pH
本实验的衍生反应是在强酸性条件下进行的,所以首先研究pH对衍生化效果的影响。取3份浓度为0.50 mg/mL的甜蜜素标准工作溶液10.0 mL,分别加入1.0 mL、3.0 mL、5.0 mL硫酸溶液,按1.5.3方法进行检测,由实验结果可知当硫酸溶液加入量为1.0 mL时,已能满足衍生反应条件要求。
2.2.2 衍生剂加入量
本实验的衍生剂是次氯酸钠,故次氯酸钠加入量直接影响到衍生反应是否能进行得完全。取5份10.0 mL浓度为0.50 mg/mL的甜蜜素标准工作溶液,按1.5.3方法进行检测,其中衍生剂加入量分别为0.5 mL、1.0 mL、2.0 mL、3.0 mL、5.0 mL 次氯酸钠溶液,实验结果见图1,表明衍生剂加入量为2.0 mL时已能满足衍生反应要求。
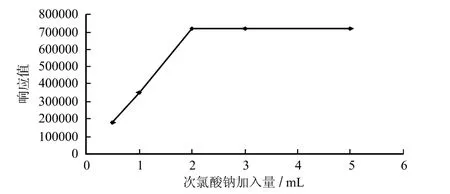
图1 衍生剂加入量
2.2.3 正己烷加入量
本实验的萃取溶剂是正己烷,取4份10.0 mL浓度为0.50 mg/mL的甜蜜素标准工作溶液,按1.5.3方法进行检测,其中正己烷的加入量分别为2.5 mL、5.0 mL、7.5 mL、10.0 mL,理论上正己烷的加入量应与响应值成反比,研究结果见图2,表明当正己烷加入量<5.0 mL时,响应值不成比例增加,说明萃取效率降低。当正己烷加入量≥5.0 mL时,响应值随着正己烷加入量的增加成比例减少,表明正己烷加入量为5.0 mL时已能满足萃取衍生物的要求。若要减少正己烷用量,可用增加萃取次数来提高衍生物提取效率。

图2 正己烷加入量
2.2.4 氯化钠加入量
反应中加入氯化钠是为了增加盐析,改善衍生物N,N-二氯环己胺在水相和有机相的分布,提高萃取效率。实验考察了氯化钠在衍生反应前添加、在反应后添加和不添加三种情况,取3份10.0 mL浓度为0.50 mg/mL的甜蜜素标准工作溶液,按1.5.3方法进行检测,结果表明在衍生反应后添加再进行萃取既不影响衍生反应产物的生成又能提高反应效率。
2.2.5 碳酸氢钠加入量
衍生反应萃取后,用10%碳酸氢钠溶液对正己烷层进行洗涤的目的是为了中和过量的硫酸溶液和次氯酸钠溶液,保护液相色谱管路和液相色谱柱的使用寿命。实验对此进行了研究,结果表明碳酸氢钠溶液加入量为15.0 mL时已能满足实验要求。
2.2.6 优化结果
经过实验优化,确定最佳的衍生化条件为:硫酸溶液加入量为1.0 mL,次氯酸钠溶液加入量为2.0 mL,正己烷加入量为5.0 mL,氯化钠在衍生反应后添加再进行萃取,碳酸氢钠溶液加入量为15.0 mL。以下实验均按照最优化结果进行。
2.3 仪器方法的选择
2.3.1 测定波长
甜蜜素在酸性条件下经次氯酸钠衍生,正己烷萃取的衍生物为N,N-二氯环己胺,对其在190~400 nm波长范围内进行全波长光谱扫描,发现在205.3 nm和311.8 nm处有强吸收峰,考虑到210 nm处流动相中的甲醇和许多杂质在此有强吸收干扰,故选择311 nm为检测波长(图3)。

图3 衍生物N,N-二氯环己胺紫外吸收光谱图
2.3.2 流动相
流动相对样品的分离有很大影响,实验比较了甲醇-水、乙腈-水两种流动相体系的分离效果,实验结果表明两者无明显差别;实验考察0.02 mol/L乙酸铵代替水作为缓冲溶液对分离效果的影响,结果表明未见明显差别,不影响色谱峰形,故测定时选用甲醇-水体系并通过实验确定甲醇-水的配比为85 : 15,甜蜜素衍生物的液相色谱图见图4。
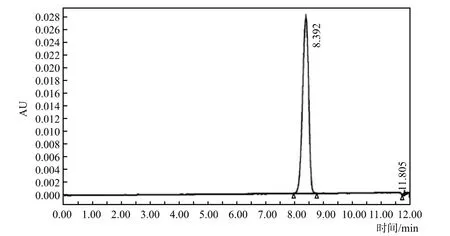
图4 甜蜜素衍生物N,N-二氯环己胺液相色谱图
2.4 标准曲线回归方程及相关系数
将1.5.2中制备好的甜蜜素标准工作溶液按2.2.6方法进行衍生化, HPLC测定,对峰面积和甜蜜素的质量浓度进行线性回归,结果可知,甜蜜素在0.01~0.50 mg/mL范围内有良好的线性关系,相关系数为0.999 4。
本方法对含乳饮料中甜蜜素测定的最低检出限为0.5 mg/kg。
2.5 回收率和精密度实验
采用含乳饮料基质添加甜蜜素标样进行回收率实验,所用的含乳饮料的本底不含甜蜜素的阴性样品,分别添加20 mg/kg、50 mg/kg、100 mg/kg,按照2.2.6方法进行衍生化,HPLC进行甜蜜素含量测定,计算甜蜜素回收率,每个水平进行n = 6次重复试验,计算平均回收率和相对标准偏差,结果见表1,测定实际样品的液相色谱见图5。
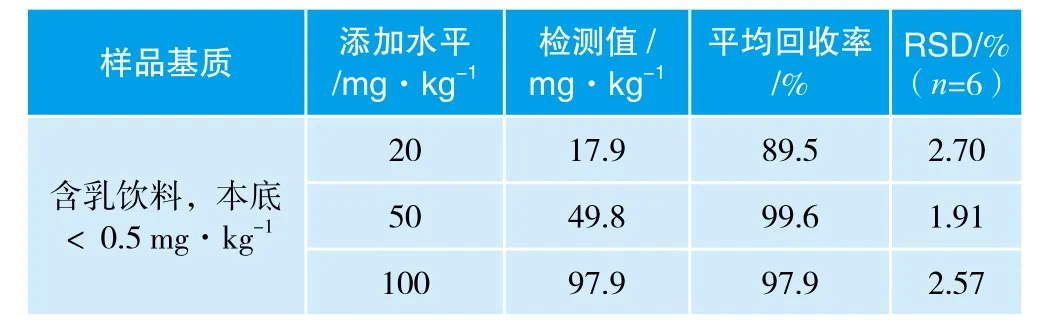
表1 方法精密度和回收率实验结果(n=6)
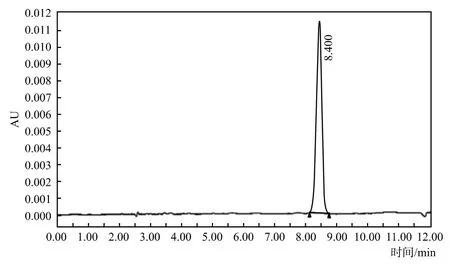
图5 N,N-二氯环己胺液相色谱图
2.6 稳定性测试
将N,N-二氯环己胺的正己烷提取物放置于室温(20~25℃)和冰箱(4℃)保存,第1 d、3 d、6 d分别测定其峰面积,响应值均未见明显变化,说明N,N-二氯环己胺在室温及(20~25℃)和冰箱(4℃)条件下是稳定的。
3 结语
本文针对市售的含乳饮料进行了前处理研究,对甜蜜素进行了衍生化、萃取过程的优化,建立了含乳饮料中快速检测甜蜜素的高效液相色谱分析定量方法,衍生产物常温下稳定,检出限低,方法精密度、回收率高,均符合日常检测要求,对于其他基质复杂的产品检验有借鉴价值。
[1]中华人民共和国卫生部. GB 2760-2011 [S]. 北京:中国标准出版社,2011.
[2]中华人民共和国卫生部. GB/T 5009.97-2003 [S]. 北京:中国标准出版社,2003.
[3]洪晓峰. 气象色谱法测定酱油中甜蜜素含量的探讨[J]. 福建分析测试,2012, 21(2):42-44.
[4]陈少波,潘超华. 食品中甜蜜素的紫外分光光度法测定[J]. 分析测试学报,2000, 19(3):82-83.
[5]刘维华,郭银燕. 薄层层析法同时测定饮料中甜蜜素和糖精钠[J]. 中国公共卫生,2000, 16(8):766.
[6]王敏,郭德华,韩丽,等. HPLC法快速分离和检测食品中微量甜蜜素含量[J]. 中国卫生检验杂志,2007, 8(17): 1421-1422.
[7]胡强,王延云. 气相色谱-质谱法对不同食品中甜蜜素的测定[J].食品科学,2009, 30(14):235-237.
[8]徐琴,牟志春,郝杰. 液相色谱-质谱法测定输韩泡菜中的甜蜜素[J]. 食品科学,2012,33(04):186-188.
