饲料中粗蛋白含量的测定方法
2013-08-25李晴媛徐晓娜
李晴媛 徐晓娜
(河南省洛阳市质量技术监督检验测试中心,洛阳 471000)
饲料中粗蛋白含量的测定方法
李晴媛 徐晓娜
(河南省洛阳市质量技术监督检验测试中心,洛阳 471000)
粗蛋白含量是饲料产品质量检测的重要控制指标。饲料样品中粗蛋白质含量的高低,是评定饲料营养价值的重要因素,决定着配合饲料及饲料原料的成本和价值。近年来,我国饲料工业发展迅速,饲料产量也随之增长,市场上出售的饲料种类繁多,质量良莠不齐。国标法测定饲料中的粗蛋白采用的是凯氏定氮法,由于操作的过程比较复杂,如果操作不当,往往会导致检测结果不准确。
1 样品制备
一般的饲料样品都是经过一定的采集过程后送检的。采集方法是否规范,是粗蛋白测定准确与否的基础。采样方法随不同的物品而有所不同,一般来说,可根据物品均匀性质分为下列两种[1]。
1.1 均匀性质物品
对于均匀性质的物品,每一小部分的成分与全部的成分相同,可以采取其任何一部分作为分析样本。在通常情况下,粉末或研碎后的样品可用“四分法”来采样。
1.2 不均匀性质物品
不均匀的物品,须采取多量样本,然后在取出的样本中重复取样多次,得出一连串逐渐减少的样本,叫做初级、次级、三级……样本。分析用的样本可以在最末一级样本中制备,使样本能代表全部物品。所采用的取样方法称为“几何法”。
经过采集的样品部分基本代表全部样品的成分,但是,由于饲料在生产过程中的工艺限制,样品颗粒并不均匀,所以在实验前要通过样品粉碎来实现称量样品的均匀性。
根据饲料工业标准标定,样品要求粉碎后全部通过40目(0.45 mm)分样筛,然后混合均匀放入密封容器[2]。一般饲料样品颗粒较大,成分复杂,检测时称量样品量较少,如果细度不够,必然造成称样时样品不均匀,这是造成结果误差的重要原因。
2 称样
用分析天平称取试样0.5~1 g(精确到0.000 1),标准要求做平行样以保证测量结果的准确性,所以需要称样2份。称样时的称样量要合适,不能太少也不能太多。一般粗蛋白含量在10%以上的饲料称样量为0.500 0 g即可;若饲料样品中粗蛋白含量较低,如含量为3%~5%的,称样量就应高于0.5000 g,一般称取1.000 g样品,否则,测定结果的误差就会偏大。
3 消化
凯氏测定法的原理是,饲料样品在催化剂的作用下,用硫酸消煮分解,使蛋白质及其他化合物中的氮转化为硫酸铵,硫酸铵在浓碱(一般使用浓度为40%的氢氧化钠溶液)的作用下放出氨气,通过蒸馏,氨气用过冷凝管的冷却回流进入吸收瓶中,与吸收液中的硼酸溶液结合生成四硼酸铵,再用盐酸标准溶液滴定,即可测定出氨氮量,根据滴定得到的氮含量,乘以换算系数6.25,计算出粗蛋白含量[3]。在这个测定过程中,消化过程是非常重要的环节,是决定蛋白质测定成败的关键。
3.1 硫酸加入量
要根据样品的用量来确定硫酸的用量,一般硫酸应加20~30 ml,对于含盐量高的样品,如某些劣质鱼粉、肉骨粉之类,须相应增加硫酸用量,因为存在2NaCl+H2SO4==2HCl↑+Na2SO4反应,会消耗一部分的硫酸,反应产生的HCl加热后挥发,对整个反应无影响。
3.2 消化温度与速度
消化时速度要缓慢,开始要用小火,待样品焦化后,逐步缓慢加强火力。如果升温过快,则部分含氮物质来不及转化成硫酸铵而以气体形式损失掉,会造成检测结果偏低,此时最好能在烧瓶口部加上一个小漏斗,形成回流,延缓蒸发损失。还要注意的是,在消化过程中饲料样品容易飞溅,因此在消化过程中间,必须将溅到瓶壁上的黑渣摇入瓶底硫酸溶液中,或用少量硫酸沿容器壁冲洗,以避免样品消化不完全。消化时要控制好温度,以380℃时最宜,最好采用可调式电炉。
3.3 催化剂的使用
在实验过程中一般会在消化液中加入大量硫酸钾[2]或硫酸铜,其目的是用于提高消化温度。
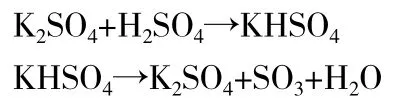
消化过程中,随着硫酸的分解和水分的蒸发,硫酸钾的浓度逐渐增大,消化液沸点升高,加速了有机物的分解速度。但应注意硫酸钾的用量不能过大,如果消化温度太高,生成的硫酸铵也会分解出氨而使测定结果偏低。
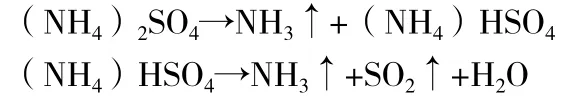
在消化液冷却后呈固态,则表明硫酸钾用量过大,或硫酸用量不足。事实上,增加试样量和硫酸量,其混合催化剂的量不必增加。
在试样消化过程中,硫酸铜的催化反应如下:
除硫酸铜外,常用的催化剂还有汞、氧化汞、硒粉、还原铁或上述物质的混合物。对于一般谷物样品,如玉米、小麦、稻谷等的消化,用硫酸铜作催化剂,只要适当增加盐用量,使用强热源,其效果与汞催化剂完全一样;对于难消化物质的样品,硫酸铜催化效果不如汞,测得蛋白质含量偏低。用硫酸铜作催化剂的好处,是在蒸馏氨时可作为碱性反应的指示剂。
添加氧化剂可帮助有机质消化,但氧化性较强的氧化剂会使氨氧化为氮气损失。对于富含脂肪或消化过程中易发泡的样品,可在消化前添加少量氧化剂,如过氧化氢,一般不用高锰酸钾和次氯酸作氧化剂。
有的饲料检测书上有快速测定蛋白质的方法,如硒粉催化法、硒粉过氧化氢催化法、过氧化氢催化法等,按照这些方法测定的蛋白质含量常常偏低0.3%~1.0%,如无特殊情况,特别是测定的结果作为饲料配方的数据时,不要用快速测定法。
3.4 注意事项
消化时还应在凯氏瓶内加几粒玻璃珠,用以防止硫酸涨沸流失;在凯氏烧瓶口盖一个小漏斗,使蒸汽凝结回流,这样会使测定结果更准确。当消化液达到透明状态时,并非表示样品已消化完全,为防止结果偏低,至少还需加热消化2 h左右。
4 转移
蛋白质测定过程中的转移过程也是关系到测定结果准确与否的重要步骤,这个过程需要注意的问题有以下几点:第一,防止烧伤。由于消化后的样品溶液中硫酸的含量较高,在烧瓶中加入水后会产生热量,容易造成烫伤,不能直接用手去摸烧瓶底部,整个转移过程都要尽量接触烧瓶瓶颈上部。第二,防止洒漏。由于烧瓶口无遮拦,在转移过程中容易使溶液损失,增加误差,这就要求操作过程谨慎准确,通过玻璃棒的引流和漏斗,快、准、稳的进行转移。第三,加水和冲洗过程要掌握少量多次,全部无损失地转移[4]。
5 蒸馏
氨的蒸馏有两种方法:常量蒸馏法和半微量蒸馏法。常量法将样品分解消化后全部用于测定,取样量大,测定结果的准确性和精确度都很高。半微量法测定结果精密度稍差一点。
蒸馏时要注意两点,一是反应容器里的溶液总体积要控制,也就是说,在冲洗加样口时用水要少,否则反应室溶液体积太大,液面升高,容易喷进冷凝管内。二是要控制蒸汽量或火力大小,蒸汽量太大也会将反应液喷进冷凝管中;火力太小,蒸馏速度慢,且易发生倒流;蒸汽产生要均匀,防止暴沸;一定要装上蒸汽发生器的安全管,同时加上几粒玻璃珠。
6 滴定
滴定用的盐酸标准溶液浓度必须准确。标准溶液在使用前应将溶剂瓶上下摇动几次,以便使凝结到瓶壁上的水珠完全溶入溶液之中,保证溶液浓度均匀一致。滴定时注意排除滴定管底部的气泡,确保滴定结果准确。
7 空白检测
空白测定是衡量整个操作过程中一个非常重要的综合性指标,良好的空白值是保证检测结果准确的前提,空白值不能超过标准范围。检测时如果发现空白值过高,应认真查找原因并及时解决。空白值超标一般是由于所用试剂级别不够、试验用水不纯或玻璃器皿不干净等原因造成的。
在日常工作中,应严格遵守操作规程,掌握好操作条件,在每一步操作中应尽量避免氮的损失,消除由于反应不完全对测定结果的影响,取得较为准确的分析结果。
[1] 张静.浅谈怎样提高饲料中粗蛋白测定的准确度[J].贵州畜牧兽医,2009,(1):9.
[2] 谢飞文.凯氏定氮法测定饲料粗蛋白的注意细节[J].饲料广角,2003,(14):17-18.
[3] 韩丹.浅谈影响饲料中粗蛋白测定准确度的几个因素[J].现代畜牧兽医,2010,(5):36-37.
[4] 曹雨莉,李芳林,薛桥.饲料样品粗蛋白质测定过程中应注意的几个问题[J].中国牛业科学,2007,33(2):43-44.
