不同分子量壳聚糖微凝胶的制备及溶胀性能研究
2013-08-06陈世兰夏培源周小涛
陈世兰,夏培源,陈 勇,周小涛,遇 丽,王 月
(重庆科技学院 化学化工学院,重庆 401331)
1 引言
壳聚糖(CS)生物相容性好,无毒,可生物降解,经微凝胶化后,可改善其物理、化学特性,如增加药物吸收、提高药物稳定性、增强药物的缓释作用、增强药物靶向性等[1,2].乳化交联法是制备壳聚糖微凝胶的一种重要方法,此方法是指在油相中乳化壳聚糖水溶液形成油包水(w/o)乳液,然后用交联剂加固液滴形成壳聚糖微凝胶的方法.微凝胶比表面积较大,对物质分子的吸附能力增强,因此其不但可应用做药物缓释载体,还可用做废水处理剂、催化剂载体等[3,4].本文采用三聚磷酸钠(TPP)为离子型交联剂,乳液交联法制备CS微凝胶,优化微凝胶的制备条件,以制得不同分子量CS微凝胶,分析分子量对CS微凝胶溶胀性能的影响.
2 实验部分
2.1 实验试剂及仪器
壳聚糖(粘均分子量约为10w、20w、30w,脱乙酰度约为86%)购于浙江金壳生物化学有限公司;三聚磷酸钠(A.R.)重庆博艺化学试剂有限公司;其它试剂均为分析纯.
2.2 壳聚糖微凝胶的制备
将壳聚糖溶解在醋酸水溶液中,加入含一定量乙酸乙酯的圆底烧瓶中,随后加入一定量混匀的司班80与吐温80,搅拌形成稳定的w/o型的壳聚糖乳液.再加入TPP溶液室温下反应2h,分离、洗涤得壳聚糖微凝胶.微凝胶真空干燥备用.
2.3 结构表征
将CS及干燥后的CS微凝胶经KBr压片,采用傅里叶变换红外光谱(FTIR)检测CS和CS微凝胶的结构.
2.4 性能检测
称取一定质量(m1)干燥的CS微凝胶装入质量为m2的湿布袋中,浸泡在一定pH值的缓冲溶液中至微凝胶溶胀平衡后,将布袋悬挂至无液体析出后,用滤纸吸干布袋表面水,称其质量m3,计算微凝胶的溶胀比(SR):

3 结果与讨论
3.1 FTIR光谱图
图1为CS和CS微凝胶的红外光谱图.从图中可以看出,壳聚糖的酰胺I谱带和II谱带分别出现在1664cm-1和1582cm-1,此类峰在CS微凝胶分别迁移至1640cm-1和1541cm-1,是由于三聚磷酸钠与壳聚糖的氨基相互作用,导致氨基中的电子云发生偏移,从而红外吸收向低波数移动,这是三聚磷酸钠与壳聚糖的-NH3+发生了离子交联的结果[5].1082cm-1的振动峰明显增强,为CS骨架C-O-C和TPP中P=O基团共同作用的结果.

图1 壳聚糖(a)及壳聚糖微凝胶(b)红外光谱图
3.2 醋酸浓度对微凝胶溶胀性能的影响
从图1中可知,随着HAc浓度增大,CS微凝胶的溶胀比先增大后减小.当CHAc<0.13mol/l时,HAc浓度增大,CS的质子化程度越大,与三聚磷酸钠的交联程度增大,微凝胶网孔增多,SR增大;当CHAc>0.13mol/l时,醋酸浓度过大,尽管CS的质子化程度会增大,但体系酸度过大,三聚磷酸钠的离子化程度降低,微凝胶交联程度降低,网孔减少,SR降低.

图2 醋酸浓度对壳聚糖微凝胶溶胀性能的影响(MCS=20w,pH=5.01)
3.3 三聚磷酸钠用量对微凝胶溶胀性能的影响
从图2中可知,随交联剂用量增大,壳聚糖微凝胶的溶胀比先增大后减小,其原因是交联剂与壳聚糖的质量比(mTPP:CS)低于0.15时,随交联剂用量增大,微凝胶的交联程度增大,凝胶网孔增多,对溶胀介质水的吸收固定程度较大,SR增加;当mTPP:CS>0.15时,交联剂用量过大,使凝胶网孔过多,网络密度过高,导致凝胶对水的吸收能力降低[6].

图3 交联剂用量对CS微凝胶溶胀性能的影响(MCS=20w,pH=5.01)
3.4 壳聚糖浓度对微凝胶溶胀性能的影响
从图4可知,当壳聚糖浓度(CCS)从1%增至2.5%时,微凝胶溶胀比逐渐增大,原因是增多的壳聚糖分子链之间的相互缠结程度增大,且与交联剂的交联程度也增大,微凝胶对溶胀剂水分子的束缚能力增强,SR增大;当CCS>2.5%时,壳聚糖分子链之间的强缠结作用及与交联剂的强交联程度使微凝胶网孔数增大但孔径减小,对水分子的吸收能力减小,SR降低.

图4 壳聚糖浓度对壳聚糖微凝胶溶胀性能的影响(MCS=20w,pH= 5.01)
3.5 油水比对微凝胶溶胀性能的影响
从图5可知,当油水比小于1.20:1时,随油相体积的增大,可能使微凝胶的粒径减小,微凝胶比表面积增大,微凝胶对水分子的吸水能力增强,SR增大;油水比大于1.20:1时,尽管此时微凝胶的比表面积增大了,但微凝胶吸水后的强度会因吸水量过多而减小,凝胶控水能力不足,SR下降.
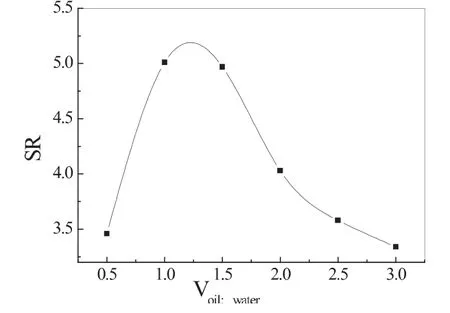
图5 油水比对壳聚糖微凝胶溶胀性能的影响(MCS=20w,pH=5.01)
3.6 不同分子量壳聚糖对微凝胶溶胀性能的影响
从图6中可知,pH=1.8时微凝胶溶胀比随着CS分子量增大减小.壳聚糖分子量增加即分子链长度增大,分子之间的相互缠结程度增大,使微凝胶网孔数增多但孔径减小,进入凝胶网孔的水分子减少,SR降低.pH=7.4时微凝胶SR较低,在该pH介质中由于微凝胶骨架壳聚糖中氨基的质子化程度降低,骨架分子链内或链间的静电斥力减小,凝胶网孔处于收缩状态,微凝胶SR低.在NaCl浓度较高的介质中,微凝胶的SR也较低,原因是溶胀介质盐浓度越大,微凝胶与介质的渗透压差减小,水分子更难进入凝胶网络,SR较低.在高pH和高盐浓度介质中,由于此时低的溶胀程度使分子量对凝胶溶胀性能的影响不明显.

图6 不同分子量壳聚糖在不同介质中的溶胀比
4 结论
壳聚糖溶剂醋酸溶液的浓度、壳聚糖浓度、交联剂用量及油水比均对壳聚糖微凝胶的溶胀性能有显著的影响,在以上参数分别为0.13mol/l、2.5%、0.15和1.20:1时微凝胶的溶胀能力最大.pH=1.8的介质中壳聚糖的分子量明显影响着微凝胶的溶胀比,即随分子量增大而溶胀比降低;微凝胶的溶胀还依赖于介质的pH值和盐浓度,因此,可通过选择制备条件和壳聚糖分子量实现对壳聚糖微凝胶溶胀性能不同要求的应用.
〔1〕王薇薇,何钢,王琼.壳聚糖纳米微粒制备条件的优化及其应用[J].中南林业科技大学学报,2012,32(2):95-99.
〔2〕李国明,叶俊生,郑国红,刘聪汪,朝阳.左旋多巴-壳聚糖微球的制备及其释药性能[J].应用化学,2007,24(9):1062-1065.
〔3〕M.A.Vitae,S.G.Vitae,A.B.Vitae,Frank Marken.Carbon nanoparticle–chitosan composite electrode with anion,cation,and neutral binding sites:Dihydroxybenzene selectivity.2012,162(1):194-200.
〔4〕I.B.Tsvetkova,L.M.Bronstein,S.N.Sidorov,O.L.Lependina.Structure and behavior of nano-particulate catalysts based on ultrathin chitosan layers.Journal of Molecular Catalysis A:Chemical,2007,276(1–2):116-129.
〔5〕权维燕,李思东,董静静,郑彦丽.利巴韦林-壳聚糖微粒的制备及载药特性.广州化工,2010,38(4):84-86.
〔6〕王彦,赖克方,张巧,马千里,王长征.离子凝胶法制备壳聚糖纳米微粒的影响因素分析.山东医药,2011,5l(27):13-15.
