蒽酮比色法测定马铃薯淀粉总糖的条件研究
2013-07-22翁霞辛广李云霞
翁霞,辛广,李云霞
(鞍山师范学院化学与生命科学学院,辽宁鞍山 114007)
马铃薯(Solanttm tubersum)又名土豆、山药、洋番薯等。主要产区在东北的中北部、华南西部、内蒙古和西北及西南各省山区[1]。在马铃薯中,淀粉的含量约为23%[2],马铃薯碳水化合物中可溶性糖主要有葡萄糖、果糖、蔗糖,测定马铃薯中糖的含量具有重要意义。有研究表明,还原糖含量作为油炸加工企业重要的检测指标,是决定马铃薯炸片、炸条加工品质的重要因素。因为在油炸过程中还原糖与氮化合物的α–氨基酸进行所谓的美拉德反应(Maillard Reaction)[3-4],致使薯片、薯条表面颜色加深,为不受消费者所欢迎的棕褐色[5]。此外,还发现还原糖含量高的马铃薯易受病原菌的侵染引起环腐病[6]。因此,对马铃薯中糖含量进行测定在实际生活中具有重大意义。
比色法是指淀粉水解成葡萄糖后,在浓硫酸的作用下脱水生成糖醛类化合物,再利用蒽酮或苯酚作显色剂,进行比色测定的方法[7]。以马铃薯淀粉为例,通过单因素及正交实验考察蒽酮比色法测定淀粉中总糖的全过程,并对其测定条件进行优化,以期找到一个准确、快捷、适宜于多个淀粉样品测定的条件。对糖的提取及测定研究较多,但针对于蒽酮比色法测定马铃薯淀粉中可溶性总糖的含量的测定条件研究较少,所以本文将对测定条件进行优化,以得到更好、更精确的测定结果。
1 材料与方法
1.1 材料与仪器
马铃薯淀粉:自制;葡萄糖、无水乙醇、蒽酮、浓硫酸等试剂均为分析纯。
SHB-B95 抽滤机:郑州长城科工贸有限公司;HH-4型数显恒温水浴锅:国华电器有限公司;TU—1810 紫外可见分光光度计:北京普析通用有限责任公司;PL2002 型电子天平:梅特勒-托利多仪器(上海)有限公司。
1.2 方法
1.2.1 标准曲线的制作
将在80 ℃烘箱中烘至恒重的葡萄糖0.1 g,定容至100 mL,取出10 mL,再定容至100 mL,即得0.1 mg/mL的葡萄糖标准液,分别取葡萄糖标准溶液0、0.1、0.2、0.3、0.4、0.6、0.8 mL,蒸馏水定容到1 mL,分别加入蒽酮试剂5 mL,沸水浴中加热10 min 后,在620 nm 波长进行测定。以吸光度值为纵坐标,各标准液浓度(μg/mL)为横坐标,作图得标准曲线。葡萄糖标准液的测定量在10 μg/mL~80 μg/mL 的浓度范围内有良好的线性关系,其回归方程为:A=0.009 6C-0.013 9,相关系数为R2=0.999 5。
1.2.2 马铃薯淀粉可溶性总糖的提取及测定
准确称取0.1 g 马铃薯干粉,再加入50 mL 质量分数为80%的乙醇,45 ℃恒温水浴中加热10 min,抽滤后,取滤液1 mL,同时以蒸馏水做空白对照,冰水浴中冷却后备用。按1.2.1 的方法测定马铃薯淀粉中可溶性总糖含量,计算公式如下:
总糖量(以葡萄糖计)=ρ×稀释倍数×10-4(%)
随着信息技术的快速发展,“互联网+”已经渗透到社会生活的各个方面,“互联网+教育”已经成为当前教育发展的新模式。这种新模式既改变了传统的教与学的过程以及教师的主体地位,也改变了高校的教育管理与决策。在此背景下,教师面临着新的课题和挑战:信息技术、大数据、微课、慕课、云技术的出现等,大有颠覆传统课堂、迎来课堂教学革命的势头。因此,作为高校教师,必须在教学方式和方法上与时俱进,不断更新自己的专业知识和能力,否则就会被时代所淘汰。
式中:ρ 为从标准曲线查得的糖浓度,(μg/mL);10-4为将μg/mL 换算为%的系数。
1.2.3 蒽酮比色法测定马铃薯淀粉中可溶性总糖的条件确定
通过对测定马铃薯淀粉中可溶性总糖的条件中反应时间、反应温度、反应后静置时间、显色剂用量等影响马铃薯淀粉中总糖的含量进行单因素试验,并在单因素的基础上进行正交试验,确定最佳的测定条件。
2 结果与分析
2.1 单因素试验结果与分析
2.1.1 反应时间的确定
分别取样液1 mL 于5 支试管,同时另取一支试管,向其中加入1 mL 蒸馏水作为空白对照管,分别加入5 mL 蒽酮试剂,100 ℃水浴中反应5、8、10、12、15 min,取出冷却,室温静置10 min,测吸光度值。测定结果见图1。
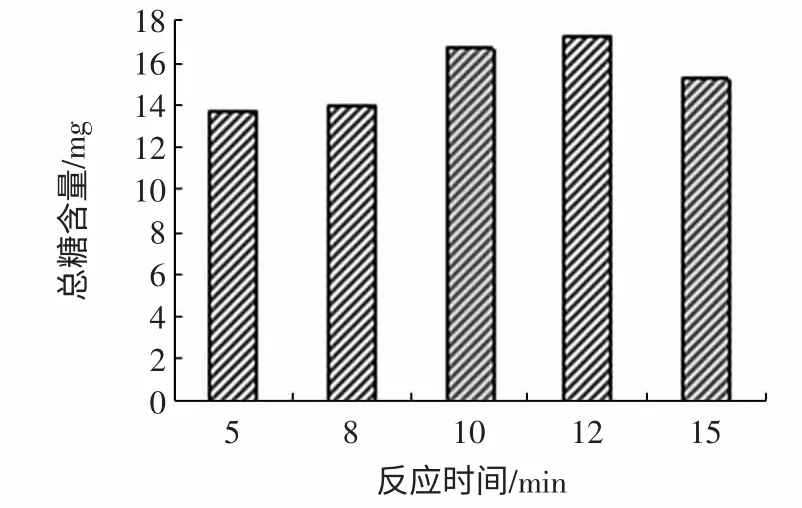
图1 反应时间对马铃薯中可溶性总糖含量的影响Fig.1 Influence of reaction time to soluble total sugar
由图1 可知,不同反应时间对马铃薯淀粉中可溶性糖的提取量不同,随着反应时间的增加,马铃薯淀粉溶液中可溶性糖的提取量先增加后逐渐减少,当反应时间为12 min 时,样液的吸光度值最大,所以最佳反应时间确定为12 min。
取样液1 mL,加蒽酮试剂5 mL,水浴加热时间为12 min,分别于80、85、90、95、100 ℃的水浴中加热。其他步骤同上,测不同温度下各管的吸光度值。测定结果见图2。
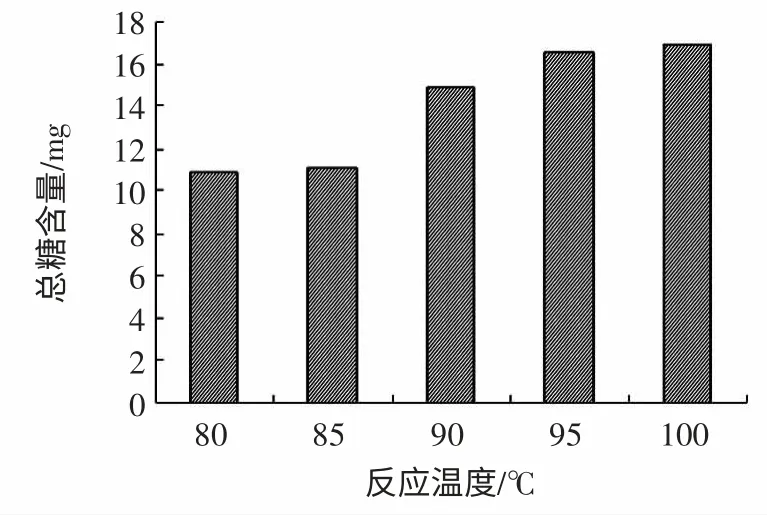
图2 反应温度对马铃薯中可溶性糖含量的影响Fig.2 Influence of reaction temperature to soluble total sugar
由图2 可知,不同反应温度对马铃薯淀粉中可溶性糖的提取量不同,随着提取温度的增加,马铃薯淀粉溶液中可溶性糖的提取量有逐渐增加的趋势,95 ℃和100 ℃时,可溶性糖含量几乎接近。反应温度为95 ℃时,样液的吸光度值最大,所以最佳反应温度确定为95 ℃。
2.1.3 反应后静置时间确定
取样液1 mL,加蒽酮试剂5 mL,水浴温度95 ℃、反应时间12 min,加热后分别静置10、15、20、25、30 min。其他步骤同上,测得不同反应静置时间下各管的吸光度值。测定结果见图3。
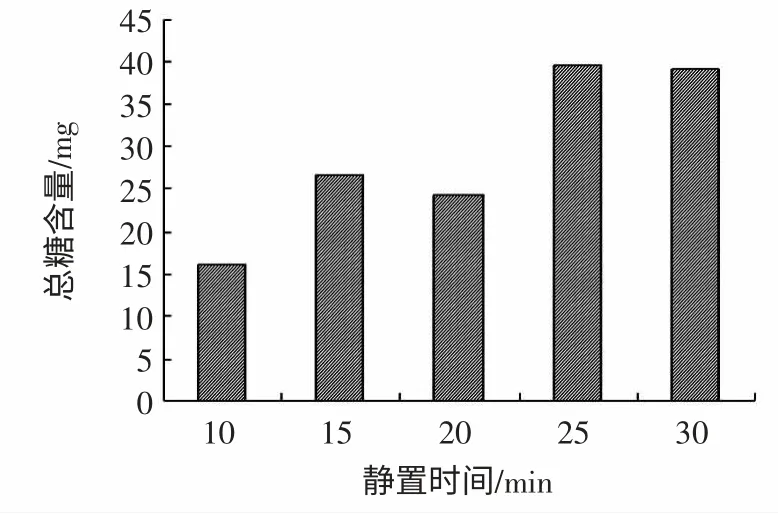
图3 静置时间对马铃薯中可溶性糖含量的影响Fig.3 Influence of setting time to soluble total sugar
由图3 可知,不同静置时间对马铃薯淀粉中可溶性糖的提取量不同,随着静置时间的增加,马铃薯淀粉溶液中可溶性糖的提取量逐渐增加,当静置时间为25 min 时,样液的吸光度值最大,所以最佳静置时间确定为25 min。
2.1.4 显色剂用量确定
取样液1 mL,各管中分别加入蒽酮3、5、7、9、11 mL。其他反应条件均为上述确定最佳条件,步骤同上,测得不同显色剂用量下各管的吸光度值。测定结果见图4。
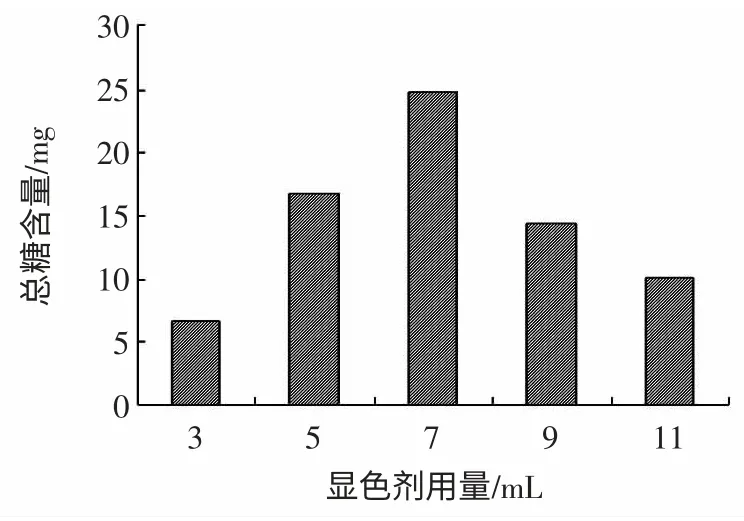
图4 显色剂用量对马铃薯中可溶性糖含量的影响Fig.4 Influence of color reagent dosage to soluble total sugar
由图4 可知,不同显色剂用量对马铃薯淀粉中可溶性糖的提取显色效果不同,随着显色剂用量的增加,马铃薯淀粉溶液中可溶性糖的提取量先增加后减小,当显色剂的用量为7 mL 时,样液的吸光度值最大,所以最佳的显色剂用量确定为7 mL。
2.2 马铃薯淀粉中可溶性总糖测定的条件的优化
在单因素试验的基础上,根据正交试验设计原理,结合单因素试验结果,以反应静置时间(A)、显色剂用量(B)、反应时间(C)、反应温度(D)为变量因素,综合考虑各因素对总糖含量的影响,每个因素设置三个水平进行试验,结果见表1。正交试验方差分析的结果见表2。
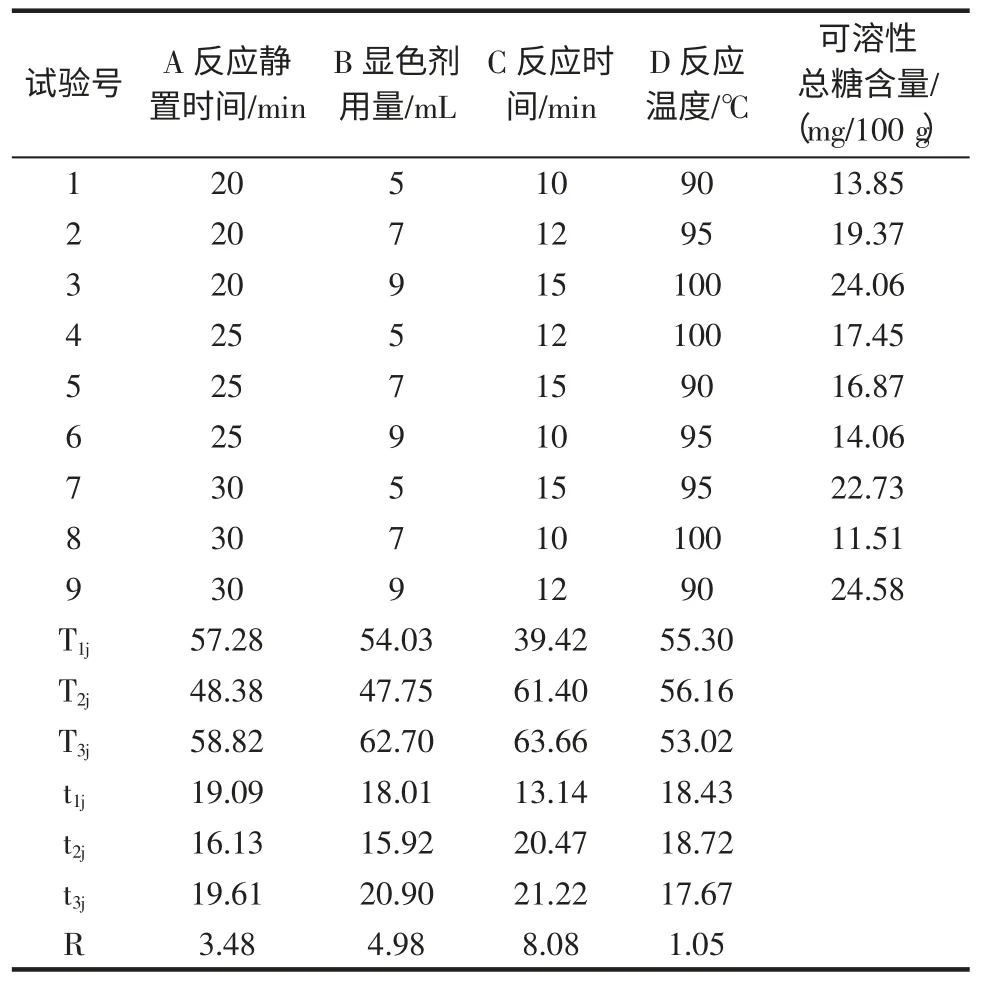
表1 正交试验表L9(34)Table 1 Table of orthogonal experiment
由表1 可知,各因素的主次顺序为:C>B>A>D,最优组合为:C3B3A3D2。正交试验确定蒽酮比色法测马铃薯淀粉中可溶性糖的最佳条件为:反应时间为15 min,显色剂用量9 mL,反应静置时间30 min,反应温度为95 ℃。由于正交试验最优组合C3B3A3D2未在正交试验各组合中,因此,在优化的最佳测定条件下,对所优化的试验条件进行验证,结果得可溶性总糖含量为23.01 mg/100 g。验证实验结果低于正交试验号为3 和9 的试验结果,可能由于蒽酮试剂在测定过程中不稳定,且蒽酮比色法测定总糖含量的几个测定条件都是范围值,之间是有联系的,不能随意改变其中任何一个,否则将影响分析结果[8]。
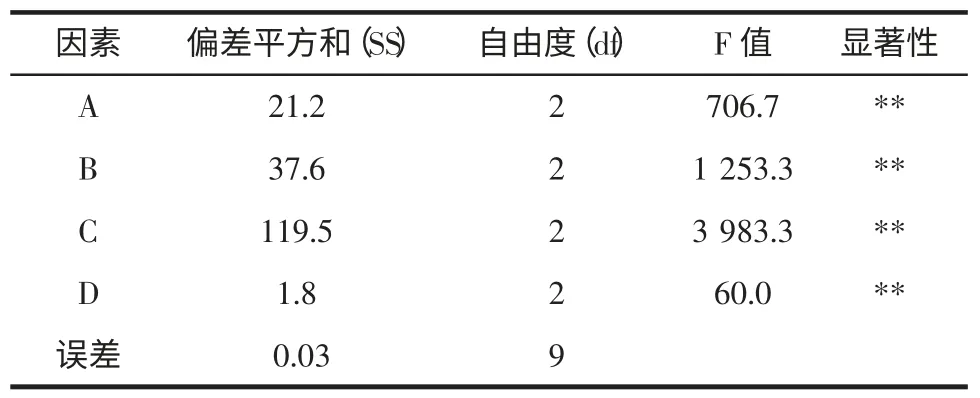
表2 正交实验结果方差分析表Table 2 The analysis of variance of orthogonal experiment
由表2 可以看出,影响马铃薯淀粉中总糖测定结果的因素主次顺序为C>B>A>D,且四个因素对马铃薯淀粉中总糖测定的结果都有极显著的影响。
3 结论
蒽酮比色法测定马铃薯淀粉中可溶性糖的直观分析结果为:反应时间的极差最大,其次分别为显色剂用量,反应静置时间,反应温度,各因素的主次顺序为C>B>A>D。最佳组合为C3B3A3D2,即最佳测定条件为:反应时间为15 min,显色剂用量9 mL,反应静置时间30 min,反应温度为95 ℃。在最佳测定条件下,马铃薯淀粉中可溶性总糖的含量为23.01 mg/100 g。
[1]常志敏.马铃薯资源开发与利用[J].安徽农学通报,2007,13(7):146-147
[2]张水华.食品分析[M].北京:中国轻工业出版社,2007:136
[3]王延平,赵谋明,彭志英,等.美拉德反应产物抗氧化性能研究进展[J].食品与发酵工业,1998(1):70-73
[4]STEFICA HORVAT,MAJA ROSC,JAROSLAV HORVAT.Synthesis of hexose related imidazolidinones:Novel glycation products in the Maillard reaction[J].Springer Netherlands,1999(6):391-398
[5]谢开云,屈冬玉,金黎平,等.我国炸片用马铃薯原料生产中存在的问题与对策[J].中国马铃薯,2001(6):355-357
[6]李寿文,李玉芳.对马铃薯薯块中还原糖测定方法的改进[J].甘肃农业科技,1996(9):16-17
[7]丛松峰.生物化学实验[M].上海:上海交通大学出版社,2005:91-93
[8]王永华.食品分析[M].北京:中国轻工业出版社,2011:75
