微电子工业用超细铜粉的制备和研究
2013-06-08刘显杰徐磊李代颖程耿
刘显杰,徐磊,李代颖,程耿
(武汉船用电力推进装置研究所,武汉430064)
0 引言
在微电子工业中,诸如电容器、电阻器、敏感元件等电子元器件的电极多以金、银等贵金属为材料。用银浆制作陶瓷电子元器件电极具有工艺简单和性能优良而被广泛应用,但陶瓷介质的优良性能常因银离子迁移而被破坏并导致电子元器件失效。在引线焊接时又会因银电极易被锡熔蚀而使电极存在潜在缺陷,为了克服银电极的这些弱点,人们曾作过不少努力,比如,在银浆中掺入比银更昂贵的钯、铂、金等。近年来,贵金属的价格随着世界政治经济形势的波动而暴涨,因此无论从技术方面还是经济角度考虑,用贱金属代替贵金属来制作电极已成为人们努力的目标。
在贱金属中,铜是主要研究对象,它不仅在性能上匹敌于贵金属,而且价格比贵金属低,是一种理想的电极材料。而且铜电极与银电极相比有以下优点: 1) 没有银离子迁移,因此可以用来制造覆盖面积大的电极;2) 耐湿特性优越;3)耐焊性优良;4)价格低廉,可确保供给。作为制备铜浆的主要原料——超细铜粉的研制也因此倍受关注,因为没有优良的金属粉末就没有优良的电子浆料,同时也无法生产高质量的电子产品。
超细铜粉的性能主要取决予其形貌、粒径及制备工艺[1-2]。本文通过研究葡萄糖预还原成Cu2O,水合肼两步法工艺[3-4],用葡萄糖作还原剂延长Cu2O中间体的生长过程,从而以Cu2O颗粒的大小和分布来影响铜粉,制备出的超细铜粉,扫描电镜下粒径为1 μm左右,比表面积为2.42 m2/g,振实密度为2.5 g/cm3。
1 实验
1.1 主要试剂和仪器
主要试剂:五水硫酸铜、葡萄糖、氢氧化钠、水合肼、聚乙烯吡咯烷酮(PVP)和乙醇均为分析纯。主要仪器:扫描电镜(日本电子株式会社,JSM一5610LV);X射线衍射仪(荷兰Panalytical公司);粒度分析测试仪(英国马尔文MASTERSIZE 2000);超级恒温水浴锅(LB801型);粉体综合特性测试仪(丹东百特公司,BT-1000型);静态氮吸附仪(北京精微高博公司,JW-RB型)。
1.2 实验步骤
将500 mL 0.5 mol/L CuS04溶液缓慢滴入350 mL 1.0 mol/L NaOH溶液中均匀混合,15 min后加入300 mL 0.5 mol/L葡萄糖溶液,搅拌30 min,30℃下保温15 min,然后快速升温至70℃,同时快速搅拌,反应0.5 h后可制得Cu2O。将制得的Cu2O离心清洗,直至上层为清液,将Cu2O转入2 L烧杯,加去离子水至1.5 L,水浴加热至40℃,然后滴加占添加总量20%的水合肼,滴完后快速升温至70℃,再次滴加总量80%的水合肼,大约1 h后反应结束,可制得超细铜粉。将制得的铜粉用去离子水离心洗涤3次,然后用无水乙醇离心洗涤2次,最后在真空干燥箱中常温干燥2h,得到干燥的超细铜粉。
2 结果与讨论
2.1 葡萄糖预还原Cu2O
在反应体系温度较低时,当硫酸铜与NaOH反应生成Cu(OH)2后立即加入葡萄糖,此时溶液非常粘稠,物质扩散阻力很大,葡萄糖还原Cu(OH)2生成的Cu2O主要通过聚集的方式形成Cu2O粒子,反应式如下:
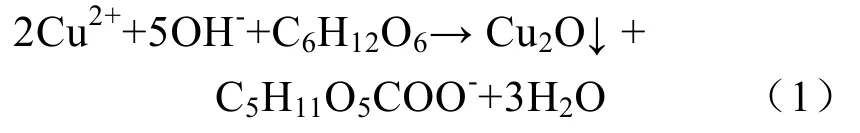
在反应温度较高的情况下,CuSO4与NaOH反应生成的Cu(OH)2在碱性环境中很快脱水成CuO,溶液黏度大大降低,加入葡萄糖后,葡萄糖还原CuO生成的Cu2O主要通过扩散的方式形成Cu2O粒子,这时整个体系中有可能存在没有参加反应的CuO,体系中发生的反应为:


按照预定实验步骤进行操作,通过对最后产物进行XRD测试,对比标准图谱,确定反应产物为纯Cu2O,如图1所示:

2.2 水合肼还原超细铜粉
粉体粒度及粒度分布控制理论很多,其中水合肼两步法制备超细铜粉可参考Weimarm法则[5]。该法则可用于对粒度大小和分布进行控制和预测。它认为沉淀时新相的生成包括成核与长大两个过程。这两个过程的相对速率将决定所得沉淀的粒子大小,其中,晶核形成速率u1为:

晶体长大速率u2为:
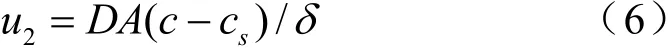
式中:u1是成核速率;K是成核速率常数;c是溶质在溶液中的实际浓度;cs是溶质溶解度;u2是晶核生长速率;D是扩散系数;A是晶核生长常数;δ是固液界面扩散层的厚度。
因此,当溶质体系中存在一定量的沉淀物质,u1>u2时,此时形成大量晶核,可得到高分散的胶体;反之,当u1<u2时,形成的晶核少,而颗粒生长迅速,易形成大颗粒沉淀。由式(5),(6)还知,晶核的形成与生长速率均以溶液的过饱和度(c-cs)为推动力。
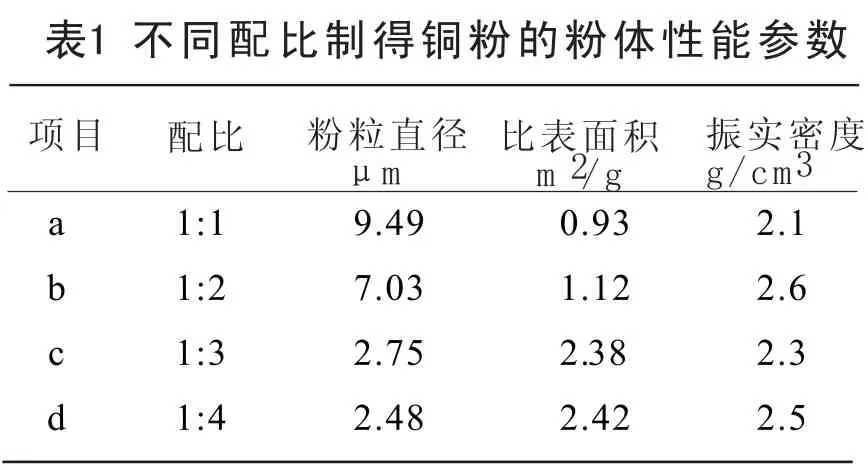
我们通过固定加入水合肼的总用量,改变第一步与第二步加入水合肼的配比,分别选取4个配比为1∶1、1∶2、1∶3、1∶4 ,制得铜粉后测得粒径分布如图2所,当水合肼加入比例为1:4的时候,铜粉整体粒径较细,D(50)为2.48 μm,随着第一步加入量的增加,粒径也增加,当比例为1:1的时候,粒径达到最粗,D(50)为9.49 μm。不同配比下制得铜粉性能如表1所示。
结合Weimarm理论,在实际应用时可以估计所形成的颗粒大小,并有助于选择形成颗粒的适宜条件。但是这个理论是不够成熟,实际上晶核的生长还与溶液中的杂质、介质的黏度、温度、搅拌强度、粒子与粒子之间的聚结作用及各种粒子不同性质等因素有关。因此,我们研究了不同反应温度下,铜粉的粒径分布,如图3所示(图中A—50℃; B—70℃; C—90℃)。

当反应温度为50℃时,反应持续2 h才结束,反应温度为70℃和90℃时候,反应时间为1 h。由于温度较低,反应活性不够,晶核形成速度过慢,颗粒长大无法控制,因此反应时间加长,粒径变大。温度太高,体系反应活性较高,晶核形成后迅速长大 ,形成铜粉颗粒较大。
如图4所示,为水合肼比例1∶4,反应温度70℃时,铜粉的SEM图像。由图可看出,颗粒近球形,粉体粒径<1 μm,存在部分团聚,小于激光粒度仪测试的粒径大小。
?
激光法粒度分析的理论模型是建立在颗粒为球形、单分散条件上的,而实际上被测颗粒多为不规则形状并呈多分散性。因此,颗粒的形状、粒径分布特点以及颗粒的分散条件对最终粒度分析结果影响较大,而且颗粒形状越不规则,粒径分布越宽,分析结果的误差就越大。
2.3 铜粉的抗氧化处理
超细铜粉的化学性质强,在空气中极易氧化,表面形成氧化亚铜,失去优良的性能。目前报道的超细铜粉的抗氧化技术主要有:铜粉表面镀银[6-7]、浆料中加还原剂保护、铜粉的有机磷化合物处理[8]、聚合物稀溶液处理、偶联剂改性[9]、存放在惰性气体或有机溶剂中等[10]。本实验采用苯并三氮唑[11]浸泡烘干,然后抽真空保存超细铜粉,可长时间保存,不发生表面氧化。

3 结论
国外市购铜粉平均粒径为1.069 μm;比表面积为0.64 m2/g;振实密度达3.89 g/cm3,分散性良好[12]。本实验制备铜粉性能与国外还有一定差距,因此,两步法制备超细铜粉工艺仍需进一步优化,其中氧化亚铜的制备是关键。目前我国超细铜粉产业发展较快,但是还存在着在工业化之前必须解决的问题及制备方法进一步开发的问题,并需要对超细铜粉的性能及应用作更深入的研究。铜浆在大功率散热电路板、电子制冷、陶瓷电容器端电极浆料领域中具有较大技术优势。作为制备铜浆的主要原料的超细铜粉的研制也倍受关注。因为没有优良的金属粉末就没有优良的电子浆料,同时也无法生产高质量的电子产品。相信在技术发展和市场需求的刺激下,超细铜粉的生产及应用将具有广阔的市场前景。
[1] 胡敏艺,周康根,陈瑞英等.超细氧化亚铜粉体的制备与应用. 中国粉体技术,2006,1(1):44-48.
[2] 黄锡文,葛庆仁,谢振风. 超细铜粉制备过程中的粒度行为研究.化学反应工程与工艺,1996,12(4):419-421.
[3] 王晓霞,叶红齐,苏周等. 超细铜粉的制备与应用.材料导报,2004,18(3):140.
[4] khtar M. Characterization of copper pastes for end termination application of base metal electrode MLCCs.Microelectronics International, 2004:36-40.
