胃神经鞘瘤的多层螺旋CT诊断
2013-04-18娄毅钱海峰应碧伟
娄毅 钱海峰 应碧伟
胃神经鞘瘤的多层螺旋CT诊断
娄毅 钱海峰 应碧伟
神经鞘瘤又称施万细胞瘤,可发生于任何有施万细胞的神经,尤其好发于外周大的神经,如脊髓、脑和颈部等,而发生于消化道的少见[1],胃神经鞘瘤更少见。文献报道,胃神经鞘瘤占整个神经鞘瘤的0.2%,占胃神经源性肿瘤的78.0%~82.4%,多为良性,恶性较为罕见[2-3]。现对宁海县第一医院及湖州市中心医院收治的5例胃神经鞘瘤的多层螺旋CT特征作一回顾性分析,旨在提高其术前诊断率,报道如下。
1 资料和方法
1.1 一般资料 2005—2010年两院共收治胃神经鞘瘤患者5例,男1例,女4例,年龄38~60岁,平均43.1岁。所有患者均经手术及病理证实。主要临床症状:上腹疼痛1例,腹部肿块2例,呕血、黑便1例,腹胀及消化道梗阻1例。病变部位:中胃底1例,胃体小弯侧2例,胃体大弯侧2例。肿瘤最大径1.5~10cm,平均5.2cm。3例肿瘤向腔外生长,1例向腔内生长,1例向腔内外生长。
1.2 方法 采用16排东芝Aquilion CT机,常规取仰卧位,扫描区域视病情而定。扫描螺距为0.935,轴位扫描层厚为0.5cm。先常规平扫,再以速率3ml/s高压注射非离子型对比剂80~100ml,进行双期或三期团注增强扫描,通过工作站后处理软件进行分析诊断。
2 结果
5例胃神经鞘瘤均为单发,病理证实为良性,肿瘤与邻近组织间分界清晰,胃壁完整,无明显侵蚀。4例CT平扫示肿瘤为均质实体肿块,位于肌壁黏膜下,呈圆形或类圆形,边缘光滑锐利(图1);1例肿瘤形态不规则,呈浅分叶,内部可见小片坏死及囊变征象,但与邻近脏器分界仍清晰(图2)。均未见明确出血及钙化征象。其中1例可见肿瘤与胃黏膜接触面有浅小溃疡形成。增强扫描示4例实质肿块中2例呈轻度强化、2例呈中度强化,另1例实性部分呈中度强化,坏死囊变区无强化;肿瘤实性部分动脉期、静脉期及平衡期均为轻度至中度强化,增强模式表现为持续平稳强化(即动脉期与平扫CT值之差、门脉期与动脉期CT值之差、平衡期与门脉期CT值之差相近)。1例胃周见小淋巴结,呈轻度强化,病理证实为炎性反应增生。均未见腹部实质脏器转移及腹水征象。
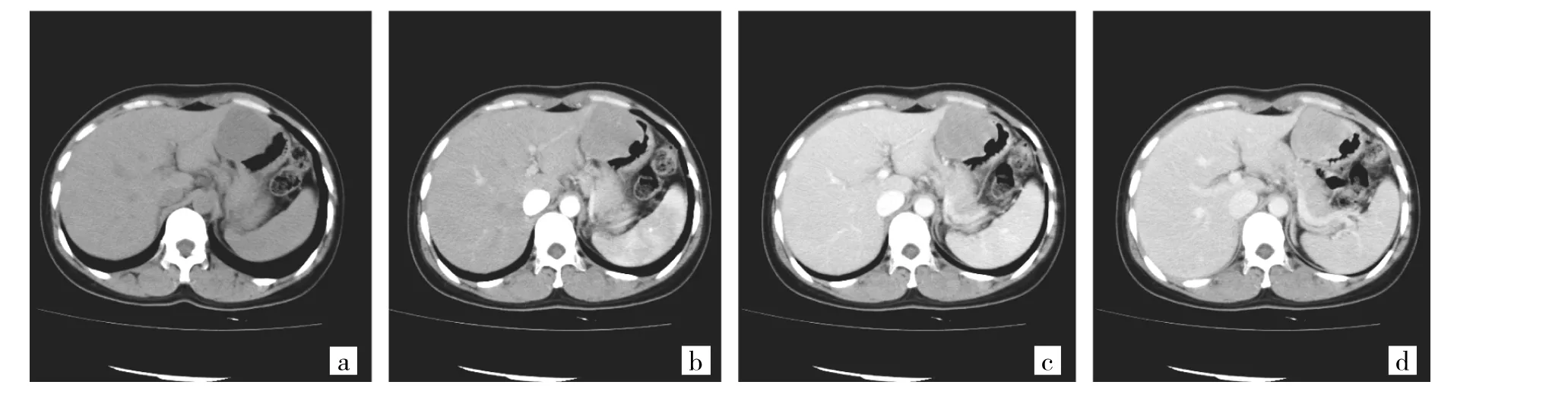
图1 胃体部小弯侧神经鞘瘤CT检查情况(a:CT平扫,病灶位于胃体部小弯侧黏膜下,形态规则,内部密度均匀,边界清,大小约5.6cm×5.4cm;b:CT增强动脉期,CT值约56Hu;c:静脉期,CT值约68Hu;d:平衡期,CT值约79Hu,病灶呈轻度平稳强化)
3 讨论
Palmer等[4]认为,胃神经鞘瘤位于胃体者最多(57.8%),其次为胃窦(24.2%)、胃底(11.7%)、幽门及贲门(3.1%),小弯多于大弯,前壁多于后壁。本组5例中肿瘤位于胃体4例,位于胃底1例,其中小弯侧2例,大弯侧2例。胃神经鞘瘤好发于30~50岁,本组患者平均年龄43.1岁。
神经鞘瘤病理上分为Antoni A型和Antoni B型两种类型,前者有许多鞘细胞,常有栅状核,CT表现为密度稍高,近于软组织密度;后者为鞘细胞稀少,含有丰富的细胞内及细胞外基质,有高脂质或黏液变性,含黏多糖,CT表现上呈囊状低密度区[3-4]。两种类型可在瘤体内随机分布,可夹有胶原、出血、囊变、钙化等改变。消化道神经鞘瘤均发生于消化道的固有肌层,无真正包膜,多呈梭形细胞形态,也可呈上皮样,甚至呈丛状神经鞘瘤形态[5]。消化道神经鞘瘤与外周神经神经鞘瘤形态学上存在差异[6],消化道神经鞘瘤无包膜,肿瘤外周见有淋巴细胞套包绕并可伴生发中心形成。
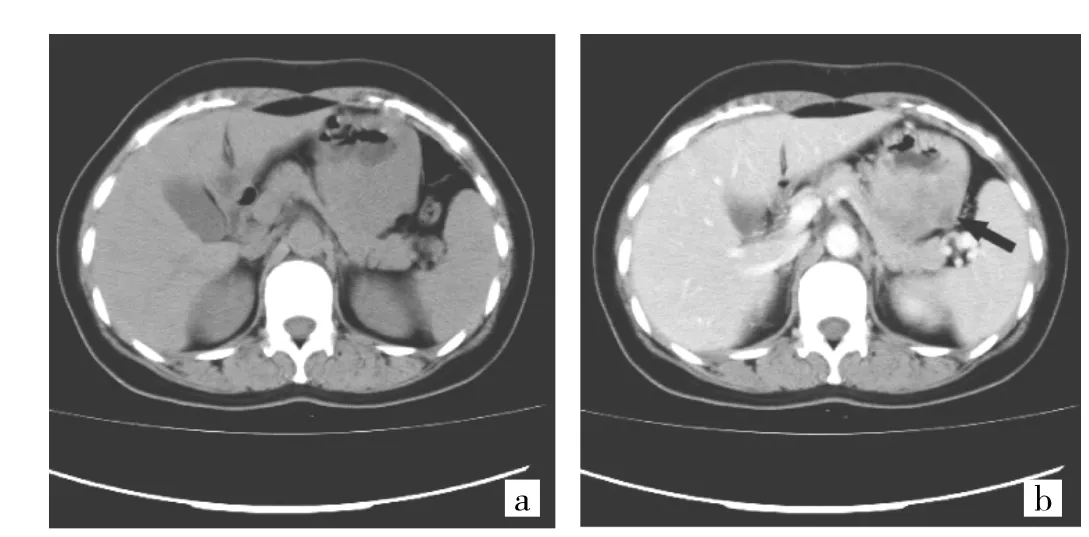
图2 胃体部大弯侧神经鞘瘤检查情况[a:CT平扫,病灶位于胃体部大弯侧黏膜下,密度较均匀,可见分叶;b:静脉期,病灶轻度强化且不均匀,肿瘤外侧部可见小片低强化区(黑箭头所示)]
胃神经鞘瘤肿块CT平扫表现为单发的圆形或类圆形软组织块影,边界清晰、锐利,内部密度多均匀,若肿瘤发生坏死液化,含脂肪或钙化时,密度则不均匀;增强扫描肿瘤实性部分轻度至中度强化,CT值提高范围21~39Hu,包膜强化,坏死囊变部分无强化,肿瘤实性部分动脉期、静脉期及平衡期均为轻度至中度强化,增强模式表现为持续平稳强化。这是由于Antoni A区为形成肿瘤强化的病理基础,而发生囊变,黄瘤变及陈旧性出血的Antoni B区是形成无强化的病理基础。本组中2例增强扫描显示轻度强化,3例增强扫描显示瘤体密度均匀,有中度持续平稳强化表现,其中1例肿瘤中心伴有小片低密度坏死区,无强化,术前CT误诊为恶性间质瘤,可能与未注意轻度强化,且持续平稳强化,且未注意肿瘤与邻近脏器分界清晰有关。
胃恶性神经鞘瘤罕见,除非有远处转移,否则CT鉴别良、恶性较为困难,需依靠病理诊断。若肿块较大(直径>5cm),形状不规则,与周围组织界限不清,呈不均匀强化或短期内病灶迅速增大,均提示恶性或恶性变可能。鉴别诊断:(1)胃平滑肌源性肿瘤:好发生于胃体部近胃底区,一般直径约3~5cm,多呈圆形或类圆形,密度多较均匀,多与肌肉呈等密度,囊变少见,多呈中度至明显均匀强化。有学者认为,如肿块内部见到明显钙化,则应考虑胃神经鞘瘤[7]。(2)胃间质瘤:间质瘤病灶大,易向腔外生长,肿瘤具富血供,易囊变或坏死区,动脉期、静脉期均强化明显,强化程度比神经鞘瘤明显,增强模式为动脉期比静脉期强化明显;部分患者经3D-CTA检查可找到肿瘤供血血管。
传统消化道钡餐造影可显示病变,以及黏膜面及溃疡、瘘道等,是胃肠道肿瘤的首选影像检查方法[2],但钡餐造影对胃壁增厚,腔外病变,特别是有无淋巴结肿大不能显示。随着CT扫描速度的提高,患者一次屏气即可完成全部检查,可减少胃肠道蠕动伪影,MSCT不仅能清楚显示病变部位、范围、大小、界面,也有利于观察病灶内部有无囊变、钙化等,以及显示对邻近脏器的压迫和侵犯情况。对浆膜下向腔外凸出的肿瘤更具有诊断价值,弥补了钡餐及胃镜检查的不足。CT在显示肿瘤钙化方面明显较X线平片及MRI敏感,同时可发现胃窦部肿瘤造成梗阻等重要并发症以及对实质性脏器的转移等,还可在工作站进行图像后处理寻找肿瘤的供血血管,为临床治疗提供诊治依据。
综上所述,MSCT扫描能准确评价胃神经鞘瘤的病变部位、大小、形态、生长方式、强化程度及增强模式、与邻近结构的关系等,有助于病变的定位、鉴别诊断及术前评估,但部分患者单纯以影像学诊断尚有一定困难,仍需病理检查确诊。
[1]李其纲,王跃生,徐荣楠.胃神经鞘瘤[J].安徽医学,1992,13(1):33-35.
[2]刘振疆,陈鹏,马斌林.胃神经鞘瘤的诊断与治疗(附2例报告)[J].实用癌症杂志,1996,11(1):36-37.
[3]Genova G,Maiorana A M,Agnella G,et al.Gastric schwannoma after nissen fundoplication:a rare complication[J]?Am Surg,1989,55(8):495-498.
[4]王伟,肖旭波,姚永强,等.胃神经鞘瘤的病理学及临床诊治分析[J].中国厂矿医学,2003,16(2):95-96.
[5]Miettinen M,Shekitka K M,Sobin L H.Schwannnomas in the colon and rectum:a clinicopathologic and immunohistochemical study of 20 cases[J].Am J Surg Pathol,2001,25:846-855.
[6]成元华,杨光华,郭立新.消化道神经鞘瘤的临床病理分析[J].中华病理学杂志,2003,31(5):442-443.
[7]李恩美,杨振燕,陈克敏.CT对胃部不同病变诊断的价值[J].实用放射学杂志,2001,17(10):780-782.
[8]Beggs I.Pictorial review:imaging of peripheral nerve tumors[J]. Clinical Radiology,1996,52(1):8-12.
2012-06-02)
(本文编辑:欧阳卿)
315600 宁海县第一医院放射科(娄毅、应碧伟);湖州市中心医院放射科(钱海峰)
