气相色谱-质谱法测定腌渍蔬菜中的丙酸及其应用
2013-01-30郝鹏飞刘东风牟志春徐琴苏广坤刘琳
郝鹏飞,刘东风,牟志春,徐琴,苏广坤,刘琳
(1.山东出入境检验检疫局食品农产品检测中心,山东青岛266002;2.海军工程大学青岛油液检测分析中心,山东青岛266012)
丙酸及其钠盐、钙盐是国家批准使用的人工合成防腐剂,但是其添加必须在规定范围内按规定限量使用,而且添加之后必须在食品标签上注明[1]。近年来出口腌渍蔬菜中被通报检出丙酸。而依据我国强制性国家标准GB 2760-2011 的规定,丙酸用于醋和糕点中的最大使用量为2.5 g/kg,不允许用于腌渍蔬菜中。因此对腌渍蔬菜中丙酸的快速准确检测方法的研究十分必要。测定丙酸的检测方法有气相色谱法[2-7]、高效液相色谱法[8-9]、离子色谱法[10]。但方法大多采用水蒸气蒸馏,操作起来相当繁琐,检测周期较长。并且气相色谱法采用氢火焰离子化检测器检测,只要保留时间一致即判定为检出,因而在定性方面存在误判的可能。本方法是样品经过酸化后用乙醇提取,用气相色谱-质谱分析,根据质谱给出的离子丰度,与标准谱库比对定性,同时结合保留时间达到双重定性的目的,可对腌渍蔬菜中的丙酸及其钠盐、钙盐实现快速和准确的测定。
1 材料与方法
1.1 仪器与试剂
气相色谱-气质联用仪,Agilent 7890A-5975C(美国安捷伦公司);INNOWAX 石英毛细管柱(30m×0.25mm×0.25 μm);电子分析天平(SartoriusBS423S);涡漩振荡器(IKA MSI Minishaker);有机相过滤膜(0.45 μm);无水乙醇(色谱纯);磷酸溶液(10%):量取10 mL 磷酸于100 mL 容量瓶,加水稀释定容;标准溶液(1.0 mg/mL):准确称取丙酸标准物质0.100 0 g 于100 mL 容量瓶,用无水乙醇定容至刻度;标准使用溶液(10.0 μg/mL):取上述标准溶液1.0 mL 置于100 mL 容量瓶中,加无水乙醇定容至刻度。
1.2 样品处理
称取样品5.0 g 于50 mL 离心管中,加入1.0 mL磷酸溶液(10%),盖好塞子,上涡旋振荡仪涡旋2 min。加入20 mL 无水乙醇,涡旋振荡提取2 min 后,4 000 r/s离心5 min,移取上清液,残渣再加入20 mL 无水乙醇重复提取一次,合并两次提取液,用无水乙醇准确定容到50 mL,混匀,经0.45 μm 有机滤膜过滤入进样小瓶中,供GC-MS 测定用。
1.3 气相色谱—质谱条件
气相条件:色谱柱为石英毛细管色谱柱(HPINNOWAX 极性柱)。进样口为200 ℃。载气:高纯氦气(>99.999%)。采用分流模式进样,分流比为10 ∶1。进样量为1.0 μL,流速:1.0 mL/min。程序升温设置为:初始50 ℃,维持2 min,再以10 ℃/min 升温至200 ℃;传输温度为240 ℃。
质谱条件:溶剂延迟:6 min。EI 电离方式,电子能量为70 eV,离子源为230 ℃,四级杆为150 ℃。采用全扫描(SCAN)时,扫描范围为30 amu~200 amu,定性离子为74、57、45,定量离子为74。采用离子监测模式(SIM)时,监测离子选择74、57、45。
2 结果与讨论
2.1 前处理方法的改进
2.1.1 处理方法的改进
国标方法GB/T 5009.120-2003 食品中丙酸钠、丙酸钙的测定[2]采用水蒸气蒸馏法,每个样品前处理时间将近1 h,操作繁琐,费时费力,对大批量样品处理不实用,且最后得到的以水为溶剂的试液对气相色谱的毛细管柱及质谱均有损害。而本方法采用样品经酸化后用有机溶剂提取,多个样品可以同时处理,操作简便、快速、提取效果好,完全能满足样品中丙酸及其钠盐、钙盐含量的测定要求。
2.1.2 酸化试剂的确定
采用磷酸溶液(10%)、盐酸溶液(10%)和硫酸溶液(10%)进行对比处理,回收率结果表明:三种试剂的酸化效果相差不大。考虑磷酸无强氧化性和强腐蚀性,属较为安全的酸,所以确定磷酸溶液(10%)为酸化试剂。
2.1.3 提取试剂的确定
分别采用无水乙醇、丙酮和甲醇作为提取溶液,结果显示甲醇的回收率较低,而无水乙醇和丙酮的回收率都较高,考虑无水乙醇价格便宜,几乎无毒等优点,所以确定无水乙醇为提取溶液。
2.2 色谱柱和程序升温条件的确定
分别采用HP-5 MS 石英毛细管柱和INNOWAX石英毛细管柱进行测定,结果显示INNOWAX 色谱柱中丙酸峰形较好。按照检测灵敏度高,检测时间短,分离效果好的原则,通过对标准溶液进样的观测确定色谱分离和质谱检测条件(1.3)。在此条件下,丙酸标准峰形较好,保留时间为12.170 min,与其他杂质峰得到了有效的分离,其色谱图如图1 所示,质谱图如图2 所示。由质谱图在谱库中检索可定性判断是否为丙酸。

图1 丙酸标准的色谱图Fig.1 Chromatogram of propionic acid

图2 丙酸标准的质谱图Fig.2 MS Chromatogram of propionic acid
2.3 线性关系及检出限
准确吸取丙酸标准使用液(10.0 μg/mL)0、1.0、2.0、4.0、8.0、10.0 mL 至10 mL 容量瓶中,加无水乙醇定容至刻度,混匀,配成0、1.0、2.0、4.0、8.0、10.0 μg/mL的标准溶液,上机测定。以丙酸浓度为横坐标,离子丰度为纵坐标,绘制标准曲线。结果显示线性良好。线性方程及相关系数分别为:Y=8.842×102X-3.782×102;r2=0.999 3。
在研究条件下以浓度为2.0 μg/mL 的标准溶液为测试液,仪器自动测得信噪比S/N,以基线噪声3 倍峰面积对应的质量浓度为检出限(RS/N=3),确定方法的检出限为0.20 mg/kg。
2.4 回收率和精密度
在上述优化条件下,以未检出本底(检测值<0.20mg/kg)的腌渍黄瓜做基质,测定了20.0、40.0、50.0 mg/kg 添加水平时丙酸的回收率,每个添加水平重复测定6 次,计算回收率和相对标准偏差(RSD),结果见表1。回收率为95.8%~97.9%,相对标准偏差为1.2%~2.3%,表明方法准确可靠。
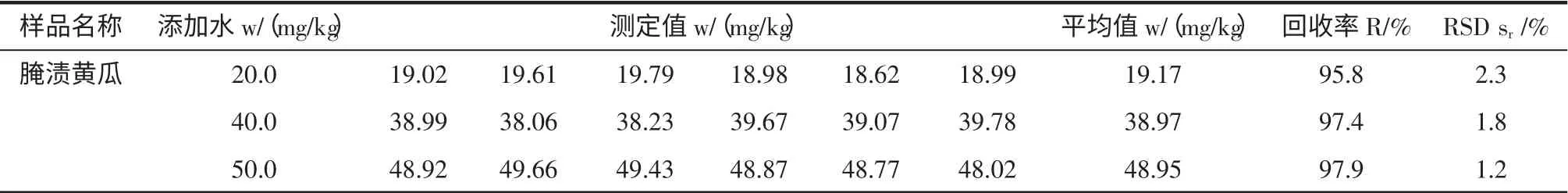
表1 腌渍黄瓜中丙酸的回收率与相对标准偏差(RSD)Table 1 Recoveries and relative standard derivations of propionic acid in pickled cucumber
2.5 方法应用-腌渍蔬菜中丙酸的测定及其引入的原因分析
对出口腌渍蔬菜如泡菜、腌渍蒜、腌渍萝卜、拌苏子叶、腌渍姜片、腌渍蒜苔、腌渍辣椒、调味黄瓜、腌渍牛蒡等产品,采用本文建立的方法进行检测,共371 个样品。如图3 为检出丙酸的腌渍姜片的色谱图。

图3 腌渍姜片的色谱图Fig.3 Chromatogram of pickled ginger
测得的结果表明这些样品均含有丙酸,90%以上的样品在国家标准的检出限20 mg/kg[2]以下,少数样品在20 mg/kg~100 mg/kg 之间。但是其中有3 份样品的丙酸含量分别高达166、314 和505 mg/kg,对这3 份样品所采用的生产原料进行检测,发现其所使用的醋酸中丙酸的含量都很高,分别为2 060、2 110 mg/kg 和3 690mg/kg。因而推测这三份样品中的丙酸是由其所使用的醋酸引入的。根据测试结果建议企业改用其他醋酸,其后生产的腌渍蔬菜中的丙酸含量均降至20mg/kg 以下。
3 结论
建立了测定腌渍蔬菜中丙酸含量的气相色谱-质谱方法,本方法准确、简便、快速,所使用的试剂对实验人员的健康危害小,可同时连续检测大量样品,能满足实际样品的检测及监控的要求。本实验室已完成了大量腌渍蔬菜样品的检测,对腌渍蔬菜中丙酸的含量作了有效的监控。
[1] 中华人民共和国卫生部.GB 2760-2011 食品安全国家标准食品添加剂使用标准[S].北京:中国标准出版社,2011
[2] 中华人民共和国卫生部.GB/T 5009.120-2003 食品中丙酸钠、丙酸钙的测定[S].北京:中国标准出版社,2003
[3] 杨乙强.顶空进样-气相色谱法测定食品中丙酸盐[J].上海计量测试,2010(2):13-15
[4] 龚睿蓉.毛细管气相色谱法测定食品中丙酸钙[J].粮油食品科技,2009,17(5):26-28
[5] 赵娅鸿. 气相色谱法测定食品中的防腐剂丙酸盐含量方法的研究[J].食品工程,2009(2):49-50,56
[6] 袁勇军.毛细管气相色谱法测定食品中的丙酸盐[J].食品科技,2009,34(8):272-274
[7] 张思群,王志元,许毅.自动进样顶空气相色谱法连续测定食品中丙酸盐[J].食品科学,2002,23(11):104-106
[8] 中华人民共和国国家质量监督检验检疫总局.GB /T 23382-2009 食品中丙酸钠、丙酸钙的测定高效液相色谱法[S].北京:中国标准出版社,2009
[9] 姜涛,潘红红,李辉章,等.高效液相色谱法测定防霉剂中丙酸含量的研究[J].粮食储藏,2011,40(5):32-33
[10] 陈玉波,陈长毅,杨芳,等.离子色谱法对食品中丙酸钙的测定[J].安徽农业科学,2010,38(33):19058-19059
