发菜中三苯甲咪唑氨基酸抗氧化和紫外吸收性质的研究
2013-01-30刘荣于海峰
刘荣,于海峰
(1.荣成检验检疫局,山东荣成264300;2.齐鲁工业大学食品与生物工程学院,山东济南250353)
三苯甲咪唑氨基酸(mycosporine-like amino acids,MAAs)是一类水溶性、小分子(<400 Da)、具有紫外吸收特性的化合物[1]。它是以环乙烯酮为基本骨架,与氨态氮或亚氨基醇共轭组成的,由于侧链和取代基的不同,不同结构的三苯甲咪唑氨基酸的波长吸收范围也有所不同[2]。三苯甲咪唑氨基酸在微生物界的分布是非常广泛的,在细菌、真菌、蓝藻、浮游植物和大型藻类中都发现三苯甲咪唑氨基酸的存在[3]。目前前对于三苯甲咪唑氨基酸的研究主要集中于环境因素(紫外辐射强度、温度、盐度等)对藻类积累MAAs 的影响、紫外线对MAAs 的诱导及MAAs 的分布等方面。对这类紫外线吸收物质的应用研究只是刚刚起步,其研究范围和深度都不够。国内对该领域的研究报道很少,本论文以液体悬浮培养的发菜细胞为原料,确定了其含有MAAs,研究了MAAs 化合物的紫外吸收及抗氧化的性质。
1 材料与方法
1.1 实验原料
发菜细胞(Nostoc flagelliforme),由齐鲁工业大学藻类生物技术研究所提供。
1.2 方法
1.2.1 MAAs 粗提物的制备
将发菜与甲醇按1 ∶4(g ∶mL)的比例进行提取,初始pH 为2、温度45 ℃、提取时间2 h。收集上清液,冰箱中放置24 h。过滤,旋蒸(45 ℃、50 r/min),将浓缩物按水∶氯仿的比例为2.5 ∶7.5(体积比)加入氯仿,取上层水溶液离心,冷冻干燥后即得MAAs 粗品[4]。
1.2.2 清除羟基自由基能力的测定
该实验采用H2O2/Fe2+体系。将1 mL 9 mmol FeSO4、1 mL 9 mmol 水杨酸-乙醇与不同浓度的MAAs 溶液混匀,37 ℃水浴30 min,5 000 r/min 离心5 min,加入1 mL 9.8 mmol H2O2启动整个反应。510 nm 下测定添加不同浓度MAAs 溶液的吸光值[5]。清除率的计算公式:
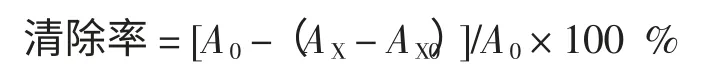
式中:A0为空白参比液的吸光值;AX为加入MAAs 溶液后反应体系的吸光值;AX0为MAAs 溶液的本底吸收值。因待测反应体系本身存在着吸光值,该试验中以1 mL 9 mmol FeSO4、1 mL 9 mmol 水杨酸-乙醇、1 mL MAAs 溶液和1 mL 蒸馏水作为待测溶液的本底吸收值。
1.2.3 清除超氧离子能力的研究
取4.5 mL pH 8.2、浓度50 mmol Tris-HCl 缓冲液,15 μL 蒸馏水,摇匀,25 ℃水浴20 min,分别加入1 mL不同浓度的MAAs 粗品溶液,再加入15 μL 预热过的(25 ℃)邻苯三酚(3 mmol,用10 mmol HCl 配置)。混匀,测定325 nm 下MAAs 溶液的吸光度值[80]。每30 s测定一次数值,以每分钟的样品溶液吸光度增加值来计算MAAs 的清除率。清除率的计算公式:

式中:ΔA0为邻苯三酚的自氧化速率;ΔA 为加入MAAs 溶液后邻苯三酚的自氧化速率。
1.2.4 MAAs 紫外吸收能力的鉴定
称取MAAs 粗提物0.05 g,将其与防晒系数为20的防晒乳霜按质量比1 ∶1、1 ∶2 的比例混合均匀,分别溶入20 mL 水中,于280 nm~400 nm 波长范围内进行光谱扫描,以未添加MAAs 粗提物的防晒乳霜做空白对照[6]。
2 结果与分析
2.1 MAAs 对超氧阴离子清除能力的测定
MAAs 对超氧阴离子的清除效果见图1。
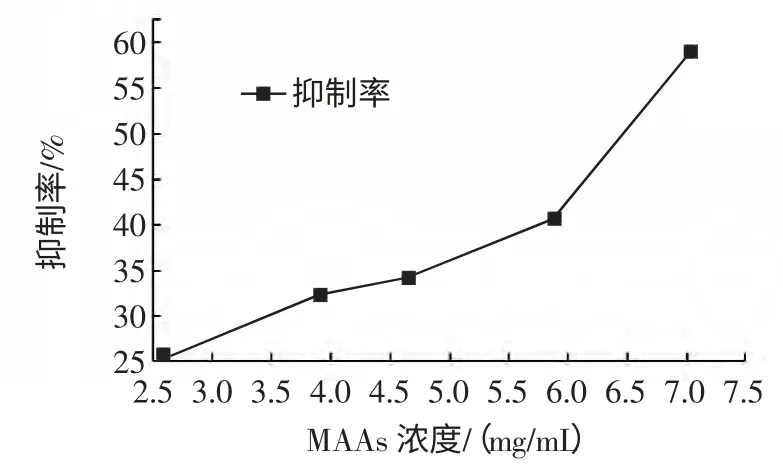
图1 MAAs 清除超氧离子能力的研究Fig.1 The superoxide anion scavenging activity of MAAs
在碱性环境下邻苯三酚能够迅速发生氧化,释放出超氧阴离子,进而生成有色的中间产物。加入抗氧化物质能够使溶液体系颜色变浅,325 nm 处吸光度降低。试验结果表明MAAs 具有清除超氧阴离子的作用。其清除作用随MAAs 浓度的增大而增大,当MAAs 浓度为7.05mg/mL 时,对超氧阴离子的清除率为59.01%。需氧生物体内95%的氧分子可以作为电子受体在物质代谢过程中发挥作用,最终被还原成水,而剩余的5%则在还原过程中由于接受的电子数目不等从而形成了多种性质活泼的活性氧,氧分子受单一电子还原的产物称为超氧阴离子。定量的超氧阴离子对于细胞来说是无害的,但过量即可造成组织损伤。紫外胁迫是一种重要的外源氧化应激因素,超氧阴离子就是细胞受到紫外辐射后的一种产物,并进一步氧化成过氧化氢等其它自由基,对细胞造成伤害[7]。因此,细胞内MAAs 含量的增加是发状念珠藻响应紫外胁迫的一个重要机制,它在短时间内能够有效地保护细胞避免受到过多的伤害。
2.2 MAAs 对羟基自由基清除能力的测定
MAAs 对羟自由基的清除效果见图2。

图2 MAAs 清除羟基自由基能力的测定Fig.2 The hydroxyl radical scavenging activity of MAAs
采用可见光分光光度法在510 nm 处测定MAAs对羟自由基的清除能力。反应体系中,水杨酸能够捕捉Fenton 反应生成的羟自由基生成2,3-二羟基苯甲酸,然后通过分光光度法测定2,3-二羟基苯甲酸的量间接的测定羟自由基的生成量。
由图2 可知,MAAs 具有清除羟自由基的能力,随浓度的增大其清除效果越明显。当浓度为30.78 mg/mL时,清除率可达到78.64%。羟基自由基也是基体受到紫外胁迫后的一种产物,是活性氧中最活泼的自由基,也是活性最大的自由基,几乎可以和细胞中的任何分子发生反应,对蛋白质、核酸、糖类和脂类都有损伤。MAAs 对羟自由基的清除作用进一步表明MAAs的生成能够有效地保护细胞免受紫外的过多胁迫。
2.3 MAAs 抗紫外吸收能力的鉴定
MAAs 的紫外吸收效果见图3。

图3 MAAs 粗提物与防晒霜(SPF20)混合后紫外吸收能力的测定Fig.3 The absorption spectrum of mixture with different amount of MAAs with SPF20
从图3 我们可以看出防晒乳霜及其与MAAs 粗提物混合物在200 nm~400 nm 波长范围内的吸光度。较纯的防晒乳霜添加MAAs 粗提物后的样品组吸光值在所测得波长范围内都有所增加。防晒乳霜吸收紫外的能力主要集中在280 nm~360 nm 处,而添加MAAs粗品后,防晒乳霜的紫外吸收能力在整个波长范围内都有显著的提高。由此可以表明,MAAs 对防晒用品的防晒能力具有促进作用。
3 结论
MAAs 具有一定的抗氧化能力。MAAs 对超氧阴离子和羟自由基的清除作用随浓度的增大而增大,MAAs含量的增加是发菜响应紫外胁迫的一个重要机制,它在短时间内能够有效地保护细胞避免受到过多的伤害。防晒乳霜吸收紫外的能力主要集中在280nm~360nm处,而添加MAAs 粗品后,防晒乳霜的紫外吸收能力在整个波长范围内都有显著的提高,说明MAAs 具有有效的防紫外线能力。在防晒要求日益提高的今天,MAAs 可作为一种较理想的防晒护肤物质。
[1] Jean F B, Noel A. Structure de la mycosporine(P310)[J]. Chem,1976,54:1105-1113
[2] Wu Won J J, Chalker B E, Rideout J A. Two new UV-absorbing compounds from Stylophora pistillata:Sulfate esters of mycosporinelike amino acids[J].Tetrahedron Lett,1997,38(14):2525-2526
[3] 陈小兰,邓国宾,刘开庆,等.水生生物的紫外光防护剂——类菌胞素氨基酸[J].植物学通报,2006,23(1):78-86
[4] 许志恒,张朝辉,李八方,等.紫菜中类菌孢素氨基酸种类的确定及提取条件优化[J].食品工业科技,2011,32(2):187-190
[5] 陈雪峰,李一.发菜多糖清除自由基活性的研究[J].安徽农业科,2008,36(8):3088-3089
[6] 郭婷婷,王春华,关万春,等.坛紫菜甲醇提取物屏蔽紫外能力的研究[J].浙江农业学报,2011,23(3):593-597
[7] Favre B J, Bernillon J, Salin N, et al. Biosynthesis of mycosporines:mycosporine glutaminol in Trichotheciwn rosewn[J].Phytochemistry,1987,26:2509-2514
