肾移植术后依维莫司在免疫抑制治疗中的有效性和安全性评价
2013-01-04毛棉吴斌蒋学华王凌四川大学华西药学院临床药学研究中心四川成都6004四川大学华西医院四川成都6004
毛棉,吴斌,蒋学华,王凌 (.四川大学华西药学院临床药学研究中心,四川 成都6004;.四川大学华西医院,四川 成都6004)
肾移植是终末期肾脏病替代治疗的方式之一,其有效性和费用均优于透析治疗[1]。目前,虽然已有多种免疫抑制剂的联用方案抑制肾移植后的排斥反应,以达到较长的人、肾生存率和提高生活质量,但是各种免疫抑制剂的作用机制和效果不一。如何将降低排斥反应的发生和降低毒副作用、感染、肿瘤的风险达到平衡,一直是移植后免疫治疗所关注的重点。依维莫司是雷帕霉素靶蛋白抑制剂,可以抑制T细胞功能、单核细胞、巨噬细胞的活化,于2011年4月被FDA批准用于预防有轻中度免疫风险的成年肾移植患者可能出现的排斥现象。与钙调磷酸酶抑制剂具有肾毒性不同,依维莫司具有肾脏保护的优势,并且已有证据支持雷帕霉素靶蛋白对肿瘤有靶向治疗作用,可能对免疫抑制剂治疗的患者有降低肿瘤发生的风险[2]。Webster等[3]在2006年发表了雷帕霉素抑制剂对肾移植患者的系统评价,但涉及依维莫司的随机对照试验(RCT)较少,仅有2个RCT评价依维莫司对照霉酚酸酯和少量依维莫司剂量间的对比。本研究将对肾移植术后应用依维莫司在免疫抑制治疗中的安全性与有效性更新系统评价,以期为肾移植术后依维莫司在免疫抑制治疗中的应用提供偱证依据。
1 资料与方法
1.1 纳入和排除标准
1.1.1 研究设计 纳入RCT,语种限定为英文和中文。
1.1.2 研究对象 纳入肾移植受者;排除伴有其他器官移植者、移植前5年有恶性肿瘤史者、移植后胃肠道功能障碍影响药物吸收者、移植后心律失常者、孕妇、儿童。
1.1.3 干预措施 依维莫司+其他药物vs阳性药物+其他药物;
1.1.4 结局指标 有效性指标:急性排斥反应发生率(ARR)、肌酐清除率(Ccr)、患者存活率(PSR)、移植物存活率(GSR);安全性指标:血清胆固醇水平、巨细胞病毒感染、尿路感染、贫血、腹泻、口腔溃疡、糖尿病、高脂血症、肿瘤、外周水肿、淋巴囊肿。
1.2 文献检索与数据提取 计算机检索Cochrane图书馆、SCI、EMBASE、PubMed、CNKI、VIP、CBM 和万方数据库。检索方式采用MeSH加自由词联合搜索,检索时间为建库至2012年1月。同时手工检索重要文献的参考文献和肾移植相关杂志《中华器官移植杂志》、《肾脏病与透析肾移植》、《中华肾脏病》、《临床肾脏病》等。对于同一RCT的不同随访时间报道均纳入。文献筛选及数据提取均由两名研究员独立进行后核对,如有分歧协商解决或由第三名研究员协助解决。
1.3 质量评价与统计分析 由于结局指标均为客观指标,故均不考虑盲法。采用RevMan5.0根据Cochrane Handbook系统评价的标准进行质量评价,包括:随机序列产生是否正确,是否分配隐藏,结果数据是否完整,失访处理是否恰当。若该研究满足所有的质量评价标准,存在偏倚的可能性很小,为A级;若该研究任何一条或多条评价标准仅为部分满足,存在偏倚的可能性为中度,为B级;若任何一条或多条评价标准完全不满足,存在偏倚的可能性很大,为C级。
采用RevMan5.0软件进行 Meta分析。首先对纳入文献进行临床异质性评价,必要时采用亚组分析或者描述性分析。采用Q检验检验统计学异质性,检验水准为α=0.10;经检验无异质性(P>0.10)的研究采用固定效应模型进行合并分析,反之寻找异质性的原因后采用随即效应模型进行合并分析。对分类变量采用危险比(RR)、连续变量采用均数差(MD)并用95%CI表示合并效应量。必要时进行敏感性分析。
2 结果
2.1 检索结果 根据检索策略初检到文献640篇,排除明显不符合的文献594篇,46篇阅读全文后进行筛选,共纳入来自7个RCT共8篇报道[4-11]。共纳入患者1 998名。
2.2 纳入研究的基本情况和方法学质量评价 纳入研究的基本情况见表1。3个研究[4-6]是依维莫司对比CNI,4个研究[7-11]是依维莫司对比吗替麦考酚酯。各研究干预药物的剂量和目标血药浓度见表1。所有研究均采用了随机分配的方法,均报道了试验组和对照组的失访情况,均采用了ITT分析。2个研究[7,11]未详细说明随机分配方法。具体纳入研究的方法学质量评价见表2。
2.3 疗效指标分析结果
2.3.1 急性排斥反应发生率(ARR)
(1)依维莫司 VS CNI:3个研究[4-6]报道了 ARR。各研究间无统计学异质性,故采用固定效应模型进行合并分析。2组差异无统计学意义[RR=1.13,95%CI(0.70,1.82)]。
(2)依维莫司 VS吗替麦考酚酯:4个 RCT[7-11]包括5篇文献报道了ARR。各研究间无统计学异质性,故采用固定效应模型进行合并分析。2组差异无统计学意义[RR=0.92,95%CI(0.75,1.13)]。见图1。
2.3.2 肌酐清除率(Ccr)
(1)依维莫司 VS CNI:1个RCT[6]报道了Ccr。2组差异无统计学意义。

表1 纳入研究的基本特征Tab 1 General information of included studies

表2 纳入研究的质量评价Tab 2 Quality evaluation of included studies
(2)依维莫司VS吗替麦考酚酯:2个RCT的3篇文献[8-10]报道了Ccr。各研究间无统计学异质性,故采用固定效应模型进行分析。2组间差异无统计学意义[MD=-0.62,95%CI(-3.60,2.36)]。见图2。
2.3.3 移植物存活率(GSR)
(1)依维莫司 VS CNI:2个研究[5,6]报道了 GSR。各研究间无统计学异质性,故采用固定效应模型进行合并分析。2组差异无统计学意义[RR=1.01,95%CI(0.99,1.04)]。见图3
(2)依维莫司VS吗替麦考酚酯:4个RCT包括5篇文献[7-11]报道了GSR。各研究间存在统计学异质性,故采用随机效应模型进行合并分析。2组差异无统计学意义[RR=1.01,95%CI(0.96,1.05)]。见图4。
2.3.4 患者存活率(PSR)
(1)依维莫司 VS CNI:3个研究[4-6]报道了 PSR。各研究间无统计学异质性,故采用固定效应模型进行合并分析。2组差异无统计学意义[RR=0.99,95%CI(0.98,1.01)]。
(2)依维莫司VS吗替麦考酚酯:4个RCT包括5篇文献[7-11]报道了PSR。各研究间无统计学异质性,故采用固定效应模型进行合并分析。2组差异无统计学意义[RR=0.99,95%CI(0.97,1.01)]。见图5。

图1 2组急性排斥反应发生率的Meta分析Fig 1 Meta analysis of acute rejection rate for two groups

图2 2组肌酐清除率的Meta分析Fig 2 Meta analysis of creatinine clearance rate for two groups
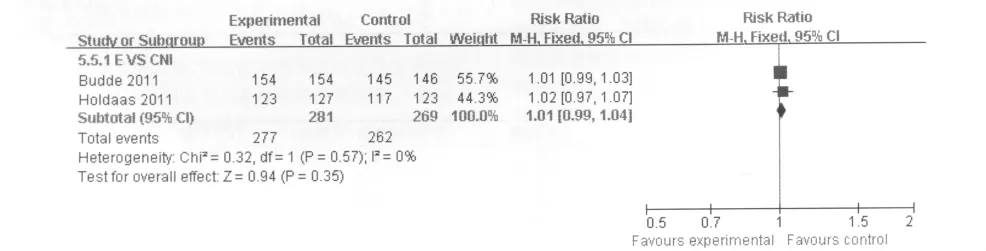
图3 依维莫司vs CNI移植物存活率的Meta分析Fig 3 Meta analysis of graft survival rate for Everolimus VS CNI

图4 依维莫司VS吗替麦考酚酯移植物存活率的Meta分析Fig 4 Meta analysis of graft survival rate for Everolimus VS MPA

图5 2组患者存活率的Meta分析Fig 5 Meta analysis of patient survival rate for two groups
2.4 安全性分析 根据临床异质性对纳入文献发生不良反应进行安全性评价。结果显示依维莫司VS吗替麦考酚酯,两组血清胆固醇水平、外周水肿和淋巴囊肿差异有统计学意义,其他指标差异无统计学意义,见表3。依维莫司VS CNI,两组血清胆固醇水平、贫血、腹泻、高脂血症、外周水肿差异有统计学意义,其他指标差异无统计学意义,见表4。

表3 依维莫司VS吗替麦考酚酯不良反应的Meta分析Tab 3 Meta analysis of adverse events for Everolimus VS MPA

表4 依维莫司VS钙调磷酸酶抑制剂不良反应的Meta分析Tab 4 Meta analysis of adverse events for Everolimus VS CNI
3 讨论
依维莫司进入细胞内后,与胞浆受体FK结合蛋白12结合,作用于雷帕霉素靶蛋白(mTOR),抑制活性,使细胞周期静止在G1期[12]。从而抑制生长因子(白细胞介素-2和15)介导的T细胞和B细胞的增殖和分化,并且介导其他细胞系包括纤维母细胞,平滑肌细胞和内皮细胞[13]。Giron等[14]总结了目前的临床试验数据,认为依维莫司与吗替麦考酚酯有相似的防止急性排斥反应发生的作用。Meta分析显示依维莫司在肾移植术后,急性排斥反应发生率、肌酐清除率、患者存活率和移植物存活率与其他药物相比均无统计学意义,表明依维莫司在随访期内表现出与其他免疫抑制方案相似的治疗疗效。随着免疫抑制剂的发展,尽管急性排斥反应的发生率已经降低,但是移植物的存活率并不尽如人意[15]。这与免疫抑制剂的应用过程中的安全性,顺应性和耐受性有关。由安全性分析可知,相对于吗替麦考酚酯和环孢素,依维莫司可以明显增高胆固醇水平,产生外周水肿和引起淋巴囊肿,并且对比环孢素有导致贫血和腹泻的可能性增加。Formica等[16]认为即使如此,依维莫司仍然增加了移植后免疫抑制治疗方案的选择性[16]。Chapman等[17]认为肾移植患者接受免疫抑制治疗发生肿瘤的风险增加。虽然实验室数据显示依维莫司具有可以通过对雷帕霉素靶蛋白酶的调节,对于肿瘤的治疗有靶向作用[18],Meta分析显示依维莫司对于抑制肿瘤发生有一定的作用,但是没有统计学意义。故需要进一步的长时间随访来观察。
本研究共纳入7个RCT,文献质量评价均为B级以上,文献质量较高。由于RCT存在临床异质性,故分亚组进行讨论。纳入研究中由于免疫抑制的治疗是多种药物联用且联用药物不尽相同,故对于合并效应量有一定的影响,并且在控制药物浓度由一定的差别,尚需更多高质量的随机对照试验以减少偏倚对于结果的影响。随访时间不尽相同且时间较短。期待有更长时间随访以获得远期疗效和安全性评价。
综上所述,依维莫司作为免疫抑制治疗的联用药物之一,在急性排斥反应发生率、肌酐清除率、患者存活率和移植物存活率等疗效指标与对照药物相似,不良反应主要表现在淋巴囊肿,外周水肿,增高胆固醇水平,其应用的安全性应予以重视。由于本研究所获取文献全出自国外,未见针对中国人的研究结果,提示依维莫司在中国人肾移植术后免疫抑制治疗的应用,尚待临床研究证据的产生。
[1]Laupacis A,Keown P,Pus N,etal.A study of the quality of life and cost-utility of renal transplantation[J].Kidney International,1996,50(1):235-242.
[2]Huang J,Manning BD.A complex interplay between Akt,TSC2,and the two mTOR complexes[J].Biochem Soc Trans,2009,37(Pt 1):217-222.
[3]Webster AC,Lee VW,Chapman JR,etal.Target of rapamycin inhibitors(sirolimus and everolimus)for primary immunosuppression of kidney transplant recipients:a systematic review and Meta-analysis of randomized trials[J].Transplantation,2006,81(9):1234-1248.
[4]Seckinger J,Sommerer C,Hinkel UP,etal.Switch of immunosuppression from cyclosporine A to everolimus:Impact on pulse wave velocity in stable de-novo renal allograft recipients[J].J Hypertens,2008,26(11):2213-2219.
[5]Budde K,Becker T,Arns W,etal.Everolimus-based,calcineurin-inhibitor-free regimen in recipients of de-novo kidney transplants:an open-label,randomised,controlled trial[J].Lancet,2011,377(9768):837-847.
[6]Holdaas H,Rostaing L,Seron D,etal.Conversion of long-term kidney transplant recipients from calcineurin inhibitor therapy to everolimus:A randomized,multicenter,24-month study[J].Transplantation,2011,92(4):410-418.
[7]Lorber MI,Mulgaonkar S,Butt KM,etal.Everolimus versus mycophenolate mofetil in the prevention of rejection in de novo renal transplant recipients:a3-year randomized,multicenter,phaseⅢstudy[J].Transplantation,2005,80(2):244-252.
[8]Tedesco Silva HJr,Cibrik D,Johnston T,etal.Everolimus plus reduced-exposure CsA versus mycophenolic acid plus standardexposure CsA in renal-transplant recipients[J].Am J Transplant,2010,10(6):1401-1413.
[9]Vitko S,Margreiter R,Weimar W,etal.Everolimus(certican)12-month safety and efficacy versus mycophenolate mofetil in de Novo renal transplant recipients[J].Transplantation,2004,78(10):1532-1540.
[10]Vitko S,Margreiter R,Weimar W,etal.Three-year efficacy and safety results from a study of everolimus versus mycophenolate mofetil in de novo renal transplant patients[J].Am J Transplant,2005,5(10):2521-2530.
[11]Bertoni E,Larti A,Rosso G,etal.Good outcomes with Cyclosporine very low exposure with Everolimus high exposure in renal transplant patients[J].J Nephrol,2011,24(5):613-618.
[12]Abraham RT.Mammalian target of rapamycin:immunosuppressive drugs uncover a novel pathway of cytokine receptor signaling[J].Curr Opin Immuno,1998,10(3):330-336.
[13]Schuler W,Sedrani R,Cottens S,etal.SDZ RAD,a new rapamycin derivative:Pharmacological propertiesinvitroandinvivo[J].Transplantation,1997,64(1):36-42.
[14]Giron F,Baez Y.Critical appraisal on the use of everolimus in renal transplantation as an immunosuppressant to prevent organ transplant rejection[J].Transplant Res Risk Manag,2010,2:11-14.
[15]Meier-Kriesche HU,Schold JD,Srinivas TR,etal.Lack of improvement in renal allograft survival despite a marked decrease in acute rejection rates over the most recent era[J].Am J Transplant,2004,4(3):378-383.
[16]Formica NR Jr,Lorber KM,Friedman AL,etal.The evolving experience using everolimus in clinical transplantation[J].Transplant Proc,2004,36(Suppl 2S):495S-499S.
[17]Chapman JR,Webster AC.Cancer after renal transplantation:the next challenge[J].Am J Transplant,2004,4(6):841-842.
[18]Yuan R,Kay A,Berg WJ,etal.Targeting tumorigenesis:Development and use of mTOR inhibitors in cancer therapy[J].J Hematol Oncol,2009,45(2):1-12.
