竹炭对亚甲基蓝的吸附平衡和动力学研究
2012-12-26王春芳宋秭龙王婷婷王伟涛李润泽胡颜荟赵地顺
张 娟,王春芳,宋秭龙,王婷婷,王伟涛,王 蒙,李润泽,胡颜荟,赵地顺
(河北科技大学化学与制药工程学院,河北石家庄 050018)
竹炭对亚甲基蓝的吸附平衡和动力学研究
张 娟,王春芳,宋秭龙,王婷婷,王伟涛,王 蒙,李润泽,胡颜荟,赵地顺
(河北科技大学化学与制药工程学院,河北石家庄 050018)
研究了室温下竹炭对亚甲基蓝的吸附平衡和动力学,考察了亚甲基蓝初始浓度和吸附剂用量的影响。由Langmuir吸附等温模型、Freundlich吸附等温模型对吸附平衡数据进行拟合;动力学由准一级反应方程和准二级反应方程进行拟合。研究结果表明:Freundlich吸附等温线模型(R2=0.99)更为精确地描述了亚甲基蓝在竹炭上的吸附;吸附动力学由二级动力学模型拟合更为准确。对动力学数据进行了计算和讨论。
竹炭;亚甲基蓝;吸附平衡;动力学
纺织工业广泛使用染料来给纺织品染色,因此纺织业最大的问题就是染料废水的排放,处理不当会污染水环境。中国印染废水日排放量为300万t~400万t,由于染料生产品种多,并朝着抗光解、抗热及抗生物氧化方向发展,使得染料废水的处理难度加大,一些染料废水还具有“致癌、致畸、致突变”作用[1]。因此,染料废水的处理一直是国内外废水处理的难点之一。亚甲基蓝废水由于有机物含量高、色度深、碱性大、水质变化大、生物毒性大,成为极难处理的染料废水之一。吸附法是去除水体中亚甲基蓝等染料的有效方法之一,常用的吸附剂有黏土矿物[2]、活性炭[3-4]和生物质[5]等。目前,中国大多数活性炭都是由木材烧制的,但是中国的木材资源日渐匮乏,而丰富的竹子资源却还没有被充分开发利用。近年来,竹炭(bamboo carbon,简称BC)作为新型吸附材料的研究在日本和中国已经成为炭材料研究领域中的一个热点[6-9],但是日本应用的竹炭主要从中国进口。在中国,以竹炭为吸附剂,吸附去除水中苯酚的研究较多[10-12],而对于吸附亚甲基蓝的研究较少。本研究采用竹炭为吸附剂,研究其对染料废水中的亚甲基蓝的吸附性能,为亚甲基蓝废水的净化提供一种新的方法。
1 实验部分
1.1 主要试剂与仪器
亚甲基蓝(简称MB,国药集团化学试剂有限公司提供);实验用水为二次蒸馏水;竹炭(浙江遂昌卖炭翁生态开发有限公司提供)。
UV1000型紫外-可见分光光度计(上海天美公司提供);S4800型扫描电子显微镜(日本Hitachi公司提供)。
1.2 MB标准曲线的绘制
因为MB在紫外-可见光区有4个吸收峰,配置不同浓度的MB水溶液,在最高吸收峰665 nm波长处用紫外-可见分光光度计测定吸光度,绘制标准曲线。
1.3 吸附实验
本实验中将竹炭直接用蒸馏水洗涤、煮沸、干燥后,研磨成0.250~0.425 mm(40~60目)的颗粒。称取不同量的竹炭,放入100 m L MB水溶液中,振荡24 h,测MB水溶液的吸光度,计算去除率,得出竹炭的最佳用量。
MB去除率A(%)和平衡时竹炭对亚甲基蓝的吸附量用式(1)和式(2)计算。

式中:qe表示每单位质量的吸附剂吸附MB的平衡吸附量;V是溶液体积;C0是MB初始浓度;Ceq是吸附达到平衡后的最终浓度;ms是吸附前竹炭的质量。
测定吸附动力学实验时,固定吸附剂用量和MB溶液浓度,在一定的时间间隔内取样测定MB浓度,吸附量qt的计算见式(3):

式中:C0是MB溶液的起始浓度;Ct是时间t时MB溶液的浓度;V是溶液体积;ms是吸附前竹炭的质量。
2 结果与讨论
2.1 竹炭的表征
图1是竹炭的SEM照片,图1 a)是竹炭0.250~0.425 mm(40~60目)的横切图,图1 b)是竹炭0.250~0.425 mm(40~60目)的纵切图。从图1 a)上可以明显地看出竹炭的大孔结构,最大孔径高达200μm;从图1 b)可以看出,在大孔的内壁上还有很多均匀的中孔和微孔,可见竹炭的孔结构非常发达。
2.2 竹炭用量对MB吸附效果的影响
室温下,固定亚甲基蓝水溶液的浓度,取500 m L MB溶液,改变竹炭的用量,考察竹炭用量对MB吸附效果的影响,见图2。从图2可以看出,随着竹炭用量的增加,MB的去除率随之增加。这是因为随着竹炭用量的增加,竹炭的吸附活性位增加。当竹炭用量超过0.5 g时,MB的去除率增加趋势缓慢还略显下降。这是因为过多的竹炭会发生重叠,会遮挡一部分吸附活性位,因此竹炭用量不是越多越好,太多不仅是一种浪费,吸附效果也会略有下降。最佳用量为0.5 g,在后期实验中,均采用0.5 g。
2.3 吸附时间和MB初始质量浓度对吸附效果的影响

图1 竹炭的SEM照片Fig.1 SEM images of bamboo carbon
吸附平衡是由平衡条件决定的,因此测定了一系列不同原始MB质量浓度(50~500 mg/L)随着吸附时间的变化情况,见图3。从图3可知:竹炭吸附MB的量随着时间的延长而增加,但是接触时间大致超过90 min后,吸附量趋于一个固定值而不再增加,这时候,MB在竹炭上吸附的量和解吸的量达到一个动态平衡,所以吸附量不再增加。吸附达到平衡的时间成为平衡时间,在平衡时间的吸附量反映了吸附剂在操作条件下的最大吸附量。
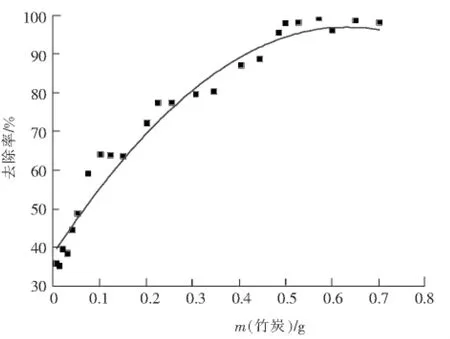
图2 竹炭用量对MB吸附去除率的影响Fig.2 Effect of amount of BC on removal ratio of MB

图3 室温下不同初始MB质量浓度下吸附能力随吸附时间的变化Fig.3 Variation of adsorption capacity with adsorption time at various initial MB concentrations at room temperature
2.4 溶液p H值对吸附的影响
在p H值为2~11范围内,固定其他条件不变,取250 mg/L的溶液,用0.1 mol/L的NaOH或0.1 mol/L的HCl溶液调节溶液p H值,考察溶液初始p H值对染料吸附的影响,结果见图4。由图4可见,溶液初始p H值对吸附影响较大,p H值为2~7时,随着p H值的增加,单位吸附量增加迅速;p H值为7~11时吸附量变化不明显。原始溶液p H值接近7可不调节。
2.5 温度对吸附的影响
温度对吸附的影响见图5。由图5可知,随着温度的升高,qe随之增加。因为随着温度的升高,溶液的黏度下降,亚甲基蓝的运动阻力减小,因此亚甲基蓝质量传递的迁移速度加快,从而造成qe增加。根据液相吸附中的“溶剂置换”理论,升温同时也加速了活性炭外表面吸附水分子的解吸,从而增加了吸附亚甲基蓝的活性位。但是温度过高,会造成吸附剂的变质。因此,温度最好还是不要太高。
2.6 Langmuir吸附等温线模型
Langmuir吸附等温线模型可以用直线形式表示[13],见式(4)。

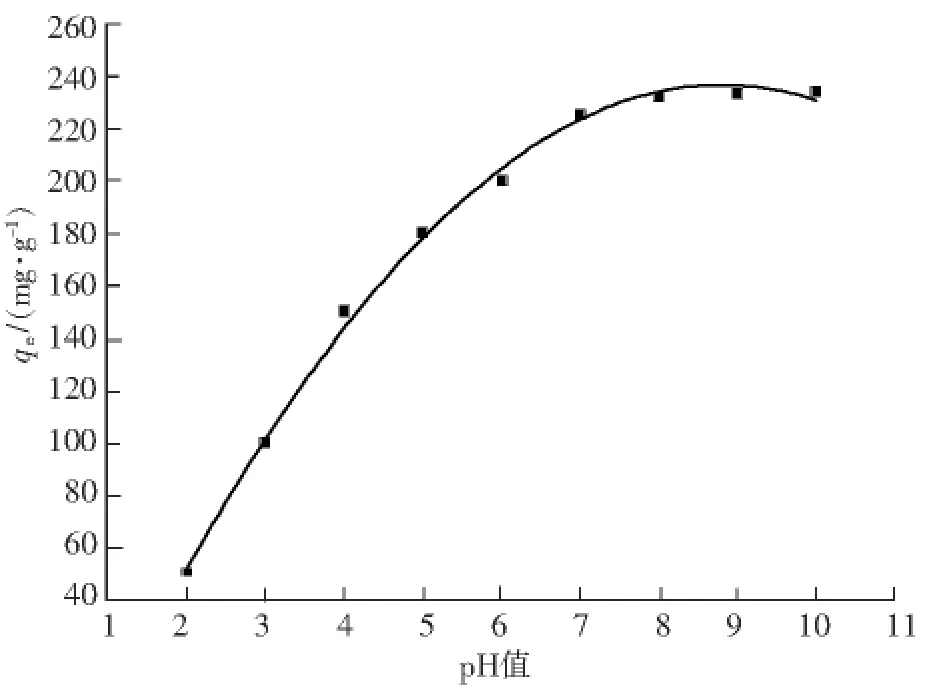
图4 p H值对吸附的影响Fig.4 Effect of p H value on adsorption
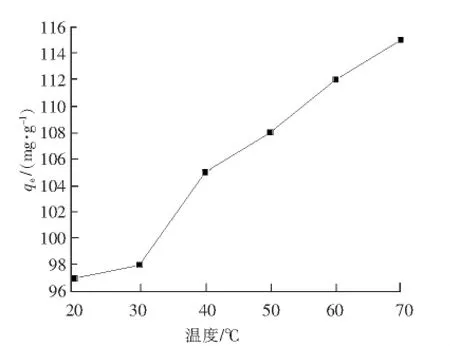
图5 温度对吸附的影响Fig.5 Effect of temperature on adsorption
式中:Ce表示MB的平衡质量浓度;qe是每单位质量的吸附剂平衡吸附量;qm是最大吸附量;KL是Langmuir吸附速率常数。若Ce/qe对于Ce可以绘制一条直线,那就说明MB在竹炭上的吸附遵循Langmuir吸附等温线,直线的斜率是1/qm(见图6)。KL和qm可以通过计算得出,结果列于表1。

表1 MB的Langmuir and Freundlich吸附常数Tab.1 Langmuir and Freundlich isotherm constants for methylene blue
2.7 Freundlich吸附等温线模型
著名的Freundlich吸附等温线模型有2种表示方式[13],分别见式(5)和式(6)。
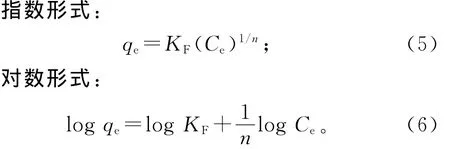
式中:Ce是 MB的平衡质量浓度(mg/L);qe是每单位质量的吸附剂平衡吸附量(mg/g);KF表示吸附剂的吸附能力;n表示吸附质和吸附剂之间的亲和力。若logqe对于logCe可以绘制一条直线,斜率为1/n(见图7),就表明 MB的吸附遵循Freundlich吸附等温线模型。
1/n的数值在0和1之间,是表示吸附剂表面
非均匀性的一个参数。1/n越接近于0,表明吸附剂表面越不均匀[14]。Langmuir和Freundlich吸附常数和拟合相关系数列于表1,Freundlich模型拟合的相关系数(R2=0.99)明显优于Langmuir模型拟合的相关系数(R2=0.90)。因此,MB在竹炭上的吸附行为更符合Freundlich吸附等温线模型。
2.8 MB在竹炭上的吸附动力学
实验测定MB在竹炭上的吸附在90 min基本达到平衡,90 min以后竹炭对MB的吸附能力增加缓慢。因此,在120 min内对MB在竹炭上的吸附动力学进行测定。吸附速率常数根据准一级动力学方程决定[15],见式(7)。

图6 MB在竹炭上的Langmuir吸附等温线Fig.6 Langmuir adsorption isotherm of methylene blue on BC

式中:qe表示每单位质量的吸附剂吸附MB的平衡吸附量;qt表示时间t时的吸附量(mg/g);k1是吸附速率常数(min-1)。若ln(qe-qt)对于t可以绘制一条直线(见图8),则由直线斜率得k1。结果列于表2。由表2可以看出,实验测得和由直线计算得到的qe值不一致,这说明MB在竹炭上的吸附动力学不符合一级动力学。
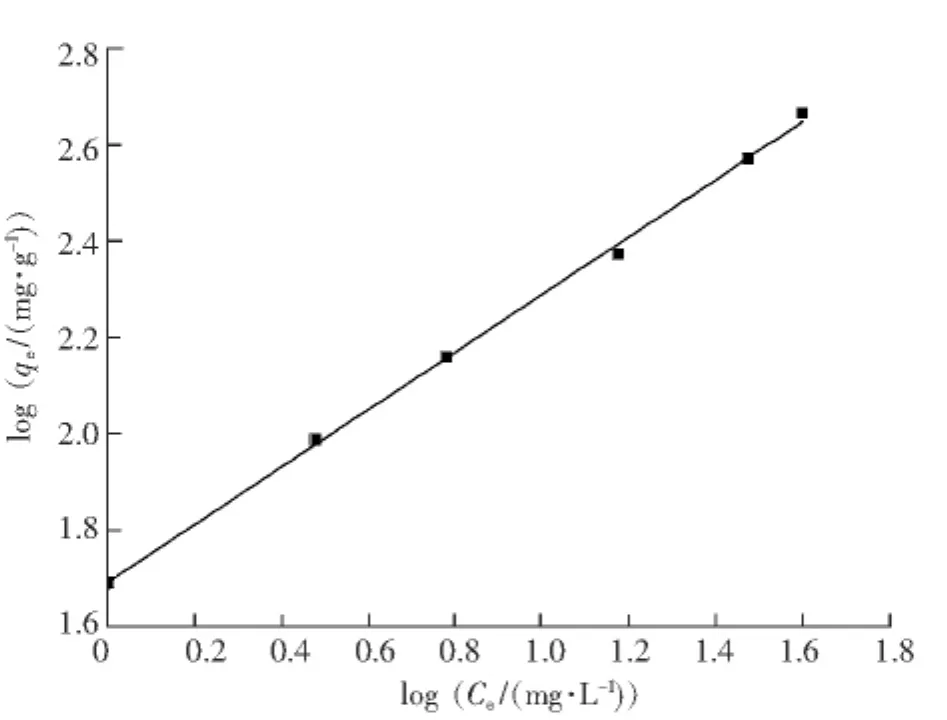
图7 MB在竹炭上的Freundlich吸附等温线Fig.7 Freundlich adsorption isotherm of methylene blue on BC
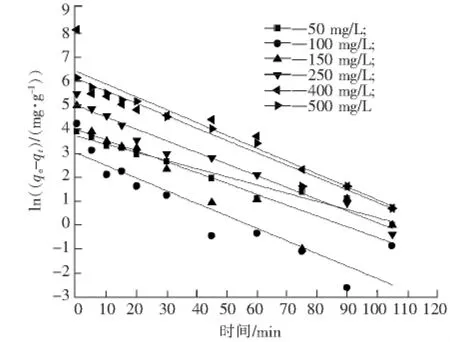
图8 MB在竹炭上的准一级动力学Fig.8 Pseudo-first-order kinetics for adsorption of methylene blue on BC
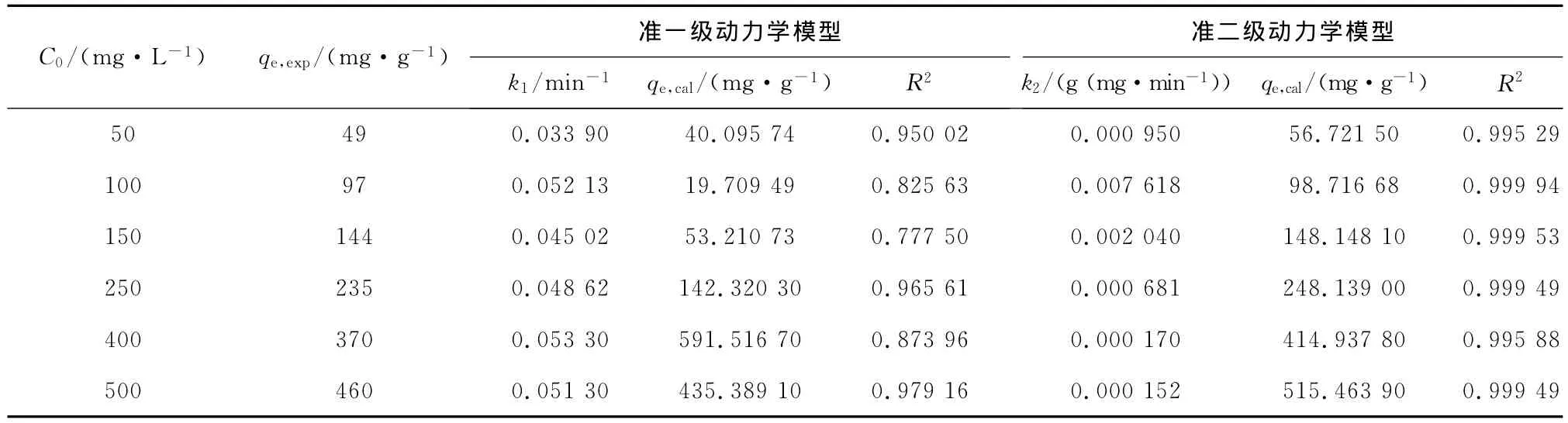
表2 准一级和准二级动力学吸附速率常数的比较Tab.2 Comparison of the pseudo first-and second-order adsorption rate constants
另一方面,基于吸附平衡的准二级动力学方程[17]用式(8)表示:
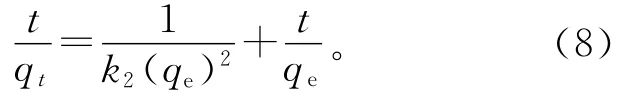
式中:qe是每单位质量的吸附剂的平衡吸附量;k2是准二级化学吸附平衡速率常数(g/(mg·min))。若这个模型有效,qe计算值应该等于实验测得值。若t/qt对于t作图可得一条直线,qe值和k2值就由直线的斜率和截矩算得,见图9。由图9可见。t/qt对于t作图确实是一条直线,而且qe实验值和计算值比较接近(见表2)。二级动力学模型的相关系数R2≥0.995,相关性很好,这表明 MB在竹炭上的吸附动力学为二级动力学。
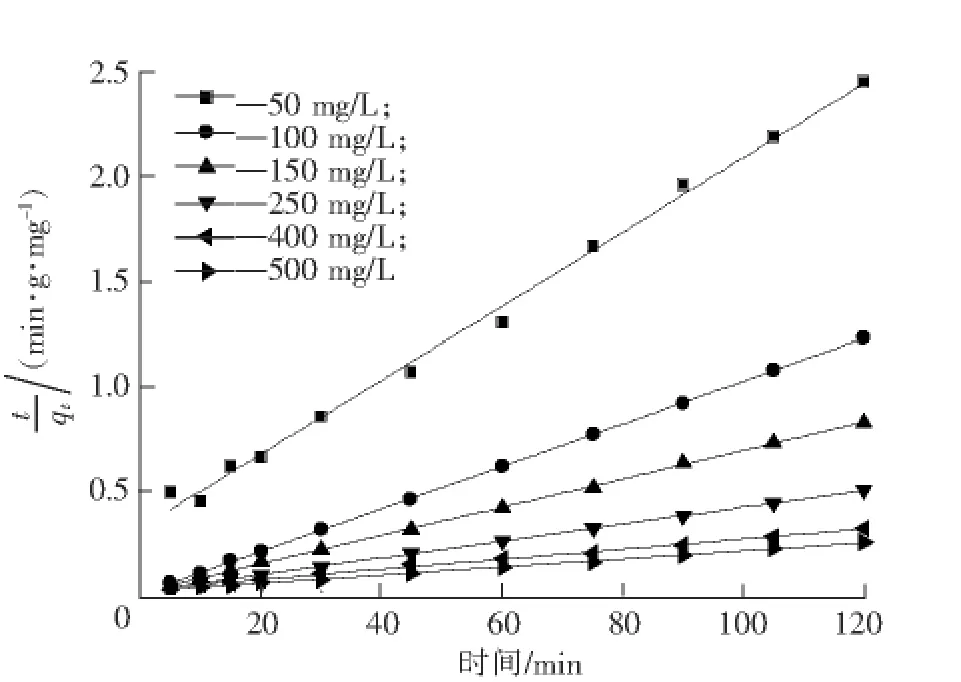
图9 MB在竹炭上的准二级动力学Fig.9 Pseudo-second-order kinetics for adsorption of methylene blue on MB
3 结 语
研究了室温下竹炭对不同浓度的MB溶液的吸附平衡和动力学,结果发现竹炭对MB有很强的吸附能力。基于两大著名的吸附模型,实验结果表明,Freundlich模型拟合的相关系数明显优于Langmuir模型拟合的相关系数。因此,MB在竹炭上的吸附行为用Freundlich吸附等温线模型来描述更为精确。由一级吸附动力学模型得到的qe计算值和实验值相差甚远,误差较大;而由二级动力学模型得到的qe计算值和实验值非常接近,误差较小。且二级动力学模型的相关系数R2≥0.995,因此MB在竹炭上的吸附动力学是二级动力学。此外,中国是竹子生长大国,更应该大力开发竹炭的应用研究领域。现在竹炭主要用于保健、净化空气,宣传力度也比较大,而用于工业研究的较少。本研究结果为MB废水的处理提供新的理论基础和方法,表明竹炭在化学工业的应用前景广阔,呼吁广大研究者致力于中国生物资源的充分开发和利用。
[1]BHATTACHARYYA K G,SARMA A.Kinetics and thermodynamics of methylene blue adsorption on neem (azadirechta indica)leaf powder[J].Dyes Pigm,2005,65(1):51-59.
[2]姚 超,刘 敏,李为民,等.凹凸棒石/氧化锌纳米复合材料对亚甲基蓝的吸附性能[J].环境科学学报(Acta Scientiae Circumstantiae),2010,30(6):1 211-1 219.
[3]左宋林,刘军利,杨建校,等.磷酸活化法活性炭性质对亚甲基蓝吸附能力的影响[J].林产化学与工业(Chemistry and Industry of Forest Products),2010,30(4):1-6.
[4]FARIA P C C,ÓRFOJ J M,PEREIRA M F R.Adsorption of anionicand cationic dyes on activated carbons with different surface chemistries[J].Water Research,2004,38(8):2 043-2 052.
[5]李红萍,韩秀丽,刘国际.气体膨胀液体处理松针落叶对水体中亚甲基蓝的吸附研究[J].高校化学工程学报(Journal of Chemical Engineering of Chinese Universities),2010,24(6):326-330.
[6]ABE I,FUKUHARA T,MARUYAMA J,et al.Preparation of carbonaceous adsorbents for removal of chloroform from drinking water[J].Carbon,2001,39:1 069-1 073.
[7]姜树海,张齐生,蒋身学.竹炭材料的有效利用理论与应用研究进展[J].东北林业大学学报(Journal of Northeast Forestry University),2002,30(4):53-56.
[8]MIZUTA K,MATSUMOTO T,HATATE Y,et al.Removal of nitrate-nitrogen from drinking water using bamboo powder charcoal[J].Bioresour Technol,2004,95:255-257.
[9]池岛庸元.木炭、竹炭大百货[M].日本京都:チャエ-ル.エミエニテイ,2000.
[10]朱江涛,黄正宏,康飞宇,等.活性竹炭对苯酚的吸附动力学[J].新型炭材料(New Carbon Materials),2008,23(4):326-330.
[11]王秀芳,张会平,肖新颜,等.苯酚在竹炭上的吸附平衡和动力学研究[J].功能材料(Journal of Functional Materials),2005,36(5):746-749.
[12]王桂仙,张启伟.竹炭吸附对氨基苯酚的热力学及动力学研究[J].林产化学与工业(Chemistry and Industry of Forest Products),2011,31(3):84-88.
[13]HAMEED B H,DIN A T M,AHMAD A L.Adsorption of methylene blue onto bamboo-based activated carbon:Kinetics and equilibrium studies[J].Journal of Hazardous Materials,2007,141:819-825.
[14]FYTIANOS K,VOUDRIAS E,KOKKALIS E.Sorption–desorption behavior of 2,4-dichlorophenol by marine sediments[J].Chemosphere,2000,40:3-6.
[15]KANNAN N,SUNDARAM M M.Kinetics and mechanism of removal of methylene blue by adsorption on various carbons comparative study[J].Dyes Pigments,2001,51:25-40.
[16]HO Y S,MCKAY G.Sorption of dye from aqueous solution by peat[J].Chem Eng J,1998,70:115-124.
[17]李秋荣,刘 遥.等离子体改性制备 NiO-TiO2/SiO2及其对甲基橙的降解性能[J].燕山大学学报(Journal of Yanshan University),2011,35(2):109-114.
[18]赵梦清,于桂花,张 波,等.大孔吸附树脂对头孢菌素C的吸附动力学研究[J].河北工业科技(Hebei Journal of Industrial Science and Technology),2008,25(2):76-78.
[19]朱华跃,蒋 茹.交联壳聚糖膜制备及对酸性大红染料吸附作用[J].河北科技大学学报(Journal of Hebei University of Science and Technology),2009,30(1):54-57.
Adsorption equilibrium and kinetic of methylene blue on bamboo carbon
ZHANG Juan,WANG Chun-fang,SONG Zi-long,WANG Ting-ting,WANG Wei-tao,WANG Meng,LI Run-ze,HU Yan-hui,ZHAO Di-shun
(College of Chemical and Pharmaceutical Engineering,Hebei University of Science and Technology,Shijiazhuang Hebei 050018,China)
The adsorption equilibrium and kinetic of methylene blue dye on bambo carbon(BC)were examined at room temperature,and the effect of the original concentration of methylene blue and the amount of bamboo carbon were measured.Adsorption isotherm of the methylene blue(MB)on the bamboo carbon was determined and correlated with Langmuir and Freundlich adsorption isotherm equations.Two simplified kinetic models including pseudo-first-order and pseudo-second-order equation were selected to follow the adsorption processes.The result shows that the equilibrium data for methylene blue adsorption fit to the Freundlich equation(R2=0.99)well.The adsorption of methylene blue could be best described by the pseudo-second-order equation.The kinetic parameters of this best-fit model were calculated and discussed.
bamboo carbon;methylene blue(MB);adsorption equilibrium;kinetics
TQ424
A
1008-1542(2012)05-0416-06
2012-07-01;
2012-09-06;责任编辑:张士莹
国家自然科学基金资助项目(21106032);河北科技大学博士科研启动基金资助项目(QD201010)
张 娟(1974-),女,河北泊头人,讲师,博士,主要从事清洁能源与绿色化工方面的研究。
