丁烯氟虫腈光降解反应过程及机理
2012-12-26夏婷婷陈景文蔡喜运大连理工大学环境学院工业生态与环境工程教育部重点实验室辽宁大连116024
王 钰,夏婷婷,陈景文,蔡喜运 (大连理工大学环境学院,工业生态与环境工程教育部重点实验室,辽宁 大连116024)
丁烯氟虫腈光降解反应过程及机理
王 钰,夏婷婷,陈景文,蔡喜运*(大连理工大学环境学院,工业生态与环境工程教育部重点实验室,辽宁 大连116024)
考察了乙腈/水混合溶液中丁烯氟虫腈的光解速率及水体中主要溶解性物质对其光解的影响,通过产物鉴定及模拟计算判定了丁烯氟虫腈光降解反应机理.结果表明,模拟日光下丁烯氟虫腈快速发生光降解,纯水中反应半衰期为 17.34 min.腐殖酸通过竞争光吸收来抑制丁烯氟虫腈的光解,NO3-和 Cl-对其光解无影响.丁烯氟虫腈光解反应位点位为亚砜基团上的硫原子,主要产物为脱硫化物(MW 442.0),砜化物(MW 506.0)及2种硫化物(MW 473.9和405.8).键级和键长分析也证实丁烯氟虫腈硫原子连接的化学键不稳定,易发生断裂重排反应,生成上述转化产物.
丁烯氟虫腈;光降解;溶解性物质;反应机理
氟虫腈为苯基吡唑类广谱型杀虫剂,具有杀虫活性高,应用范围广,与已有农药无交互抗性的特点.因其在水和土壤中降解缓慢[1-3],2009年10月 1日起我国境内停止销售和使用含有氟虫腈成分的农药制剂(卫生用及旱田种子包衣剂除外).氟虫腈 5位氨基的差异性取代,可能生成具有不同生物毒性的活性结构[4].采用甲代烯丙基取代氟虫腈的5位氨基氢原子,可合成一种新型杀虫剂丁烯氟虫腈[5].该农药可用于鳞翅目,蝇类和鞘翅目害虫等有害生物防治,在水稻与蔬菜等作物上具有与氟虫腈相当的杀虫活性,但对家蚕低毒,对鸟类中低毒,对鱼类的毒性是氟虫腈的千分之一.
研究表明,光解是氟虫腈及氟乙腈等苯基吡唑类杀虫剂重要的降解途径,水中溶解性物质对其光解产生影响[6-7].目前,关于丁烯氟虫腈光降解的研究尚未见报道.研究丁烯氟虫腈在环境中的光解降解行为,将有助于评估其环境归趋及环境风险.本研究选取模拟太阳光为光源,研究丁烯氟虫腈在乙腈/水溶液中的光降解行为;考察了溶解性物质(HA,NO3-,Cl-)对其光解反应速率的影响;进行了产物鉴定并利用模拟计算的方法研究了丁烯氟虫腈的光解反应机理.
1 材料与方法
1.1 材料
丁烯氟虫腈(纯度98.1%)由大连瑞泽农药股份有限公司提供;腐殖酸(HA,Fluka NO.53680)购于Sigma-Aldrich公司;乙腈、甲醇、石油醚、乙酸乙酯及正己烷均为色谱纯.
1.2 光解实验
光解实验在 XPA-1旋转光化学反应仪(南京胥江机电厂)中进行,光源为模拟太阳光(300W 汞灯+290nm滤光片,λ>290nm),反应液置于石英管中.丁烯氟虫腈浓度为1mg/L.鉴于丁烯氟虫腈在纯水中溶解度较低,添加乙腈作为助溶剂,溶液中乙腈体积比例 20%,30%,40%,50%.水体中主要溶解性物质的浓度设定参照其常见环境水平[8-9]. HA 浓度设置为2,4,8,12,15mg/L;NO3-浓度设置为5,10,15, 20,30mg/L;Cl-浓度设置为 10,20,30,40,60mg/L.光解实验过程中设置暗对照,每组实验重复2次.
采用准一级反应动力学描述光解反应,并使用 ln(Ct/C0)-t线性拟合得到准一级反应速率常数(k).半衰期使用公式t1/2=ln2/k计算.
1.3 样品分析
采用 Techcomp UV-2003型紫外可见分光光度计测定样品紫外可见吸收光谱;使用Hitachi L2000型高效液相色谱(Hitachi)测定丁烯氟虫腈浓度,色谱条件如下:色谱柱为大连依利特 YWG C18(10µm,250nm×4.6mm);流动相为甲醇:乙腈:水=35:40:25(体积比);流速为 1.0mL/min;检测波长为215nm;进样量10µL.
1.4 产物鉴定
将100mL含10mg/L丁烯氟虫腈的反应液置于光解实验条件下连续光照 10h.反应液用石油醚:乙酸乙酯(V: V) = 50:50萃取3次,有机相经无水硫酸钠脱水后于旋转蒸发器中浓缩至近干,用甲醇定容至1mL待测.
采用Agilent 1100 LC/MS/MS(Agilent)进行产物分析鉴定.分析条件如下:色谱柱为 Zorbax SB-C18(1.5µm,2.1mm×50mm);流动相为甲醇:乙腈:水=35:40:25(体积比);流速为 0.2mL/min;进样量为5µL;离子源为ESI,负离子扫描模式;质量扫描范围100~600m/z[10].
1.5 键长键级的计算
使用Gaussian 09软件对丁烯氟虫腈及氟虫腈的分子结构进行优化并对其键长、键级进行计算.使用 PM3算法预优化目标化合物,利用密度泛函理论(DFT)中B3LYP泛函在6-31G(d,p)基组水平优化获得稳定构型,并对稳定构型进行频率分析[11-12];采用Natural Bond Orbital (NBO)方法进行键级计算[13].
2 结果与讨论
2.1 丁烯氟虫腈在不同比例乙腈溶液中的光解
由图1可知,实验条件下丁烯氟虫腈迅速光解,遵循准一级反应动力学方程(R2> 0.95).乙腈对光解过程产生抑制作用,作用效果随其体积百分比的增加而增强.乙腈的加入一方面降低了溶剂极性,一方面可能增强了体系的紫外可见光吸收强度,起到光掩蔽作用[14-15].
丁烯氟虫腈光反应速率与溶液中乙腈比例线性负相关,拟合得方程,Y=-0.0327X+3.9952(R2= 0.85,P<0.001),外推得到丁烯氟虫腈在纯水中光解反应速率为3.99×10-2min-1,半衰期17.35min.
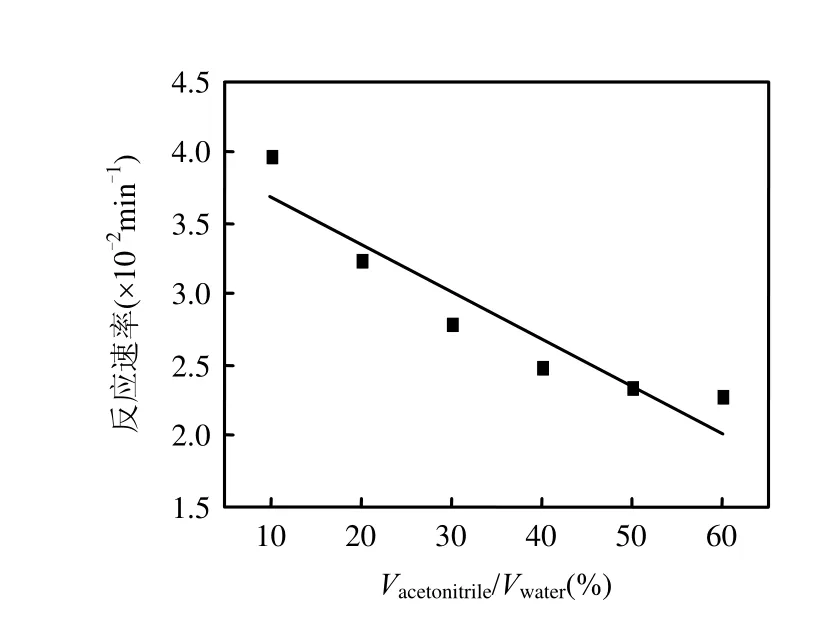
图1 乙腈对丁烯氟虫腈光解的影响Fig.1 Effect of the acetonitrile concentration on the butylene fipronil photolysis rate constants
2.2 溶解性物质对丁烯氟虫腈光降解的影响
由表 1可知,加入腐殖酸(2~15mg/L)显著抑制丁烯氟虫腈的光解,抑制效应与腐植酸浓度表现出明显的线性相关(R2>0.95,P<0.05).溶液中乙腈比例为20%时, 2,4,8,12,15mg/L腐殖酸的光解反应抑制率分别为 8.9%,17.8%,34.6%,42.7%, 51.6%.腐殖酸的加入增强了体系 190~300nm的紫外可见光吸收(图 2),产生强烈光掩蔽效应,进而对丁烯氟虫腈的光降解产生抑制作用.这与Walse等[16]对氟虫腈光解的研究结果一致,腐殖酸等可溶性有机质可通过竞争光吸收及淬灭激发态来影响氟虫腈的光解反应速率.

表1 溶解性物质对丁烯氟虫腈光解反应速率的影响(×10-2min-1)Table 1 Values of k calculated from photolysis data (×10-2min-1)
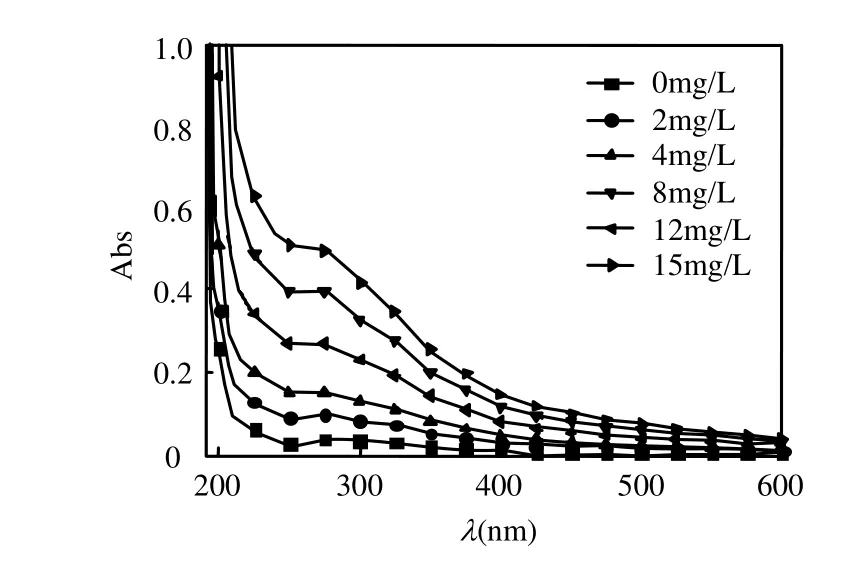
图2 腐殖酸对体系紫外可见吸光光谱的影响Fig.2 UV-vis absorption spectra of butylene fipronil in the presence of HA
NO3-(5~30mg/L)对丁烯氟虫腈光解无影响.有研究表明,NO3-主要通过光屏蔽作用及产生活性氧物种(ROS)来影响化合物光降解过程[8,17-18].本研究中NO3-显著增强体系190~250nm的紫外可见光吸收强度,但模拟日光照射下化合物实际接受λ>290nm范围内的光照,NO3-与丁烯氟虫腈不存在竞争光吸收关系.而反应中产生的ROS一方面促进化合物的光降解,另一方面可通过竞争吸收对光解产生抑制作用.
研究表明,Cl-可捕获·OH转化成 Cl2,影响化合物的间接光解,而其对光解的双重作用机理仍有待于研究[9,19].添加 3%的 NaCl可提高氟虫腈光解反应速率 20%[16].在本研究中 10~60mg/L Cl-对丁烯氟虫腈光解反应速率未产生显著影响,对体系紫外可见吸收光谱亦无影响.可能原因是丁烯氟虫腈未发生间接光解,此外,Cl-双重作用机理相互抵消,表观上呈现出无影响.
环境水体中,HA,NO3-及 Cl-等光活性物质共存,单独和交互的影响化合物的光化学行为,致使化合物的环境光化学行为更趋复杂[16].
2.3 丁烯氟虫腈光降解产物鉴定
由图4可知,丁烯氟虫腈光解后生成一系列产物.使用 ESI负离子模式扫描光解产物,得到M,M-1,M+Cl及M+62离子碎片.其中分子离子失去H形成的M—H及获得COO-和H2O形成的M+62碎片离子表现为强峰,用于定性分析.离子碎片解析结果表明,丁烯氟虫腈(MW 489.9)光解主要生成4种产物.脱硫化物(MW 442.0, 5-甲代烯丙基氨基-1-(2,6-二氯-4-三氟甲基苯基)-4-三氟甲基-3-氰基吡唑),砜化物(MW 506.0, 5-甲代烯丙基氨基-1-(2,6-二氯-4-三氟甲基苯基)-4-三氟甲基磺酰基-3-氰基吡唑)及两种硫化物(MW 473.9, 5-甲代烯丙基氨基-1-(2,6-二氯-4-三氟甲基苯基)-4-三氟甲基硫基-3-氰基吡唑; MW 405.8, 5-甲代烯丙基氨基-1-(2,6-二氯-4-三氟甲基苯基)-4-巯基-3-氰基吡唑).该结果与文献中报道的氟虫腈光降解产物质谱分析结果相一致[10,23].
以往研究表明,氟虫腈在水环境中迅速光解.光解主产物为脱硫化物氟甲腈,并有伴微量砜化物,硫化物,脱三氟甲基亚硫酰基及磺酸衍生物生成[20-23].综上,丁烯氟虫腈与氟虫腈具有相似的产物构成,其光解途径可能与氟虫腈相似.
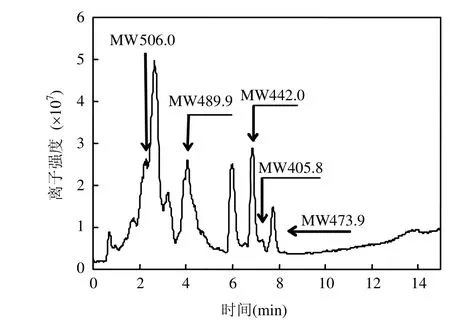
图3 丁烯氟虫腈光解产物的总离子色谱Fig.3 Total ion chromatogram of photoproduct
2.4 丁烯氟虫腈的理论计算及光解反应机理

图4 氟虫腈(a,c)及丁烯氟虫腈(b,d)的键长键级Fig.4 Bond order and length of fipronil and butylene fipronil
理论上,化学键越稳固,键能越大,键长越短,键级则越大[24].丁烯氟虫腈C4—S8,S8=O9及S8—C10的键长(或键级)分别为1.7806 (0.9355), 1.5095 (1.2465)及 1.9099 (0.7631);氟虫腈 C4—S8,S8=O9及 S8—C10的键长(或键级)分别为1.7714(0.9440),1.2283 (1.2283)及 1.9119(0.7620).2种化合物的C4—S8, S8—C10键键长较长,键级较小,表现出不稳定性,光降解过程中较易发生断裂(图4).该结果与产物鉴定中得到的丁烯氟虫腈及氟虫腈[20-21]主要光解产物相一致,表明该化学键易于断裂,发生转化反应.
苯基吡唑类农药因结构相似性,可能具有相似的光解反应路径.产物鉴定及键长键级计算证实了氟乙腈和氟虫腈具有相同的光解反应活性中心,光照后均发生氧化,还原及脱亚磺酸基反应[7].甲代烯丙基取代氟虫腈 5位氨基氢而形成的丁烯氟虫腈,其S8原子周边化学键性能与氟虫腈相比未发生显著变化,加之光降解产物构成相似,判断丁烯氟虫腈与氟虫腈具有相同的光解反应机理(图5).光解反应中,丁烯氟虫腈C4—S8键断裂生成脱硫化物,质谱解析 MW=442.0; S8=O9断裂生成硫化物,质谱解析 MW=473.9; S8=O9及 S8—C10同时断裂生成硫化物,质谱解析MW=405.8; S8=O9氧化加氧生成砜化物质谱解析MW=506.0.
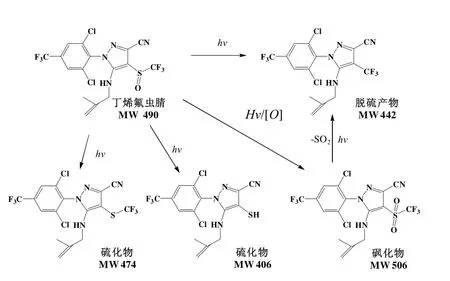
图5 丁烯氟虫腈光解反应路径Fig.5 Photolysis reaction mechanism of butylene fipronil in aqueous solution
然而丁烯氟虫腈与氟虫腈的光解产物在分布上存在显著差异.氟虫腈光降解产生脱硫化物的比例大于 50%;丁烯氟虫腈光解中未产生脱三氟甲基亚磺酰基产物,脱硫化物产率最高而2种硫化物产率相当,结合分子的立体结构可以解释该现象.氟虫腈生成脱硫化物及脱三氟甲基亚磺酰基产物需要邻位氨基氢的参与[20].反应时,O9首先与氨基氢形成大环氢键过渡态,而后生成产物.甲代烯丙基取代后,氧原子与氨基氢的空间位阻增加,氨基氢与氧原子的距离由2.0852增加至4.6201,不利于大环氢键过渡态的形成,进而抑制脱硫化物的生成.
3 结论
3.1 丁烯氟虫腈在模拟太阳光下可快速光解,半衰期为17.34min.
3.2 水体中腐殖酸可通过光掩蔽作用,抑制丁烯氟虫腈的光解,NO3-及Cl-对其光解无影响.
3.3 丁烯氟虫腈的光解反应活性位点为亚砜基团上的硫原子,该杀虫剂发生脱硫,还原及氧化反应,生成脱硫化物,砜化物及硫化物.
[1] Gunasekara A S, Truong T, Goh K S, et al. Environmental fate and toxicology of fipronil [J]. Journal of Pesticide Science, 2007,32(3):189-199.
[2] Nillos M G, Lin K, Gan J, et al. Enantioselectivity in fipronil aquatic toxicity and degradation [J]. Environmental Toxicology and Chemistry, 2009,28(9):1825-1833.
[3] Aajoud A, Ravanel P, Tissut M. Fipronil metabolism and dissipation in a simplified aquatic ecosystem [J]. Journal of Agricultural and Food Chemistry, 2003,51(5):1347-1352.
[4] Huber S K. (S)-Enantiomer enriched fipronil composition: US, PCT/EP2000/004172 [P]. 2000.4-12.
[5] 丁烯氟虫腈 [J]. 农药科学与管理, 2008,29(9):58.
[6] Ramesh A, Balasubramanian M. Kinetics and hydrolysis of fenamiphos, fipronil, and trifluralin in aqueous buffer solutions [J]. Journal of Agricultural and Food Chemistry, 1999,47(8): 3367-3371.
[7] Caboni P, Sammelson R E, Casida J E. Phenylpyrazole insecticide photochemistry, metabolism, and GABAergic action: Ethiprole compared with fipronil [J]. Journal of Agricultural and Food Chemistry, 2003,51(24):7055-7061.
[8] Fisher J M, Reese J G, Pellechia P J, et al. Role of Fe(III), phosphate, dissolved organic matter, and nitrate during the photodegradation of domoic acid in the marine environment [J]. Environmental Science and Technology, 2006,40(7):2200-2205.
[9] Chiron S, Minero C, Vione D. Photodegradation processes of the antiepileptic drug carbamazepine, relevant to estuarine waters [J]. Environmental Science and Technology, 2006,40(19):5977-5983.
[10] Lacroix M Z, Puel S, Toutain P L, et al. Quantification of fipronil and its metabolite fipronil sulfone in rat plasma over a wide range of concentrations by LC/UV/MS [J]. Journal of Chromatography B-Analytical Technologies in the Biomedical and Life Sciences, 2010,878(22):1934-1938.
[11] Becke A D, Johnson E R. A density-functional model of the dispersion interaction [J]. Journal of Chemical Physics, 2005, 123(15):154101.
[12] Chengteh L, Weitao Y, Par R G. Development of the Colle-Salvetti correlation-energy formula into a functional of the electron density [J]. Physical Review B (Condensed Matter), 1988,37(2):785-9.
[13] Frank W, Clark R L. Natural bond orbitals and extensions of localized bonding concepts [J]. Chemistry Education: Research and Practice in Europe, 2001,2(2):91-104.
[14] Schick B, Moza P N, Hustert K, et al. Photochemistry of vinclozolin in water and methanol-water solution [J]. Pesticide Science, 1999,55(11):1116-1122.
[15] Choi J, Choi W, Mhin B J. Solvent-specific photolytic behavior of octachlorodibenzo-p-dioxin [J]. Environmental Science and Technology, 2004,38(7):2082-2088.
[16] Walse S S, Morgan S L, Kong L, et al. Role of dissolved organic matter, nitrate, and bicarbonate in the photolysis of aqueous fipronil [J]. Environmental Science and Technology, 2004,38(14): 3908-3915.
[17] Mack J, Bolton J R. Photochemistry of nitrite and nitrate in aqueous solution: a review [J]. Journal of Photochemistry and Photobiology A-Chemistry, 1999,128(1-3):1-13.
[18] 展漫军,杨 曦,鲜啟鸣,等.双酚A在硝酸根溶液中的光解研究[J]. 中国环境科学, 2005,25(4):487-490.
[19] Liao C H, Kang S F, Wu F A. Hydroxyl radical scavenging role of chloride and bicarbonate ions in the H2O2/UV process [J]. Chemosphere, 2001,44(5):1193-1200.
[20] Bobe A, Meallier P, Cooper J F, et al. Kinetics and mechanisms of abiotic degradation of fipronil (hydrolysis and photolysis) [J]. Journal of Agricultural and Food Chemistry, 1998,46(7):2834-2839.
[21] Hainzl D, Casida J E. Fipronil insecticide: Novel photochemical desulfinylation with retention of neurotoxicity [J]. Proceedings of the National Academy of Sciences of the United States of America, 1996,93(23):12764-12767.
[22] Raveton M, Aajoud A, Willison J C, et al. Phototransformation of the insecticide fipronil: Identification of novel photoproducts and evidence for an alternative pathway of photodegradation [J]. Environmental Science and Technology, 2006,40(13):4151-4157.
[23] Ngim K K, Mabury S A, Crosby D G. Elucidation of fipronil photodegradation pathways [J]. Journal of Agricultural and Food Chemistry, 2000,48(10):4661-4665.
[24] Bruce A, Patricia E. Chemistry: Principles, Patterns, and Applications [M]. US:Pearson/Prentice Hall, 2007:409.
Kinetics and mechanism of photolysis of new insecticide butylene fipronil.
WANG Yu, XIA Ting-ting, CHEN Jing-wen, CAI Xi-yun*(Key Laboratory of Industrial Ecology and Environmental Engineering, Ministry of Education, School of Environmental Science and Technology, Dalian University of Technology, Dalian 116024, China). China Environmental Science, 2012,32(1):89~93
Photolysis of butylene fipronil was investigated, including reaction kinetics, transformation product identification and theoretical computation analysis. Photolysis of butylene fipronil under simulated sunlight was well fitted to first-order kinetic model with a half-life of 17.34min. Humic acids significantly reduced photoactivity of the insecticide, due to competitive light absorption, while NO3-and Cl-, didn’t affect its photolysis. Major transformation products were identified as desulfinyl derivative (MW 442.0), sulfone derivative (MW 506.0) and sulfide derivatives (MW 473.9 and 405.8). The proposed pathway of the insecticide was further confirmed by bond order and bond length analysis. The bonds round sulfur atom were easily broken and rearranged to form the transformation products.
butylene fipronil;photolysis;dissolved substances;mechanism
2011-03-19
国家自然科学基金资助项目(21077020);中国博士后科学基金资助项目(20090450103);中央高校基本科研业务费专项资金资助(DUT10LK02)
* 责任作者, 副教授, xiyuncai@dlut.edu.cn
X592
A
1000-6923(2012)01-0089-05
王 钰(1985-),女,辽宁大连人,大连理工大学环境学院硕士研究生,主要从事污染物环境光化学行为研究.
