铜基化学镀Ni-P-B合金工艺及镀层性能研究
2012-12-06石建华王钰蓉王文昌刘智超陈智栋
石建华, 王钰蓉, 王文昌, 刘智超, 陈智栋
(常州大学石油化工学院,江苏常州 213164)
铜基化学镀Ni-P-B合金工艺及镀层性能研究
石建华, 王钰蓉, 王文昌, 刘智超, 陈智栋
(常州大学石油化工学院,江苏常州 213164)
通过向Ni-P二元合金镀层中引入微量B元素,制备了性能优异的Ni-P-B三元合金镀层。研究了镀液中络合剂甘氨酸和乳酸、还原剂次磷酸钠和硼氢化钾对镀速、镀层成分的影响,确定镀液的最佳配方及工艺条件为25 g/L NiSO4·6H2O,30 g/L NH2CH2COOH,20 g/L CH3CH(OH)COOH,25 g/L NaH2PO2,0.2 g/L KBH4,1 mg/L CdSO4·8H2O,pH=12,θ=69 ~71 ℃。并对在最佳工艺条件下获得的镀层进行了耐腐蚀性、可焊性及与基体结合力的测试。结果表明,该镀层具有较好的抗腐蚀性和可焊性,并且与铜基体结合牢固。
化学镀;Ni-P-B合金镀层;可焊性;耐腐蚀性
引 言
随着表面贴装技术(SMT)在生产中的大规模应用,印制板(PCB)对焊盘的平整度、板面翘曲度和可焊性的要求愈加苛刻,而细导线、细间距的PCB对其制作技术也提出了更高的要求。集成电路(IC)与PCB板面的固定和装联是通过将芯片引出的端头用导线与印制板焊盘焊接而实现的。不论是金丝导线焊接还是铝基导线焊接,都要求PCB表面提供一个平整、可焊的焊盘[1-2]。目前,该焊盘一般为化学镀镍基合金,其中以Ni-P合金和Ni-B合金最为常用。Ni-P合金镀层的耐蚀性比Ni-B合金镀层好;而Ni-B合金镀层的可焊性、硬度和耐磨性比Ni-P合金镀层优越。Ni-P-B合金镀层兼有Ni-P和Ni-B镀层的优点,该镀层不仅具有较为优良的抗腐蚀性,而且B元素的加入赋予了镀层优异的耐磨性,镀层具有致密性好、可焊性好和孔隙率低等优点,能够满足焊盘表面两种焊接工艺的要求。
化学镀Ni-P-B合金是多元化学镀镍的一种,目前国内外已有部分研究报道,但多集中于中、高硼合金[w(B)=2.1% ~9.8%]。但中、高硼含量的多元镀层仍有许多的缺点,如性脆、韧性差、润滑性能低、与基体结合力不强而容易剥落等,在生产中不能很好的得到应用[3-4]。因而必须研究出具有高硬度、高韧性、优异抗腐蚀性能的合金镀层以满足生产要求,而化学镀高磷低硼[w(P)=6% ~9%,w(B)=0.5% ~1.5%]合金镀层具有上述优点。
在Ni-P-B合金镀层中,磷元素一般来自于次磷酸钠,而硼的来源是硼氢化钾或硼烷类化合物。硼烷类化合物能在相对宽松的环境中稳定存在,是比较理想的还原剂,但高昂的价格和较低的还原效率限制了其在生产中的应用;而硼氢化物不仅具有极高的还原能力和还原效率,价格也相对较低。但硼氢化物在中性及酸性条件下极易分解[5],该反应受温度、pH及溶液成分影响较大。根据Kreevoy等[6]提出的硼氢化物的分解经验公式,确定硼氢化物在生产中使用应保持pH≥11。
本文以电镀铜板为基体,以KBH4和NaH2PO2为还原剂,在pH=12的镀液中得到了高P低B的Ni-P-B合金镀层,并测试了沉积速度、镀层成分和各项性能。
1 实验方法
1.1 化学镀Ni-P-B合金镀层的制备
实验所用试样为0.2 mm×20 mm×10 mm的树脂覆铜板。化学镀的工艺流程为:基体抛光→水洗→脱脂→水洗→酸洗→水洗→钯活化→水洗→化学镀Ni-P-B合金→水洗→吹干。
所用试剂均为分析纯,镀液用去离子水配制,用10 g/L NaOH调节pH。
为了考察Ni-P-B合金镀层的形貌和可焊性,又制备了Ni-P合金镀层,将两种合金镀层的微观结构和可焊性进行了比较。实验中化学镀Ni-P合金溶液配方及操作条件为:

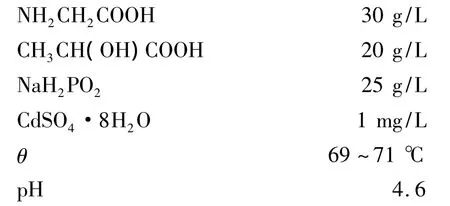
向化学镀Ni-P合金镀液中加入适量KBH4,获得化学镀Ni-P-B合金镀液。对镀液中络合剂和还原剂的影响进行正交试验,综合考虑沉积速度、镀层表观及成分等指标,获得化学镀Ni-P-B合金最佳溶液配方及操作条件为:

1.2 测试方法和条件
1.2.1 沉积速度测定
以单位时间内镀层厚度来表征沉积速度。计算方法:化学镀Ni-P-B合金后,测量镀层δ(μm),除以施镀 t(h)即为沉积速度(μm/h)。使用 EDX 1800-X型X-荧光光谱仪(苏州天瑞电子有限公司)测量镀层厚度。选择Ni-P-B/Cu工作曲线,利用纯银进行初始化,测定t为60 s,各试片随机测定10个点的厚度值,每点平行测定三次,取平均值。
1.2.2 镀层成分分析
利用 V(HCl)∶V(HNO3)∶V(H2O)=85∶10∶5 的混酸溶液溶解试片,采用ICPS-7510型电感耦合高频等离子体发射光谱仪(日本理学株式会社)测定镀层的成分。为防止B元素的挥发,溶解前酸液中需滴加0.1 mL 5%甘露醇。
1.2.3 镀层形貌及结构分析
利用JSM-6360LA型电子扫描显微镜(日本电子株式会社)和 OLYMPUS BX51型光学显微镜(400×)观察镀层形貌。
采用D/Max2500PC型X-射线衍射仪(日本理学株式会社)表征镀层晶体结构。测试前对试片进行脱脂处理,衍射角为15~80°。
1.2.4 耐蚀性能和可焊性测试
用CHI-660D电化学工作站(上海辰华仪器有限公司)测试镀层的耐蚀性能。以试片为工作电极,铂片为对电极,饱和甘汞电极为参比电极,分别在3.5%NaCl和 0.5 mol/L H2SO4溶液中,以 10 mV/s的扫描速度,室温下测试镀层极化曲线。
用流布面积法[7]测定镀层的可焊性。测试前用酒精对镀层进行脱脂处理,然后在试片中部放一个焊料环、在环中央滴加0.10 mL助焊剂。再将试片水平地放置在235℃的锡焊槽的熔融焊锡表面上保持30 s,取出试片并水平放置,冷却至室温,用无水乙醇擦去助焊剂残渣,观察焊料扩展情况。
用SKC-8H型润湿法[8]可焊性测试仪(上海润普检测设备有限公司)测定镀层的可焊性。在d为1.7 mm的铜线上分别镀Ni-P和Ni-P-B合金镀层,利用可焊性测试仪对镀层的可焊性进行测试。其中,助焊剂为25%松香的乙醇溶液,焊料组成为Sn63Pb37。老化试验参照文献[9],采用4 h的蒸汽老化试验。
2 结果与讨论
2.1 络合剂对镀层成分及沉积速度的影响
甘氨酸是镀液中的主络合剂,起维持镀液稳定的作用。络合剂之所以能起到稳定镀液的作用,是因为络合剂与金属离子Ni2+形成了相对稳定的络合离子,提高了Ni2+的还原电位,使Ni2+只在较高的温度及催化剂存在的条件下才能被还原[10]。
图1为络合剂甘氨酸、乳酸对沉积速度和镀层中w(P)和w(B)的影响。从图1(a)中可以看出,随着ρ(甘氨酸)的提高,镀层中w(P)减少,w(B)增加,而沉积速度急剧下降,这是由于过量的络合剂抑制了镀液的沉积速度;但当ρ(甘氨酸)超过40 g/L后,沉积速度和镀层中w(B)、w(P)相对恒定。当ρ(甘氨酸)低于30 g/L,镀液极不稳定,当θ升至40℃时镀液出现浑浊,其原因是镀液中的Ni2+未完全被甘氨酸络合,游离的Ni2+极易被还原成金属单质,导致镀液失效。
乳酸是镀液的辅助络合剂,与主络合剂甘氨酸共同作用,稳定镀液,从图1(b)中可以看出,乳酸质量浓度对镀层各元素的质量分数影响较小。但乳酸的加入能够使镀层平整光亮[10],经实验观察,若ρ(乳酸)低于10 g/L时,镀层发黄,当ρ(乳酸)为20 g/L时,镀层外观光亮,沉积速度适中。

图1 络合剂对沉积速度和镀层中w(B)和w(P)的影响
溶液中甘氨酸与Ni2+的络合情况可以通过紫外-可见光谱(UV-via)来考察。如图 2所示,当pH=12.0时,甘氨酸在250~800 nm内没有吸收峰(曲线5),而 Ni2+的吸收峰位于407 nm处(曲线4)。在25 g/L的硫酸镍溶液中,ρ(甘氨酸)分别为30、35及40 g/L时,镀液的 UV-via谱线在363 nm处的峰高基本重合(曲线1、2、3),说明甘氨酸与Ni2+完全络合。
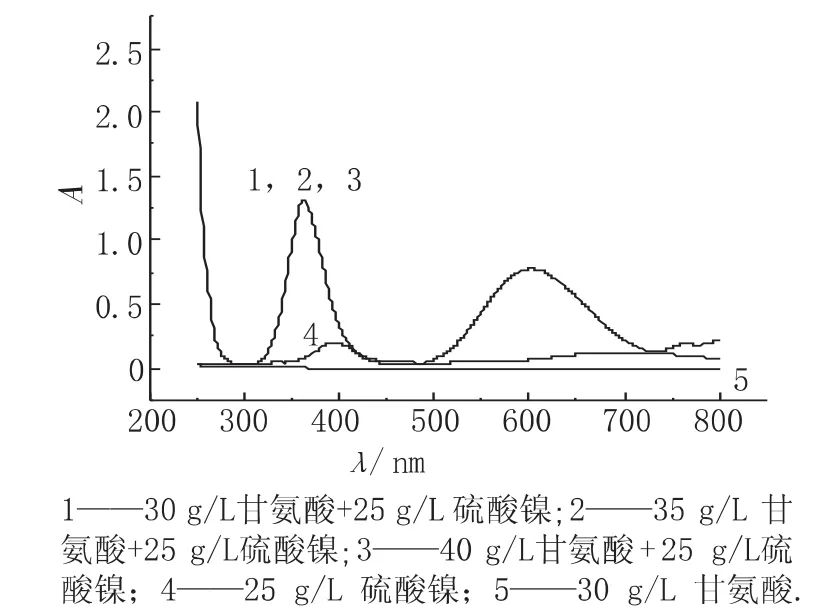
图2 镀液的UV-via光谱图
2.2 还原剂对镀层成分及沉积速度的影响
图3为还原剂KBH4和NaH2PO2对沉积速度和镀层中w(P)、w(B)的影响。随着 ρ(KBH4)从0.1 g/L提高到0.5 g/L,镀液的沉积速度呈下降趋势,与文献[11]一致。溶液中 ρ(KBH4)为 0.3~0.4 g/L时镀层中的 w(B)达到最大值为2%,若ρ(KBH4)继续增大,镀液中KBH4会加速分解,导致镀层中w(B)降低。

图3 还原剂对沉积速度和镀层中w(B)和w(P)的影响
由图3(b)可以看出,随着NaH2PO2质量浓度的提高,镀层中w(P)增大,而w(B)稍微减少;当ρ(NaH2PO2)为25 g/L时,沉积速度达到最大,此时ρ(Ni2+)∶ρ(H2PO2-)=0.40。若 ρ(NaH2PO2)<15 g/L时镀层发暗,沉积速度较低;ρ(NaH2PO2)>35 g/L,沉积速度下降,镀层中w(B)降低。
2.3 镀层表面形貌及结构表征
图4为Ni-P合金镀层和Ni-P-B合金镀层的SEM照片。在微观结构上,Ni-P-B合金镀层表面颗粒较Ni-P镀层均匀细密,这也为该镀层具有良好抗腐蚀性能提供了保证。从图4中可以看出,两种镀层表面均有许多馒头状凸起,这是由于在化学镀过程中伴随着催化核心的成核和生长过程。镀液中被还原的合金颗粒首先在铜基体表面的Pd原子附近发生吸附沉积,形成镀层的最基层。随着施镀时间的延长,这些催化核心开始长大并伴随着新的催化核心的形成。这些新老催化核心相互堆积,使镀层逐渐增厚;长大的催化核心向四周扩展,从而形成大面积的镀层。相邻催化核心由于竞争的扩展关系,形成了这些凸起。

图4 镀层的SEM照片
图5为采用NaH2PO2和KBH4为还原剂获得的Ni-P-B合金镀层经400℃1 h热处理后的XRD图谱。从图5中可以看出,未经热处理的镀层为无定形结构,呈现馒头峰。经400℃1 h热处理后,镀层由非晶结构转变为晶体结构,峰型变的尖锐。非晶态的表面结构使镀层表面组织中不存在晶界、位错、孪晶或者其它表面缺陷,使镀层具有较好的抗腐蚀性。

图5 Ni-P-B合金镀层的XRD图谱
2.4 镀层结合力、可焊性和耐蚀性测试
按照SJ1282-77标准中的弯曲法和划痕法对施镀20 min的Ni-P-B合金镀层进行结合力测试,镀层无翘起或剥落;用粘胶带反复对镀层进行剥离试验,镀层无脱落。测试结果表明镀层与基体结合力极强。
为了考察Ni-P-B合金镀层的可焊性,采用流布面积法(图6)和润湿法(图7)将该镀层与常规Ni-P合金镀层的可焊性进行了比较。经计算,Ni-P-B、Ni-P合金镀层的扩展率分别为89.88%和89.79%,即Ni-P-B合金镀层的可焊性略大于Ni-P合金镀层,试验结果表明,B元素的加入改善了镀层的可焊性能。从图6中也可以看出,经可焊性测试后,Ni-P合金镀层表面发黑并失去金属光泽,而Ni-P-B合金镀层变化不大,表明Ni-P-B合金镀层的抗变色能力强于Ni-P合金镀层。润湿法测试镀层可焊性表明,Ni-P合金镀层的润湿开始时间 tb=1.32 s,Ft1=1.6 mN,Ni-P-B 合金镀层的 tb=1.27 s,Ft1=2.08 mN,这与扩展率试验结果一致。从图7中还可以看出,镀层经4 h的蒸汽老化试验后,可焊性明显下降,原因是镀层的表面结构发生了破坏,镀层颜色变暗。

图6 镀层的可焊性流布面积图

图7 润湿法测定镀层可焊性曲线图
图8为在3.5%NaCl和0.5 mol/L H2SO4溶液中,室温条件下测得试片的极化曲线,由极化曲线拟合计算出腐蚀电位和腐蚀电流密度结果见表1。由极化曲线可以看出,Ni-P-B合金镀层在两种介质中的腐蚀电位都高于Ni-P合金镀层,腐蚀电流密度小于Ni-P合金镀层。可知,Ni-P-B合金镀层的抗腐蚀性能优于Ni-P合金镀层。
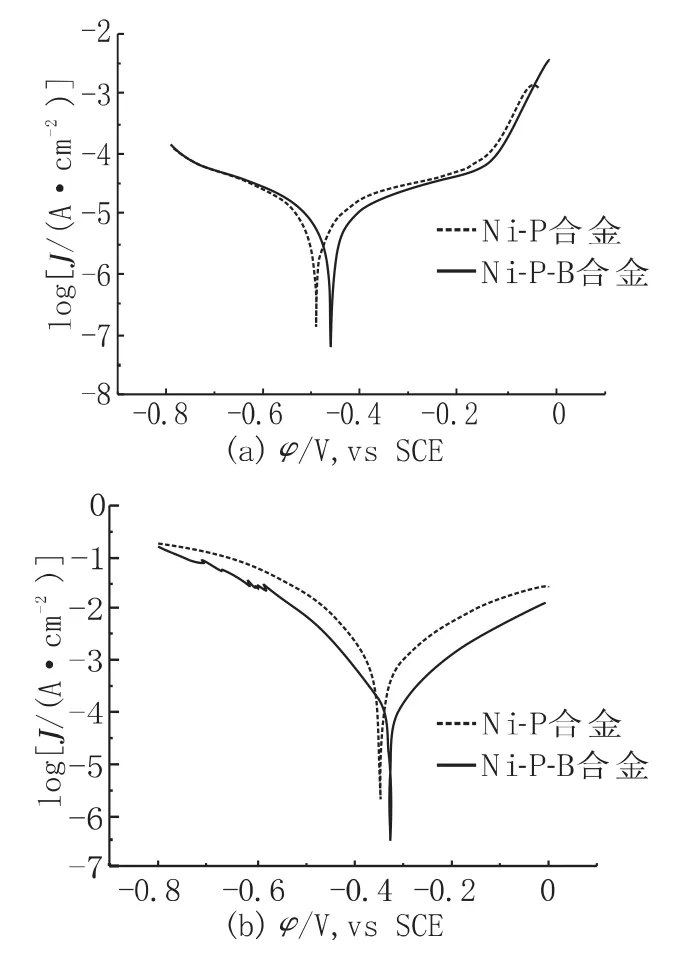
图8 极化曲线

表1 极化曲线测试结果
3 结论
1)通过分析各因素对沉积速度、镀层表观形貌、镀层成分及镀液稳定性的影响,确定化学镀Ni-P-B合金的最佳工艺配方及条件为:25 g/L NiSO4·6H2O,30 g/L NH2CH2COOH,20 g/L CH3CH(OH)COOH,25 g/L NaH2PO2,0.2 g/L KBH4,1 mg/L CdSO4·8H2O,pH=12,θ为69~71℃。镀层中 w(P)=8.99%,w(B)=1.14%,v=5.95 μm/h。该镀液具有较高的稳定性;通过对镀层性能的测试,表明Ni-P-B合金镀层的抗腐蚀性、可焊性均优于Ni-P合金镀层;剥离强度测试表明镀层与基体结合力极强。
2)提高镀液中甘氨酸、乳酸以及硼氢化钾的质量浓度均会降低镀层沉积速度,而ρ(NaH2PO2)在25 g/L时沉积速度最大。
[1]李乙翘,陈长生.印制电路[M].北京:化学工业出版社,2007:211-219.
[2]林金堵.SMT使PCB走上新一代产品[J].印制电路信息,2002,(01):12-15.
[3]El-Mallah A Talaat,Abbas M Hassib,Shafei M Farid,et al.Structure of electroless nickel deposits from baths containing sodium hypophosphite and potassium borohydride[J].Plating and Surface Finishing,1989,76(5):124-128.
[4]Mital C K,Shrvastava P B.Electroless nickel-phosphorous-boron alloy coatings[J].Metal Finishing,1986,84(10):67-70.
[5]Kaufman C M,Sen B.Hydrogen generation by hydrolysis of sodium tetrahydroborate:Effects of acids and transition metals and their salts[J].Journal of the Chemical Society,Dalton Transactions,1985,(2):307-313.
[6]Kreevoym M,Jacobson R W.The rate of decomposition of NaBH4in basic aqueous solutions[J].Ventron Alembic,1979,(15):2-3.
[7]GB/T 9491-202,锡焊用液态焊剂(松香型)[S].
[8]GB/T 2423.32-2008,电工电子产品环境试验,第2部分:试验方法,试验Ta:润湿称量法可焊性[S].
[9]GB/T 2423.28-2005,电工电子产品环境试验,第2部分:试验方法,试验T:锡焊[S].
[10]姜晓霞,沈伟.化学镀理论与实践[M].北京:国防工业出版社,2000:26-91.
[11]Boquan Jiang,Lin Xiao,Shufen Hu,et al.Optimization and kinetics of electroless Ni-P-B plating of quartz optical fiber[J].Optical Materials,2009,(31):1532-1539.
Study on Technology and Performance of Electroless Ni-P-B Alloy Coating on Copper Substrate
SHI Jian-hua,WANG Yu-rong,WANG Wen-chang,LIU Zhi-chao,CHEN Zhi-dong
(School of Petrochemical Engineering,Changzhou University,Changzhou 213164,China)
Ni-P-B alloy coating with outstanding quality was obtained by introducing trace boron into Ni-P alloy.The optimum processing formulation of electroless Ni-P-B alloy was determined[25 g/L NiSO4·6H2O,30 g/L NH2CH2COOH,20 g/L CH3CH(OH)COOH,25 g/L NaH2PO2,0.2 g/L KBH4,1 mg/L CdSO4·8H2O,pH=12,θ=69 ~71 ℃]by investigating the influences of complexing agent(NH2CH2COOH and CH3CH(OH)COOH)and reducer(NaH2PO2and KBH4)on plating rate and component concentration.Corrosion resistance,solderability and adhesive strength of the coating were also tested.Results showed that the Ni-P-B ternary alloy coating was of better corrosion-resistance,solderability and excellent bonding with copper substrate.
electroless plating;Ni-P-B alloy coating;solderability;corrosion resistance
TQ153.2
A
1001-3849(2012)02-0001-05
2011-05-27
