抗凝血灭鼠剂杀它仗的合成
2012-11-21程传杰
丁 薇, 程传杰
(1. 北京理工大学 生命科学学院,北京 100081; 2. 江西科技师范学院 化学化工学院,江西 南昌 330013)
3-{3-[4-(4-三氟甲基苄氧基)苯基]-1,2,3,4-四氢化萘基}-4-羟基香豆素(1),俗名杀它仗或氟鼠灵,是高效第二代抗凝血灭鼠剂之一,对各种鼠类,包括对其它抗凝血剂具有抗药性的鼠类均具有良好的防治作用[1,2]。目前,1在国内尚无工业生产[3],市售均为美国氰氨公司进口[4],迫切需要研究具有工业化生产价值的合成方法。
本文在文献[5,6]方法的基础上,以苯乙酰氯和苯甲醚为起始原料,经酰化、缩合、消除、水解、成环、脱保护、氢化还原等9步反应合成了1(Scheme 1),总收率8.4%,其结构经1H NMR和IR确证。
与文献方法相比,改进路线具有反应条件温和、操作简易、总收率高等优点,对1的工业化生产具有参考价值。
1 实验部分
1.1 仪器与试剂
XT-4A型显微熔点仪;Bruker Vance 400 MHz型核磁共振仪(CDCl3为溶剂,TMS为内标);Nicolet 360型红外光谱仪(KBr压片);FLASHEA 1112型元素分析仪。
所用试剂均为分析纯。
1.2 合成
(1) 对甲氧基苯基苄基甲酮(2)的合成
在反应瓶中加入无水AlCl386 g(640 mmol)和苯甲醚72 mL(670 mmol)的二氯甲烷(500 mL)溶液,搅拌下于0 ℃缓慢滴加苯乙酰氯85 mL(550 mmol),滴毕,于室温反应30 min;回流反应3 h。冷却至室温,倒入冷的 2 mol·L-1盐酸中,分液,有机相用无水硫酸镁干燥,减压浓缩得红色黏稠液体,冷冻,过滤,滤饼干燥得棕黄色晶体2 107.9 g,收率86.7%, m.p.102 ℃~105 ℃;1H NMRδ: 3.80(s, 3H, CH3), 4.02(s, 2H, CH2), 6.93(d,J=8.5 Hz, 2H, ArH), 7.05~7.18(m, 5H, ArH), 7.88(d,J=8.5 Hz, 2H, ArH); IRν: 3 420, 3 100, 3 011, 2 950, 1 679, 1 601, 1 514, 1 340, 1 267, 1 174, 1 031, 993, 835, 727, 696, 572 cm-1。
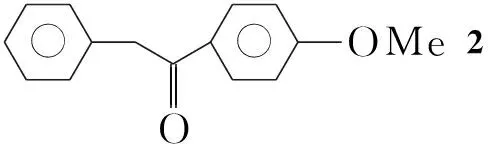
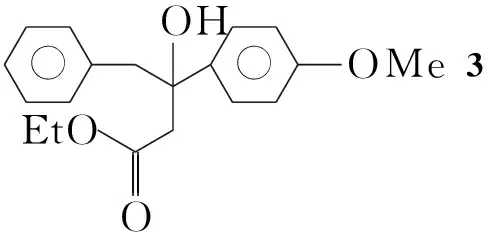
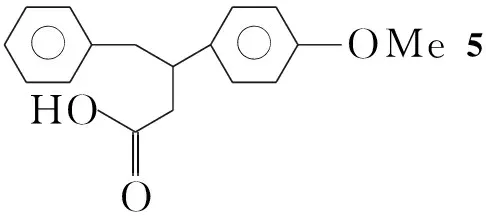
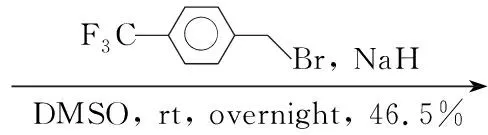

Scheme1
(2) 3-对甲氧基苯基-3-羟基-4-苯基丁酸乙酯(3)的合成
在反应瓶中依次加入294 g(420 mmol),锌粉30 g(460 mmol),碘0.6 g及苯500 mL,搅拌使其溶解;缓慢滴加溴乙酸乙酯50 mL(450 mmol),回流反应3 h。用10%硫酸(300 mL)中和,分液,有机相依次用10%NaHCO3溶液(300 mL),水洗涤,无水硫酸镁干燥,减压浓缩得黏稠物,用石油醚重结晶得淡黄色固体3 85.2 g,收率64.5%, m.p.46 ℃~49 ℃;1H NMRδ: 1.20(t,J=7.14 Hz, 3H, CH3), 2.87(d,J=8.50 Hz, 2H, CH2), 3.11(s, 2H, CH2), 3.73(s, 3H, CH3), 3.90(d,J=7.14 Hz, 2H, CH2), 4.62(s, 1H, OH), 6.70(d,J=8.79 Hz, 2H, ArH), 7.11(d,J=8.79 Hz, 7H, ArH); IRν: 3 480, 3 067, 3 041, 2 990, 2 933, 2 845, 1 742, 1 722, 1 675, 1 608, 1 515, 1 256, 1 184, 1 028, 837 cm-1。
(3) 3-苄基-3-对甲氧基苯基丙酸乙酯(4)的合成
在反应瓶中依次加入3 27.6 g(87.9 mmol),三乙基硅烷11.4 g(98.3 mmol),三氟乙酸40 g(350 mmol)及三氟化硼合乙醚0.32 mL,搅拌下回流反应8 h。用30%Na2CO3溶液(100 mL)中和,分液,有机相用水(3×30 mL)洗涤,无水硫酸镁干燥,减压浓缩得橙红色黏稠物4 25.2 g,收率96.2%;1H NMRδ: 1.30(t,J=7.4 Hz, 3H, CH3), 2.71(d,J=7.4 Hz, 2H, CH2), 3.01(d,J=7.4 Hz, 2H, CH2), 3.73(s, 3H, CH3), 3.92(d,J=7.4 Hz, 2H, CH2), 6.72(d,J=8.79 Hz, 2H, ArH), 7.05~7.21(d,J=8.79 Hz, 7H, ArH); IRν: 3 450, 3 000, 2 950, 1 732, 1 677, 1 599, 1 508, 1 453, 1 339, 1 276, 1 202, 1 170, 1 032 cm-1。
(4) 3-苄基-3-对甲氧基苯基丙酸(5)的合成
在反应瓶中加入425.2 g(84.6 mmol), NaOH 22 g(550 mmol)及水76 mL,搅拌使其溶解;回流反应8 h。冷却至室温,用苯(3×20 mL)萃取,水相用10%盐酸(300 mL)中和后,用二氯甲烷萃取;合并有机层,用无水硫酸镁干燥,减压浓缩得桔黄色固体,用乙酸乙酯重结晶得白色粉末5 15.2 g,收率64%, m.p.124 ℃~127 ℃;1H NMRδ: 2.49(m, 2H, CH2), 2.71(d,J=7.50 Hz, 1H, CH2), 3.09(d,J=7.50 Hz, 1H, CH), 3.70(s, 3H, CH3), 6.89(d,J=7.50 Hz, 2H, ArH), 7.02~7.21(m, 7H, ArH), 10.8(s, 1H, CO2H); IRν: 3 100, 2 988, 2 500, 1 701, 1 610, 1 516, 1 433, 1 245, 1 182, 1 032, 962, 824 cm-1。
(5) 3-对甲氧基苯基-1,2,3,4-四氢萘满酮(6)的合成
在反应瓶中加入多聚磷酸(PPA)18 g(53.3 mmol),搅拌下于80 ℃分批加入53.7 g(13.7 mmol),加毕,反应 2 h。用二氯甲烷(3×20 mL)萃取,合并有机相,依次用10%Na2CO3溶液,水洗涤,无水硫酸镁干燥,减压浓缩得棕黄色黏稠物,冷冻结晶后用甲醇重结晶得淡黄色粉末6 2.7 g,收率82.6%, m.p.101 ℃~103 ℃;1H NMRδ: 2.71(m, 2H, CH), 3.03(m, 3H, ArH), 3.80(s, 3H, CH3), 6.89(d,J=8.50 Hz, 2H, ArH), 7.02~7.45(m, 5H, ArH), 7.98(m, 1H, ArH); IRν: 3 200, 2 900, 1 677, 1 606, 1 508, 1 296, 1 253, 1 182, 1 032, 848, 769 cm-1。
(6) 3-对羟苯基-1,2,3,4-四氢萘满酮(7)的合成
在反应瓶中依次加入65.9 g(23.4 mmol),40%氢溴酸35 mL及冰乙酸45 mL,搅拌下回流反应8 h。减压浓缩后加入80 mL水稀释,用二氯甲烷(3×25 mL)萃取,合并有机相,依次用10%NaHCO3溶液,水洗涤,无水硫酸镁干燥,减压浓缩得土黄色固体,用乙酸乙酯重结晶得白色固体7 3.6 g,收率64.6%, m.p.194 ℃~195 ℃;1H NMRδ: 2.86(m, 2H, CH2), 3.15(m, 2H, CH2), 3.18(m, 1H, CH2), 4.95(s, 1H, OH), 6.85(d,J=7.42 Hz, 2H, ArH), 7.20(d,J=7.42 Hz, 1H, ArH), 7.25(d,J=7.42 Hz, 4H, ArH), 8.12(d,J=7.42 Hz, 1H, ArH); IRν: 3 390, 3 032, 2 934, 1 672, 1 601, 1 514, 1 454, 1 297, 1 221, 1 112, 1 019, 829, 770 cm-1。
(7) 3-(4-三氟甲基苄氧苯基-4-基)-1,2,3,4-四氢萘满酮(8)的合成
在反应瓶中加入NaH 0.2 g(8.33 mmol)和DMSO 20 mL,搅拌使其溶解;分批加入70.6 g(2.52 mmol),加毕,于室温反应3 h(溶液变黑);缓慢加入对三氟甲基溴苄1.0 g(3.13 mmol)的DMSO(10 mL)溶液,于室温搅拌反应过夜。减压浓缩,加水200 mL,过滤,滤饼真空干燥得咖啡色粉末8 0.4 g,收率46.5%;1H NMRδ: 2.57(s, 2H, CH2), 3.40(d,J=8.57 Hz, 2H, CH2), 4.90~5.2(s, 2H, OCH2), 5.78(d,J=8.57 Hz, 1H, ArH), 6.15(d,J=8.57 Hz, 1H, ArH), 6.4~7.2(m, 1H, ArH); IRν: 2 950, 2 350, 2 330, 1 608, 1 506, 1 413, 1 319, 1 158, 1 107, 1 060, 1 012, 821, 780, 592 cm-1。
(8) 3-(4-三氟甲基苄氧苯基-4-基)-1,2,3,4-四氢萘满醇(9)的合成
在反应瓶中加入82.5 g(6.33 mmol)和乙醇20 mL,于60 ℃搅拌使其溶解;分批加入NaBH40.6 g(15.9 mmol),加毕,反应 3 h。反应液用水稀释后,用10%盐酸调至pH 1~2,用二氯甲烷(3×25 mL)萃取,合并有机层,依次用碳酸氢钠溶液,水洗涤,无水硫酸镁干燥,减压浓缩得土黄色固体9 2.42 g,收率96%;1H NMRδ: 2.17(d,J=8.14 Hz, 2H, CH2), 2.96(d,J=8.14 Hz, 1H, CH2), 3.33(d,J=8.14 Hz, 2H, CH2), 4.45(d,J=8.14 Hz, 1H, OH), 4.68(m, 1H, CH), 5.20(s, 2H, OCH2), 6.85(m, 2H, ArH), 7.02~7.45(m, 6H, ArH), 7.42(m, 2H, ArH)。
(9) 1的合成
在反应瓶中加入4-羟基香豆素6.5 g(40 mmol),对甲苯磺酸(TsOH)1.9 g(11.05 mmol)和二氯乙烷(80 mL),搅拌使其溶解;升温至回流后,滴加98 g(20.15 mmol)的二氯乙烷(40 mL)溶液,滴毕,回流反应25 h,放置过夜。过滤,滤液浓缩至1/2,析出少量固体;过滤,滤液用水洗涤,无水硫酸镁干燥,减压浓缩得棕色固体;合并三次收集到的固体,用乙酸乙酯重结晶得灰白色粉末1 9.9 g,收率92.5%, m.p.160 ℃~165 ℃;1H NMRδ: 1.86(d,J=6.95 Hz, 2H, CH2), 2.51(d,J=6.95 Hz, 2H, CH2), 3.01(d,J=6.95 Hz, 1H, ArCH), 3.92(d,J=6.95 Hz, 2H, CH2), 5.10(s, 2H, OCH2), 6.85(m, 2H, ArH), 7.02~7.15(m, 11H, ArH), 7.42(m, 2H, ArH), 14.5(d,J=6.95 Hz, 1H, OH); Anal.calcd for C33H25O4F3: C 73.05, H 4.64; found C 73.10, H 4.63。
2 结果与讨论

表1 反应条件对1收率的影响*Table 1 Effect of reaction conditions on the yield of 1
*反应条件同1.2(9);r=n(4-羟基香豆素) ∶n(9);y=n(催化剂) ∶n(9);a甲磺酸;b苯磺酸,其余催化剂为TsOH
合成3的反应是Reformatskii反应,有两个重要因素:一是溴乙酸乙酯的滴加速度。由于溴代物比较活泼,滴加速度过快会发生两种可能的副反应,α-卤代羧酸酯的Wurtz缩合或两分子α-卤代羧酸酯自身缩合形成β-酮酸酯。其次,反应体系必须绝对无水。
合成1的反应是缩合反应,其影响因素见表1。从表1可以看出,r[n(4-羟基香豆素) ∶n(9)]是决定收率的关键因素。r=2时,收率最高。使用TsOH,苯磺酸和甲磺酸作为催化剂得到了相似的结果。
[1] Gill J R. Laboratory evaluation of the toxicity of flocoumafen as single-feed rodenticide to seven rodent species[J].Int Biodeterior Biodegrad,1992,44(1):15-20.
[2] 曹晓梅,郝连义. 杀它仗毒饵动物园灭鼠现场试验观察[J].医学动物防制,1998,14(6):20-21.
[3] 刘晓峰,孙媛媛,王毓芳,等. 高效灭鼠剂杀它仗的合成[J].精细化工,2000,17(1):39-41.
[4] Jung J C, Jang S, Oh S,etal. Simple synthesis and biological evaluation of flocoumafen and its structural isomers[J].J Chem Sci,2010,122(6):833-838.
[5] 冯流星,宋华付,丁绍民. 3-对甲氧基苯基-1,2,3,4-四氢-1-萘酚的合成[J].精细化工,2002,19(12):739-749.
[6] Oee Sook Park, Bong Suek Jang. Synthesis of 4-hydro xycoumarin derivatives-1:An efficient synthesis of flocoumafen[J].Arch.Pharm Res,1995,18(4):277-281.
