S2-控制剂对Ag纳米产物的形貌及光学性能的影响
2012-11-09邵桂雪李天保刘海瑞赵君芙许并社
邵桂雪 梁 建 李天保 刘海瑞 赵君芙 许并社*,
(1太原理工大学新材料界面科学与工程教育部重点实验室,太原 030024)
(2山西省新材料工程技术研究中心,太原 030024)
(3太原理工大学材料科学与工程学院,太原 030024)
S2-控制剂对Ag纳米产物的形貌及光学性能的影响
邵桂雪1,2,3梁 建1,2,3李天保1,2,3刘海瑞1,2,3赵君芙1,2,3许并社*,1,2,3
(1太原理工大学新材料界面科学与工程教育部重点实验室,太原 030024)
(2山西省新材料工程技术研究中心,太原 030024)
(3太原理工大学材料科学与工程学院,太原 030024)
采用改装的微波冷凝回流装置,以乙二醇作为还原剂和溶剂,在表面活性剂聚乙烯吡咯烷酮的保护下,添加Na2S与AgNO3反应生成Ag2S,对Ag2S进行热分解即可获得Ag纳米产物。保持其它参数(加热功率、加热时间、表面活性剂浓度和反应物溶液浓度等)不变的条件下,通过改变Na2S的浓度得到不同形貌的Ag纳米产物。利用扫描电子显微镜、X射线衍射仪和紫外-可见分析仪对所得Ag纳米产物的形貌、物相和光学性能进行分析表征,结果表明,在微波冷凝回流作用下,Na2S浓度的逐渐增大使银纳米产物经历了一个类球形-立方体-线形的形貌演变。此外,通过分析反应过程,对S2-如何影响Ag纳米产物的形貌及Ag纳米线的生长机理作了进一步研究探讨。
Ag纳米结构;微波法;冷凝回流
0 引 言
由于金属纳米晶体的优异性能及在催化、生物传感、电子、光子和传感器等设备中的各种应用,使金属纳米晶体成为近年来研究者广泛关注的热点之一[1-2]。然而,金属纳米晶体的性能主要依赖于其形貌和尺寸[3-4],这是因为金属纳米粒子的形状和尺寸直接决定了其化学、物理、电学、光学、磁性和催化等特性[5-9]。对于Ag纳米结构,控制其形貌可以优化化学传感器或提高表面增强拉曼散射(SERS)中的表面等离子共振及局部电场强度[10-12]。由于Ag纳米线有很高的导电性、热导率以及较好的光学性能,因而它在光偏振镜[13]、光子晶体[14]、催化剂[15]、表面增强拉曼散射(SERS)[10]、透明电极[16-17]和生物传感器[11-12]等许多应用领域中的有很重要的应用。此外,纳米Ag具有较高的抗菌性,可广泛应用于提高羊毛的抗菌性[18]。
对于如何获得可控的银纳米结构,首先需要考虑的是晶种的形貌与尺寸,因为两者均会对产物的最终形貌有很大影响。改变晶种的形貌及尺寸的通常方法有“引用外来晶种”、“晶种氧化蚀刻”、“添加控制剂”等。“引入外来晶种”是通过调节晶种制备过程来控制产物的形貌,是最早用于制备形貌可控的金属纳米材料的一种方法[19]。“晶种氧化刻蚀”即引入Cl-,在O2存在的条件下,通过Cl-/O2氧化蚀刻原理促进不同结构晶种之间的转变,以获得不同形貌的银纳米产物[20]。“添加控制剂”通常是在晶种初期成核过程中加入少量离子及有机分子(称为:控制剂)形成银盐胶体或改变银离子的还原速度,从而影响晶种初期成核过程[21]。“控制晶种”通常采用氢气作保护氛围,从而具有一定危险性和复杂性[21-22],“晶种氧化蚀刻”过程比较缓慢[23],而“引入控制剂”不仅实验过程简便、反应时间短,还有利于成核粒子的稳定,其离子或有机分子能吸附在晶种表面,降低其表面能,从而稳定和调节粒子尺寸[24]。
目前,用于制备Ag纳米结构的方法有多种,包括多元醇法[25]、微波辅助法[26]、水热法[27]、超声化学法[28]、电化学法[29]、模板法[30]等。然而,要实现高产量、高纯度、高分散性和大规模的商业生产,这些方法还需进一步改进和完善。对于制备金属纳米粒子,多元醇方法简便、灵活且成本低[31],但是要实现产物的高产量化,该方法的过程复杂且耗时[32]。由于微波加热速度极快,近年来微波辅助法在化学合成方面应用越来越多[33-34]。例如姚宝慧等[35]采用微波辐射硝酸银水溶液直接制备出了纳米银/PVP复合物。最近,Chen等将多元醇与微波加热结合起来,直接快速制备出了较纯Ag纳米立方体和纳米线[36]。尽管微波辅助多元醇方法反应时间短、简便,但是往往采用密闭反应[37],由于微波加热速度非常迅速且很难控制温度,反应溶液在短时间内达到沸腾,容易导致喷溅和爆炸,然而通过冷凝回流能使体系的温度和浓度恒定[38],提高了反应装置的安全性和可靠性。本研究在微波辅助多元醇的基础上,加入冷凝回流,以EG作为还原剂和溶剂,PVP为表面活性剂,Na2S为形貌控制剂,AgNO3为银源,通过改变Na2S浓度来制备合成不同形貌的Ag纳米产物,研究S2-对Ag纳米产物形貌的影响,并对Ag纳米线的形成机理进行初步探讨。
1 实验部分
研究所用的实验装置如图1所示:
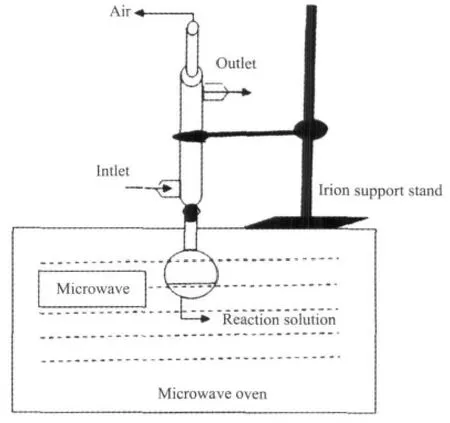
图1 改装的微波冷凝回流装置图Fig.1 Schematic diagram of modified microwave condensing reflux system
样品制备过程:本研究所采用的试剂均为分析纯。首先,分别将不同质量的Na2S加入到10 mL EG溶液中,使Na2S浓度分别为0 mol·L-1、0.5 mmol· L-1、1 mmol·L-1、1.5 mmol·L-1和2 mmol·L-1。随后,在磁力搅拌作用下分别加入一定量的PVP,使PVP的浓度均为114 mmol·L-1。此外,将一定量的AgNO3加入到10 mL EG溶液中,得到AgNO3浓度为94 mmol·L-1。
将不同浓度的Na2S/PVP/EG溶液依次通过蠕动泵(转速为40 rad·min-1)逐滴滴入到AgNO3/EG溶液中,其中AgNO3/EG溶液处于磁力搅拌作用下。由于在滴定过程中,Na2S与AgNO3反应生成Ag2S,所以溶液的颜色逐渐由无色变为黄色。随后将混合溶液移入微波炉中进行加热反应,以便得到Ag纳米产物。反应结束后,溶液在空气中冷却至室温,然后将其放入离心机中,分别采用丙酮、乙醇和去离子水,在转速为5000 r·min-1下离心,目的是为了除去溶液中剩余的EG和PVP。最后将获得的Ag纳米产品分散到乙醇中便于以后分析测试。
样品测试表征设备:XRD为Y-2000 Automated X-Ray Diffractometer,测试条件:Cu Kα射线 (λ= 0.154 18 nm),扫描速度0.05°·s-1,扫描范围20°~80°,以连续扫描方式收集数据;扫描电镜为JSM-6700型场发射扫描电镜。紫外-可见光谱分析(UVVisible spectrophotometer,UV-Vis)采用北京普析通用仪器有限责任公司生产的TU-1901型双光紫外-可见分光光度计分析仪,在装入乙醇的石英比色皿中滴加银纳米产物待测。
2 结果与讨论
图2是保持其它反应条件不变,改变Na2S的浓度进行试验所得Ag纳米产物的SEM图。由图2(a)可知,未加Na2S时,所得产物为形貌规则、尺寸均匀的类球形银纳米颗粒。平均晶粒尺寸约为90~100 nm。通过对应图3(a)的TEM图,可知,此过程所得银纳米颗粒含有孪晶十面体,通过其HRTEM可以很明显得观察出其5个孪晶界 (见白色箭头),对银纳米线的生长起到重要作用,其作用见生长机理部分。当加入0.5 mmol·L-1的Na2S时,出现了许多大小均匀的Ag纳米立方体,其平均晶粒尺寸约为80~90 nm,但也有极少部分的不规则的Ag纳米颗粒(如图2(b)),这表明了Na2S的浓度对其产物的最终形貌有着决定的作用。增大Na2S浓度到1 mmol· L-1时,发现银纳米立方体明显增多且形状规则,平均边长为70~80 nm左右,同时还发现了极少的银纳米棒 (见图2(c))。继续增大Na2S的浓度到1.5 mmol·L-1,可以发现立方体的数量明显减少,得到了形貌混合的Ag纳米产物(如图2(d)),其中包括纳米立方体、纳米棒、纳米线、纳米双椎体等,同时,从图2(d)中红色箭头所指的方向还可看出银纳米棒的头部和尾部为五角形。当Na2S的浓度增大到2 mmol· L-1,发现生成了大量的银纳米线(如图2(e))。银纳米线平均直径约为100 nm。其TEM图见图3(b),银纳米线的5个对称边都与[112]相一致[36]。同其他文献相比,例如Chen[36]或Liu[39]的研究组采用了微波辅助法快速制备,只得到了立方体和线或者棒和颗粒2种形貌,本研究采用的微波冷凝回流辅助多元醇法不仅能缩短反应时间,而且通过调整S2-、AgNO3和PVP三者浓度可以获得类球形、立方体和线等3种以上不同形貌的Ag纳米产物。图2(f)是图2(e)Ag纳米线的EDS谱图,从图中可以看出生成的产物主要为Ag,并没有发现Na和S,表明了Na2S的加入对控制银纳米产物的形貌起了主导作用。

图2 不同Na2S浓度下所得Ag样品的SEM图Fig.2 SEM images of silver samples prepared with different Na2S concentrations
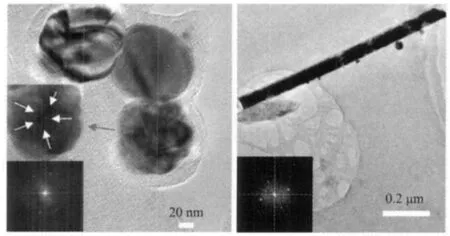
图3 (a)Ag纳米粒子的TEM图,插入部分为孪晶的HRTEM及FFT图;(b)Ag纳米线的TEM,插入部分为其FFT图Fig.3 (a)A TEM image and the corresponding FFT pattern and HRTEM as the insets,taken from Ag nanoparticles;(b)A TEM image and a corresponding FFT pattern (inset)taken from Ag nanowire
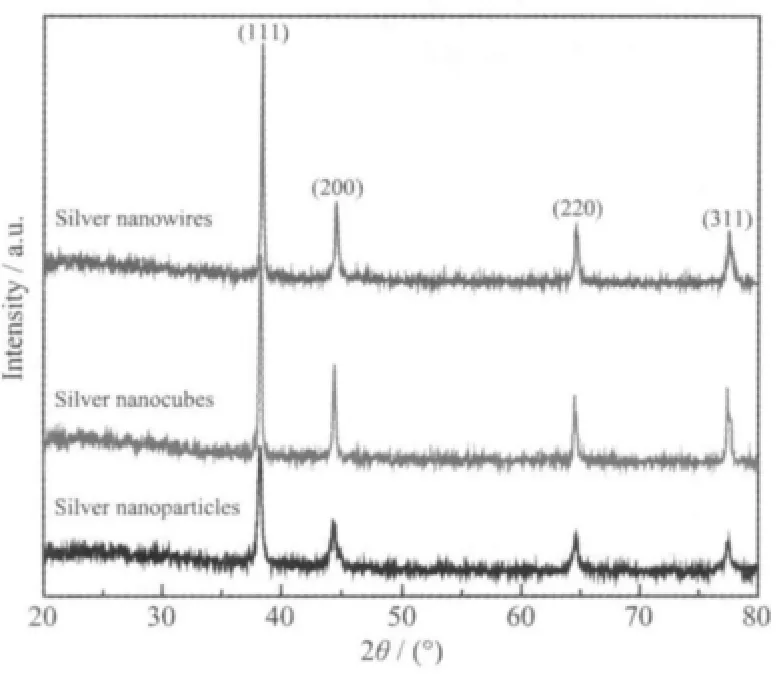
图4 不同形貌的Ag纳米产物的XRD图Fig.4 XRD patterns of Ag nanoproducts with different morphologies
图4显示的是微波功率为400 W,反应3 min、PVP浓度为 114 mmol·L-1和 AgNO3浓度为 94 mmol·L-1下得到的不同形貌的Ag纳米产物的XRD图。由图3可知,在38.1°、44.3°、64.4°、77.5°出现的衍射峰分别对应于Ag晶体的 (111)、(200)、(220)、(311)晶面,与粉末衍射卡片(PDF No.04-0783)的数据相一致,表明所得Ag纳米产物均为纯面心立方晶体结构。其中(111)面衍射峰最强,表明了Ag纳米产物均沿[111]方向上优先取向结晶。从图4还可以看出,未加Na2S所制备的Ag纳米颗粒的衍射峰最弱,衍射峰半峰宽相对较大,表明其颗粒的尺寸细小。随着添加Na2S的浓度依次增加,Ag纳米立方体和Ag纳米线衍射峰的强度逐渐增强,表明结晶强度逐渐增大,且衍射峰的峰形较尖锐、半峰宽小,均表明微波冷凝回流辅助多元醇法制备所得的Ag产物具有很高的结晶度。尽管在最初阶段有Ag2S(根据最初滴定时颜色由无色变为黄色判定)形成,但是并未发现Ag2S的衍射峰 (PDF No.76-0134),表明Ag2S只是在最初阶段形成,随后因释放出Ag+而分解,从而缓解Ag+的减少量[36]。实验结果表明,Na2S浓度的增大只是改变了Ag纳米产物的形貌,并不改变其晶体结构。
银纳米结构的紫外-可见吸收光谱强烈的依赖于银纳米产物的形状和尺寸[40-41],且UV-Vis吸收光谱是分析界面现象和描述银纳米粒子的演变的一个重要工具[42-43]。图5(a)为不同形貌银纳米产物的紫外-可见吸收光谱。所有样品均在大约320 nm左右出现了凹峰,其峰为银的带间吸收峰[44]。从图中看出,对于银纳米粒子来说,在492 nm处发现最强吸收峰,该峰被认为是等离子体共振(SPR)峰。早期的实验和理论表明银纳米立方体的3个表面等离子体共振(SPR)峰位于350 nm,390 nm,470 nm,其中最大的峰(470 nm)是由于两级电荷分布导致的等离子共振,而其他2个峰则是由于较高的多级电荷分布激发导致而形成的[45]。而银纳米线的SPR峰位于350 nm和380 nm处,主要是由于含有五边形截面的一维产物的横向模式,符合平面外的四级共振及两级共振模式[46-47]。此外,银纳米线吸收峰的波长在400 nm以后,吸收峰的强度下降很少,是因为银纳米线在445 nm及514 nm的平面四级与两级共振重叠所致[45]。在近红外这么宽的吸收决定了由银纳米线制备的电极可被广泛应用于红外太阳能电池[18]。图5(b)是最强SPR峰值与Na2S浓度的关系曲线。从图中可以看出,当Na2S浓度从0到0.5 mmol· L-1时,发现SPR峰的最大值由492 nm转变为506 nm,产生这种现象的原因是由于所得产物的形貌改变所致。而当Na2S浓度从0.5到1.0 mmol·L-1时,形貌主要是银纳米立方体,其平均尺寸由80~90 nm降到70~80 nm,且SPR峰最大值发生了蓝移,表明了银纳米立方体的尺寸随Na2S浓度增大而变小。根据该变化规律,当Na2S的浓度继续增大到1.5 mmol·L-1时,银纳米产物的生成速度放缓,其形貌从单一的立方体变成立方体与棒状物的多元形貌混合物;当浓度达到2 mmol·L-1就生成了银纳米线,其最强吸收峰为388 nm。
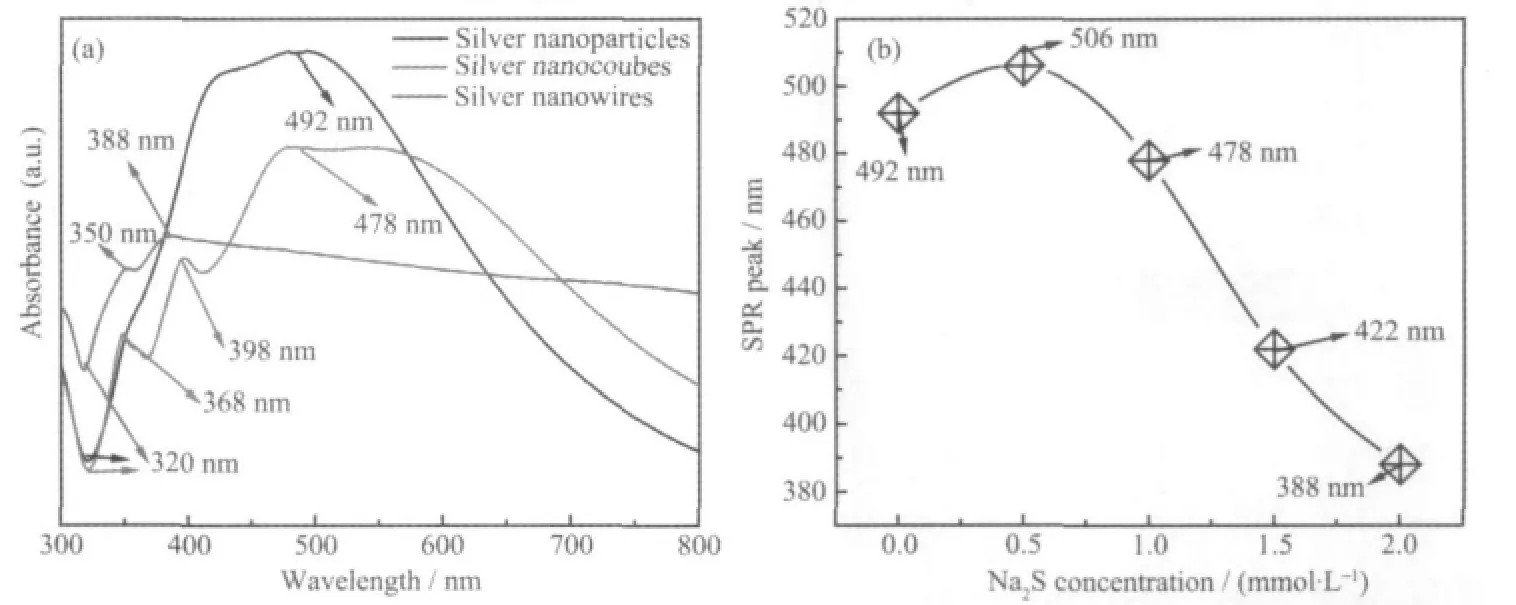
图5 (a)不同形貌银纳米产物的紫外-可见吸收光谱;(b)银样品最强SPR峰与Na2S浓度的关系曲线Fig.5 (a)UV-Visible absorption spectra of silver samples with different morphologies; (b)Relationship between the strongest SPR peak of silver samples and Na2S concentrations
3 形貌演变过程及形成机理
3.1 银纳米产物形貌的演变过程
在表面活性剂PVP的保护和辅助作用下,由于添加Na2S后,S2-与Ag+反应生成Ag2S,减少了Ag+自由离子的浓度,从而对Ag纳米产物的生长起到了缓冲作用。根据Nernst方程,Ag+的浓度降低导致了Ag+/Ag0电极阴极移动,减缓了Ag0的形成[48],从而促进了Ag纳米线的生长。图6为Na2S的浓度与Ag纳米产物形貌的演变过程图解。从图中可以看出,随着Na2S浓度的增加,Ag纳米产物的形貌经历了一个由类球形到立方体再到线的演变过程。即未加Na2S时,所得银纳米产物为类球形纳米颗粒,由于微波辐射加热迅速,在局部产生的高温将导致生成过度饱和的银纳米晶核。根据Ostwald Ripening过程,这些过度饱和的晶核在PVP的存在下迅速长大,从而生成尺寸均匀的银纳米颗粒,此方法可用于快速制备大量尺寸均匀的银纳米颗粒。当加入Na2S浓度较低时,容易形成大量的银纳米立方体,主要是因为初期形成的Ag2S浓度比较低,且Ag2S为窄带系n型半导体,在还原银时起显著的晶种催化作用[49],从而促进银纳米立方体的形成。而当Na2S浓度较高时,则容易产生大量的Ag纳米线。这是由于初期形成高浓度的Ag2S,减少了自由Ag+的浓度,对最初Ag晶种的形成起到了一个控制剂的作用,从而促进了Ag纳米线的形成。由此可见,在表面活性剂PVP的保护和辅助作用下,通过控制Na2S的浓度,可以用来制备不同形貌的Ag纳米产物。
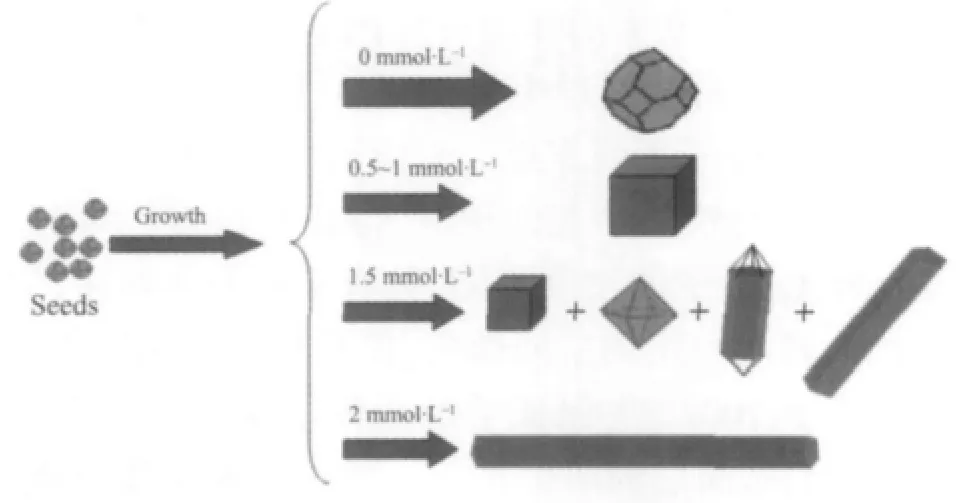
图6 Na2S浓度对银纳米产物形貌的影响变化示意图Fig.6 Schematic illustration of the shape evolution process of Ag nanocrystals as a function of the Na2S concentrations
3.2 银纳米线的形成机理
图7给出了整个Ag纳米线形成的生长机理示意图。主要包含以下几部分:(1)还原银离子。根据Fie′vet[31]最初提出的反应原理,由于EG在反应中既是溶剂也是还原剂,所以EG在高温下脱水生成乙醛,然后乙醛将Ag+还原成Ag0,反应过程如下:
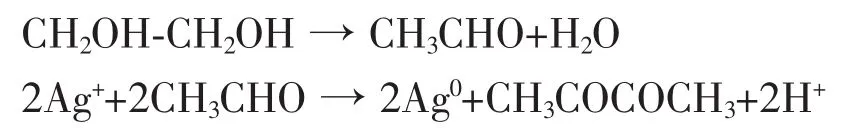
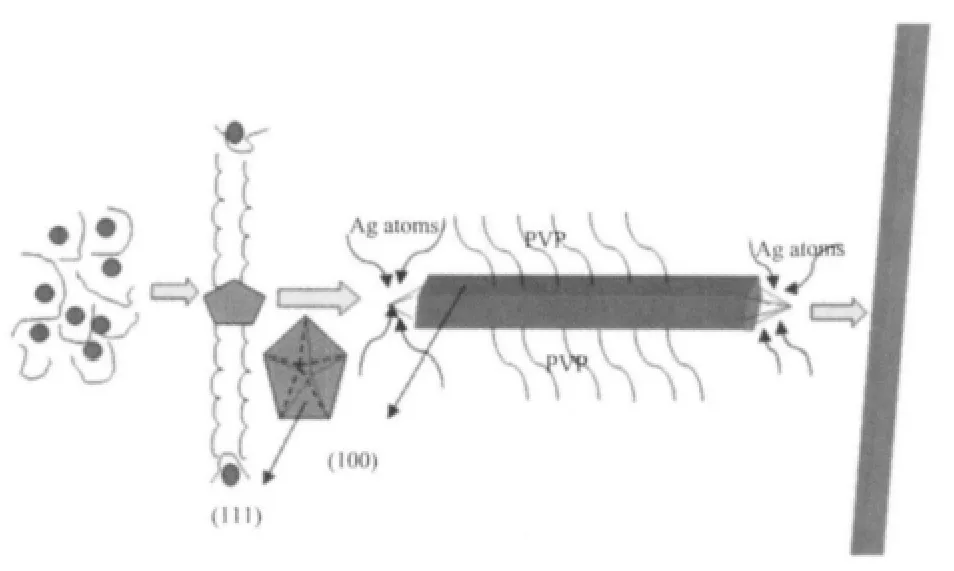
图7 Ag纳米线的生长机理Fig.7 Proposed mechanism for the formation of Ag nanowires
(2)孪晶十面体晶种(MTPs)的形成。PVP的吸附不仅使银表面{100}晶面钝化,同时也是孪晶十面体晶种(MTPs)形成的驱动力[25]。反应最初阶段形成的MTPs有5个对称折痕且其表面围绕着{111}。形成稳定晶核后的MTPs必然长大,晶核长大过程是液相内原子不断向晶核表面迁移,固液-界面向液相推移的过程。从热力学考虑晶体长大过程中应该始终保持界面能的最低能态,所以MTPs在Ostwald Ripening过程中容易产生十面体粒子,由于角度缺口或锲板边度旋7.5°产生孪晶晶界[45]。这种孪晶十面体晶种对于控制纳米线的直径以及纳米线的轴向生长起到非常大的作用。(3)PVP的辅助作用。在Ostwald Ripening过程中,由于孪晶边界有很高的能量,吸引银原子不断靠近。表面活性剂PVP中其链上的C=O与银晶体表面形成Ag-O配位键,不同晶面上的Ag原子的密度不同,具有不同的表面能,加上PVP具有一定的空间效应,使其对于(111)的相互作用弱于(100)[50-51],保证了纳米棒或纳米线沿着晶体的(111)晶面呈轴向生长。一旦纳米棒或线形成,由于PVP强烈地吸附在Ag晶体的(100)面,抑制了Ag在(100)面上的生长,从而促使线性晶种快速长成纳米棒或纳米线。
4 结 论
为了提高微波反应装置的安全性和可靠性,本研究在微波加热的基础上加装了冷凝回流装置,该反应体系同传统的微波辅助装置和传统的加热装置相比,装置简便安全,体系温度恒定,适应于制备各种纳米产物。通过添加Na2S,在改进的体系装置中采用辅助多元醇法成功的制备出了不同形貌的银纳米产物。在微波冷凝回流作用下,通过改变Na2S浓度,发现Na2S的浓度对于Ag纳米产物的形貌有着密切的相关性,即随着Na2S浓度的增大,Ag纳米产物经历了一个由类球形-立方体-线形的形貌演变过程。通过分析反应过程,对S2-如何影响Ag纳米产物的形貌以及Ag纳米线的生长机理作了进一步研究探讨。
[1]Daniel M C,Astruc D.Chem.Rev.,2004,104(1):293-346
[2]Rosi N L,Mirkin C A.Chem.Rev.,2005,105(4):1547-1562
[3]Burda C,Chen X B,Narayanan R,et al.Chem.Rev.,2005, 105(4):1025-1102
[4]Kelly K L,Coronado E,Zhao L L,et al.J.Phys.Chem.B, 2003,107(3):668-677
[5]Xia Y N,Yang P D,Sun Y G,et al.Adv.Mater.,2003,15 (5):353-389
[6]Salzemann C,Lisiecki I,Brioude A,et al.J.Phys.Chem.B, 2004,108(35):13242-13248
[7]Jana N R,Gearheart L,Obare S O,et al.Langmuir.,2002, 18(3):922-927
[8]Puntes V F,Krishnan K M,Alivisatos A P.Sci.,2001,291 (5511):2115-2117
[9]Wang Z L,Ahmad T S,El-Sayed M A.Surf.Sci.,1997,380 (2/3):302-310
[10]Cao Y W,Jin R C,Mirkin C A.Science,2002,297(5586): 1536-1540
[11]Haes A J,Van Duyne R P.J.Am.Chem.Soc.,2002,124 (35):10596-10604
[12]Wang H C,Wang X S,Zhang X Q,et al.Biosens.Bioelectron., 2009,25(1):142-146
[13]Pang Y T,Meng G W,Fang Q,et al.Nanotechnology,2003, 14(1):20-24
[14]Hu X,Chan C T.Appl.Phys.Lett.,2004,85(9):1520-1522
[15]Chimentao R J,Kirm I,Medina F,et al.Chem.Commun., 2004(7):846-847
[16]Hu L B,Kim H S,Lee J Y,et al.Nano Lett.,2010,4(5): 2955-2963
[17]Lee J Y,Connor S T,Cui Y,et al.Nano Lett.,2010,10(4): 1276-1279
[18]Rai M,Yadav A,Gade A.Biotechnology Advances,2009,27 (1):76-83
[19]Wile B,Sun Y,Mayers B,et al.Chem.Eur.J.,2005,11(2): 454-463
[20]Wiley B,Herricks T,Sun Y,et al.Nano Lett.,2004,4(9): 1733-1739
[21]CHEN Chang(陈昌).Thesis for the Master of Zhejiang University(浙江大学硕士论文).2006.
[22]Chen C,Wang L,Jiang G,et al.Nanotechnology,2006,17 (2):466-474
[23]Im S,Lee Y T,Wiley B,et al.Angew Chem.Int.Ed.,2005, 44:2154-2157
[24]Lin S,Tsai Y,Chen C,et al.J.Phys.Chem.B,2004,108(7): 2134-2139
[25]Sun Y G,Mayers B,Herricks T,et al.Nano Lett.,2003,3 (7):955-960
[26]Liu F K,Ko F H,Huang P W,et al.J.Cryst.Growth,2005, 273(3/4):439-445
[27]Becker R,Söderlind F,Liedberg B,et al.Mater.Lett.,2010, 64(8):956-958
[28]SHAO Li(邵 丽),WANG Xi-Kui(王西奎),GUO Wei-Lin(国伟林),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao), 2007,23(10):1824-1828
[29]Zhu J J,Liao X H,Zhao X N,et al.Mater.Lett.,2001,49 (2):91-95
[30]ZHANG Xiao-Guang(张晓光),YUAN Zhi-Hao(袁志好),XU Li-Ping(徐丽萍).Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2006,22(10):1916-1920
[31]Fievet F,Lagier J P,Figlarz M.MRS Bull.,1989,14:29-34
[32]Li C C,Shuford K L,Chen M H,et al.Nano Lett.,2008,2 (9):1760-1769
[33]Komarneni S,Li D S,Newalkar B,et al.Langmuir,2002,18 (15):5959-5962
[34]Zhu J J,Palchik O,Chen S G,et al.J.Phys.Chem.B, 2000,104(31):7344-7347
[35]YAO Bao-Hui(姚宝慧),XU Guo-Cai(徐国财),ZHANG Hong-Yan(张宏艳),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2010,26(9):1629-1632
[36]Chen D P,Qiao X L,Qiu X L,et al.Nanotechnology,2010, 21(2):1-7
[37]Nadagouda M N,Varma R S.Cryst.Growth Des.,2008,8(1): 291-295
[38]FU Min(付敏),JIANG Zhi-Dong(江志东),MA Zi-Feng(马紫峰),et al.Chinese J.Inorg.Materials(Wuji Cailiao Xuebao), 2005,20(4):808-814
[39]Liu F K,Huang P W,Chang Y C,et al.J.Mater.Res., 2004,19(2):469-473
[40]Mock J J,Barbic M,Smith D R,et al.J.Chem.Phys., 2002,116(15):6755-6760
[41]Wiley B J,Im S H,Li Z Y,et al.J.Phys.Chem.B,2006, 110(32):15666-15675
[42]Sosa I O,Noguez C,Barrera R G.J.Phys.Chem.B,2003, 107(26):6269-6275
[43]Slistan-Grijalva A,Herrera-Urbina R,Rivas-Silva J F,et al. Physica E,2005,25(4):438-448
[44]Henglein A.J.Phys.Chem.,1993,97(21):5457-5471
[45]Marks L D.Rep.Prog Phys,1994,57(6):603-649
[46]Gao Y,Jiang P,Song L,et al.J.Phys.D:Appl.Phys.,2005, 38(7):1061-1067
[47]Gao Y,Song L,Jiang P,et al.J.Cryst.Growth,2005,276(3/ 4):606-612
[48]Yu D B,Yam V W W.J.Phys.Chem.B,2005,109(12): 5497-5503
[49]Kryukov A I,Stroyuk A L,Zin′chuk N N,et al.Journal of Molecular Catalysis A:Chemical,2004,221(1/2):209-221
[50]Huang H H,Ni X P,Loy G L,et al.Langmuir,1996,12(4): 909-912
[51]Bonet F,Tekaia-Elhsissen K,Sarathy K V.Bull.Mater.Sci., 2000,23(3):165-168
Effects of Sulfur Ion on Morphology and Optical Properties of Silver Nano-Products
SHAO Gui-Xue1,2,3LIANG Jian1,2,3LI Tian-Bao1,2,3LIU Hai-Rui1,2,3ZHAO Jun-Fu1,2,3XU Bing-She*,1,2,3
(1Key Laboratory of Interface Science and Engineering in Advanced Materials
(Taiyuan University of Technology),Ministry of Education,Taiyuan030024,China)
(2Shanxi Research Center of Advanced Materials Science and Technology,Taiyuan030024,China)
(3College of Material Science and Technology,Tiyuan University of Technology,Taiyuan 030024,China)
Silver nanostructures were synthesized by decomposing silver sulfide via a modified microwave condensing reflux method by adding sodium sulfide (Na2S)in the presence of polyvinyl pyrrolidone (PVP)as protecting agent and ethylene glycol(EG)as reductant and solvent.The different morphologies of silver nanoproducts were obtained through changing the concentration of Na2S under the constant parameters such as: heating power,reaction time,surfactant,and reagent concentration.The morphology,crystalline phase,and optical property of the samples were examined by SEM,XRD,and UV-Visible spectrophotometer.The results show that the silver nanoproducts have gone through a spherical-cube-linear evolution in the morphology with gradually increasing Na2S concentration.In addition,the effect of S2-on the morphology of silver nanoproducts and the formation mechanism of silver nanowires are further discussed by analyzing the reaction process and the results obtained in this study.
silver nanostructure;microwave method;condensing reflux
TG146.3;O614.122
A
1001-4861(2012)01-0055-07
2011-06-27。收修改稿日期:2011-08-05。
国家自然科学基金(No.51002102)和山西省回国留学人员重点科研(2009-03)资助项目。*
。E-mail:xubs@tyut.edu.cn,Tel:(0351)6011311;会员登记号:E63080002GJ。
猜你喜欢
杂志排行
无机化学学报的其它文章
- 碳酸盐共沉淀法制备Li[Li0.2Co0.13Ni0.13Mn0.54]O2中加料方式对产物性能的影响
- Sonochemical Synthesis of Different Morphological CaF2Microstructures
- Synthesis,Crystal Structure and Properties of a Manganese(Ⅱ)Complex with an Asymmetrical Substituted Triaryltriazole
- Syntheses and Crystal Structures of Nickeand CopperComplexes with Schiff Base Ligand of 5-Chlorosalicylaldehyde
- Hydrothermal Synthesis,Crystal Structure and Catalytic Properties of a Polyoxovanadate Organicamine
- Tumor-Imaging Core-Shell Nano-Models for Catalase
