高速逆流色谱法分离野马追乙酸乙酯萃取物中三种倍半萜烯内酯
2012-11-08鄢贵龙纪丽莲罗玉明胡永红
鄢贵龙, 纪丽莲, 罗玉明, 胡永红
(1.淮阴师范学院 江苏省生物质能与酶技术重点实验室, 江苏 淮安 223300;2.淮阴师范学院 江苏省环洪泽湖生态农业生物技术重点实验室, 江苏 淮安 223300;3.南京工业大学 生物与制药工程学院, 江苏 南京 210009)
高速逆流色谱法分离野马追乙酸乙酯萃取物中三种倍半萜烯内酯
鄢贵龙1,2,3, 纪丽莲2, 罗玉明2, 胡永红3
(1.淮阴师范学院 江苏省生物质能与酶技术重点实验室, 江苏 淮安 223300;2.淮阴师范学院 江苏省环洪泽湖生态农业生物技术重点实验室, 江苏 淮安 223300;3.南京工业大学 生物与制药工程学院, 江苏 南京 210009)
建立了应用高速逆流色谱(HSCCC)从野马追乙酸乙酯萃取物中分离纯化3种倍半萜烯内酯的方法.采用正己烷-乙酸乙酯-甲醇-水(1∶4∶2∶3)作为两相溶剂体系,从900mg野马追乙酸乙酯萃取物中分离得到3β-Hydroxy-8β-[4′-hydroxytigloyloxy]-costunolide 6.5mg,野马追内酯A28.5mg和野马追内酯B29.3mg,其纯度分别为92.5%,91.7%和93.9%.3种化合物的结构通过ESI-MS和1H NMR进行了鉴定.
野马追; 高速逆流色谱; 倍半萜烯内酯; 分离
0 引言
野马追为菊科泽兰属植物轮叶泽兰(EupatoriumlindleyanumDC.)的干燥地上部分,味苦,性平,有清肺止咳、化痰平喘、抗菌消炎、利尿消肿、抗氧化等功效,临床常用于治疗气管炎、高血压等病[1-3].植物化学研究[4-9]表明野马追中含有黄酮类、生物碱类、香豆素类、酯类和萜类等成分.药理学研究表明野马追中分离的一些倍半萜内酯具有抗癌等活性[7],说明其中萜类可能是野马追中重要的活性成分之一.而这些萜类具有相似结构,依靠传统的柱色谱方法分离,不仅收率低、耗时,而且消耗大量试剂.为此,建立一种大量且快速有效地从野马追中分离纯化萜类成分的方法成为研发这些萜类所需急待解决的问题.
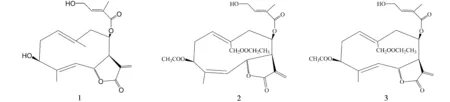
图1 三种倍半萜烯内酯化学结构
高速逆流色谱(High-speed countercurrent chromatography, HSCCC)是一种液-液分配色谱技术,利用样品在两相中分配系数的不同实现分离.HSCCC具有简单易行、制备量大、重现性好、无需固相载体、无不可逆吸附等特点[10],被广泛应用于天然活性成分的制备分离[10-13].本实验首次建立了从野马追乙酸乙酯萃取物中分离3种倍半萜烯内酯的高速逆流色谱制备方法,并采用ESI-MS、NMR等技术对所得单体的结构进行鉴定,其化学结构见图1.
1 材料和方法
1.1 材料与试剂
野马追:采购于江苏盱眙王店乡;乙腈(色谱纯,江苏汉邦公司);其他试剂均为分析纯.
1.2 主要仪器
TBE-300A型高速逆流色谱仪(上海同田生化技术有限公司);Inifinte 1260高效液相色谱(美国安捷伦公司);LCQ Advantage质谱仪(美国菲尼根公司);Avavce 400核磁共振仪(瑞士布鲁克公司).
1.3 样品的制备
自然干燥的野马追(10.0kg)粉碎后用100L95%的乙醇于室温下浸泡3天,过滤,收集滤液,滤渣重复浸泡4次.合并滤液并减压浓缩,获得乙醇提取物765.3g.所得醇提物先用水混悬,然后分别用石油醚、乙酸乙酯、正丁醇萃取,其中获得乙酸乙酯萃取物(EF)为121.50g,下面分离即以乙酸乙酯萃取物为离对象.样品置冰箱中保存备用.
1.4 溶剂系统的选择
溶剂系统的选择主要根据目标物的分配系数进行确定,称取6mg左右野马追乙酸乙酯萃取物溶于5mL具塞试管中,分别加入按一定比例混合并已经达到平衡的正己烷-乙酸乙酯-甲醇-水体系上、下相各1mL,充分震荡使样品溶解并达到分配平衡,静置,然后上下相各取0.5mL真空浓缩干燥,用1mL甲醇溶解,HPLC分别测定目标化合物在两相中的峰面积,计算分配系数K,即个目标成分在上相中的峰面与在下相中峰面积之比值,根据分配系数选择适宜的溶剂体系.
1.5 HSCCC分离纯化方法
以正己烷-乙酸乙酯-甲醇-水(1∶2∶1∶2)配制溶剂体系,于分液漏斗中将溶剂充分震荡混匀,使两相达到平衡,静置分为两相,其中,上相作为固定相,下相作为流动相.然后将两相溶剂系统中已超声脱气的上相以20mL/min的速度泵入HSCCC分离管中,待上相充满整个分离管后,调节主机转速至900rpm,正转,柱温30℃,同时以2.0mL/min的速度泵入下相,待两相达到动态平衡后,称取900mg左右野马追乙酸乙酯萃取物用5mL上相和5mL下相溶解,由进样阀注入分离管中,同时于254nm开始采集数据,按照色谱峰收集目标成分.
1.6 HPLC分析条件
色谱柱:XDB-C18 (100mm×4.6mm I.D., 3μm);流动相:含0.4%磷酸水(A)-乙腈(B),梯度洗脱程序:0~10min,10%~20%B,10~35min,20%~27%B,35~45min,27%~35%B,45~50min,35%~10%B;流速1.0mL/min,检测波长254nm,柱温:30℃,进样量:25μL.
2 结果与讨论
2.1 HSCCC溶剂体系的选择
在应用HSCCC进行分离时,溶剂系统的选择是最为关键部分.而选择溶剂系统时,其主要选择的依据即是目标组分在溶剂体系中的分配系数K,一般来说K值在0.5~2之间较好,同时要求溶剂系统分相速度快、对样品的溶解度大以及有足够高的固定相保留率.跟据所分离样品的性质,实验测定了正己烷-乙酸乙酯-甲醇-水在不同比例下对所分离3种倍半萜烯内酯的分配系数,结果见表1.从表1中可以看出当溶剂体系为正己烷-乙酸乙酯-甲醇-水(1∶1∶1∶1)时,各目标成分的分配系数过小,组分就容易与无保留的杂质一起出峰,并且出峰过快影响分离度,因此体系极性过弱而不适合此类成分的分离纯化.而当体系为正己烷-乙酸乙酯-甲醇-水(2∶5∶2∶5)时,化合物2和3的分配系数过大,将极大地延长出峰时间,同时会使峰展宽.当体系为正己烷-乙酸乙酯-甲醇-水(1∶2∶1∶2)时,各目标化合物的分配系数较好,且分离度均较合理.经HSCCC上机验证,最终选择正己烷-乙酸乙酯-甲醇-水(1∶2∶1∶2)为分离的溶剂体系.
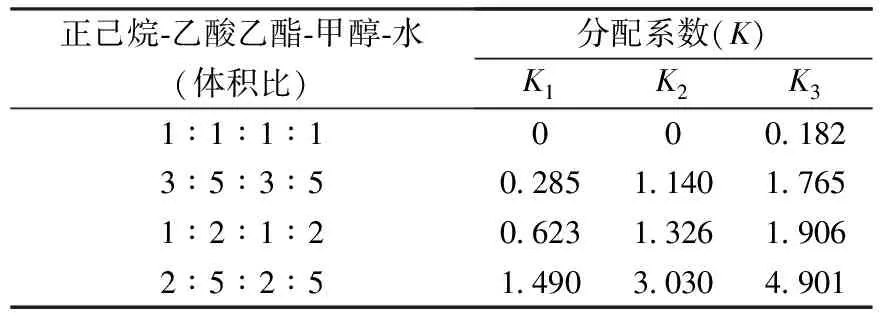
表1 不同溶剂体系中各化合物的分配系数
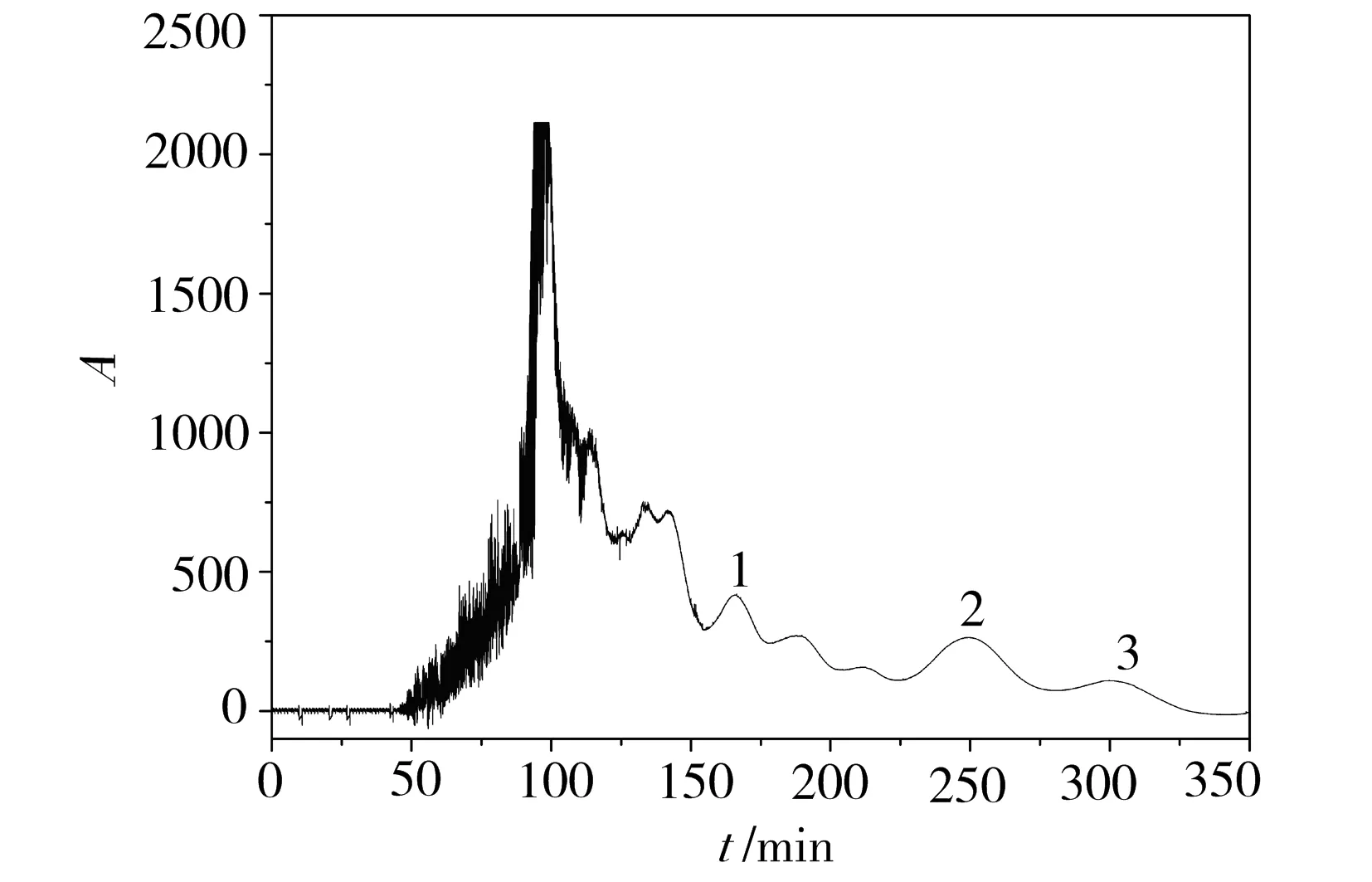
图2 野马追乙酸乙酯提取物HSCCC色谱图
2.2 HSCCC分离纯化结果
以正己烷-乙酸乙酯-甲醇-水(1∶2∶1∶2)为溶剂体系,固定相保留率为70%,分离时间为350min,对野马追乙酸乙酯萃取物进行HSCCC分离,分离色谱图见图2.将3个收集馏分减压浓缩干燥,从9000mg野马追丁醇提取物中分别得到6.5mg化合物1,28.5mg化合物2和29.3mg化合物3,对粗提物及化合物1~3分别进行HPLC检测(见图3),以面积归一化法测定其纯度分别为:92.5%,91.7%和93.9%.结果表明,利用高速逆流色谱可以对野马追中的有效成分物进行快速大量地分离制备.
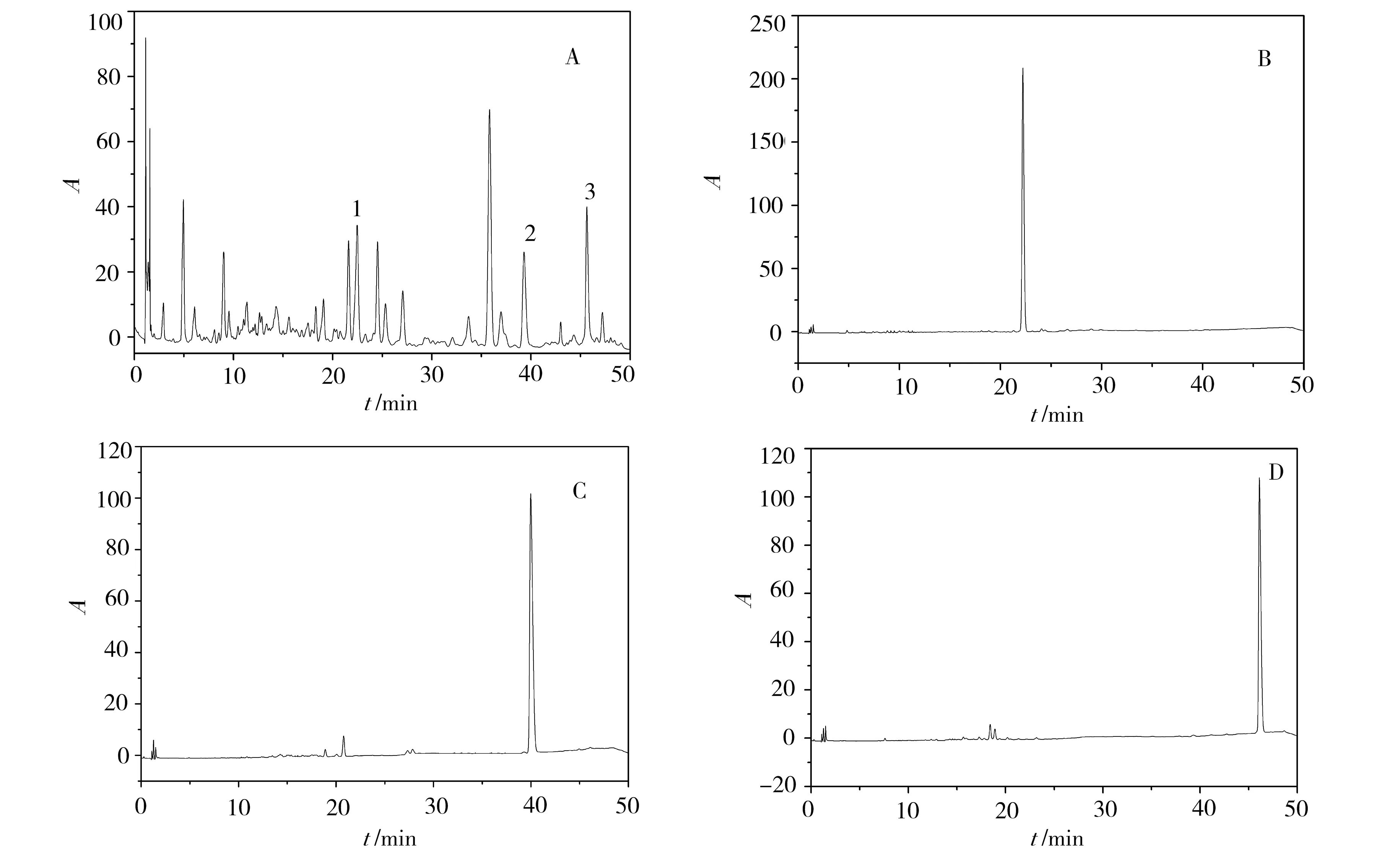
(A) 乙酸乙酯萃取物; (B) 图2中峰1; (C) 图2中峰2; (D) 图2中峰3
2.3 结构鉴定
化合物1: 无色油状物;ESI-MS:m/z 421.7 [M+CH3COOH]-;1H NMR(400MHz, CDCl3):4.93(1H, br dd, 8.5, 3.3, H-1), 2.51(1H, m, H-2a), 2.33(1H, m, H-2b), 4.35(1H, br dd, 14.4, 6.2, H-3), 4.85(1H, br d, 9.9, H-5), 5.21(1H, t, 9.2, H-6), 2.92(1H, m, H-7), 5.80(1H, br d, 2.6, H-8), 2.84(1H, dd, 14.4, 4.5, H-9a), 2.30(1H, br d, 14.4, 2.0, H-9b), 6.33(1H, d, 3.4, H-13a), 5.64(1H, d, 3.4, H-13b), 1.52(3H, br s, H-14), 1.81(3H, br s, H-15), 6.79(1H, m, H-3′),4.38(2H, br dd, 5.2, 5.8, H-4′), 1.83(3H, br s, H-5′).经与文献[14]对照,推断化合物1为3β-Hydroxy-8β-[4′-hydroxytigloyloxy]-costunolide.
化合物2: 无色油状物;ESI-MS: m/z 463.3 [M+H]+;1H NMR(400MHz, CDCl3): 5.27(1H, m, H-1), 2.42(1H, m, H-2a), 2.75(1H, m, H-2b), 5.30(1H, m, H-3), 5.23(1H, br d, 9.9, H-5), 5.83(1H, dd, 11.2, 9.9, H-6), 2.98(1H, m, H-7), 5.48(1H, m, H-8), 2.30(1H, br d, 14.2, H-9a), 3.15(1H, br d, 12.8, H-9b), 6.38(1H, d, 1.4, H-13a), 5.80(1H, d, 1.4, H-13b), 4.90(1H, d, 13.2, H-14a), 4.71(1H, d, 13.2, H-14b), 1.85(3H, br s, H-15), 6.76(1H, t, 5.3, H-3′), 4.30(2H, m, H-4′), 1.80(3H, br s, H-5′), 2.01(3H, s, CH3COO), 2.19(3H, s, CH3COO).经与文献[6]对照,推断化合物2为野马追内酯 A.
化合物3: 无色油状物;ESI-MS:m/z 463.3 [M+H]+;1H NMR(400MHz, CDCl3): 5.37(1H, m, H-1), 2.32(1H, m, H-2a), 3.02(1H, m, H-2b), 5.27(1H, br d, 8.7, H-3), 5.35(1H, br d, 10.4, H-5), 5.25(1H, m, H-6), 3.02(1H, m, H-7), 5.51(1H, m, H-8), 2.21(1H, m, H-9a), 2.88(1H, m, H-9b), 6.37(1H, d, 2.0, H-13a), 5.82(1H, d, 2.0, H-13b), 4.97(1H, d, 12.6, H-14a), 4.69(1H, d, 12.7, H-14b), 1.81(3H, br s, H-15), 6.77(1H, t, 5.4, H-3′), 4.30(2H, d, 5.8, H-4′), 1.80(3H, br s, H-5′), 2.03(3H, s, CH3COO), 2.11(3H, s, CH3COO).经与文献[6]对照,推断化合物3为野马追内酯 B.
3 结论
本文首次研究了使用高速逆流色谱分离制备野马追中3种倍半萜烯内酯化合物的方法,与常规硅胶柱色谱的方法相比,该方法具有快速、高效、节省溶剂等优点,得到的高纯度样品可以作为标准品用于分析测试或药理与毒理试验.此方法可为野马追植物化学成分的分离提取提供技术参考,也为野马追中活性化合物的筛选提供物质基础.
[1] 国家中医药管理局. 中华本草[M]. 上海:上海科学技术出版社, 1999.
[2] Ji L L, Luo Y M, Yan G L. Studies on the antimicrobial activities of extracts from Eupatorium lindleyanum DC against food spoilage and food-borne pathogens[J]. Food Control, 2008, 19(10):995-1001.
[3] Yan G L, Ji L L, Luo Y M,et al. Antioxidant activities of extracts and fractions from Eupatorium lindleyanum DC[J]. Molecules, 2011, 16(7):5998-6009.
[4] Yang N Y, Duan J A, Shang E X, et al. Analysis of Sesquiterpene Lactones in Eupatorium lindleyanum by HPLC-PDA-ESI-MS/MS[J]. Phytochemical Analysis, 2010, 21(2):144-149.
[5] Ye G, Huang X Y, Li Z X, et al. A new cadinane type sesquiterpene from Eupatorium lindleyanum (Compositae)[J]. Biochemical Systematics and Ecology, 2008, 36(9): 741-744.
[6] Yang N Y, Qian S H, Duan J A, et al. Two new sesquiterpenes from Eupatotium lindleyanum[J]. Chinese Chemical Letters, 2005, 16(9): 1223-1226.
[7] Huo J, Yang S P, Ding J, et al. Cytotoxic sesquiterpene lactones from Eupatorium lindleyanum[J]. Journal of Natural Products, 2004, 67(9), 1470-1475.
[8] 杨念云,钱士辉,段金廒,等.野马追地上部分的化学成分研究[J]. 中国药科大学学报, 2003, 34(3):220-221.
[9] Kazuo I, Yoshihisa S, Mitsumasa H, et al. Four new germacranolides from Eupatorium lindleyanum DC[J]. Chemistry Letters, 1979, 12: 1469-1472.
[10] Ito, Y, Conway W D. High-speed countercurrent chromatography[J]. Critical Reviews in Analytical Chemistry, 1986. 17(1): 65-143.
[11] Gutzeit. Preparative Isolation and Purification of Flavonoids and Protocatechuic Acid from Sea Buckthorn Juice Concentrate by High-Speed Counter-Current Chromatography[J]. Chromatographia, 2007, 65(1):1-7.
[12] Weisz A, Ito Y. Performance comparison of three types of high-speed counter-current chromatographs for the separation of components of hydrophilic and hydrophobic color additives[J]. Journal of Chromatography A, 2011, 1218(36): 6156-6164.
[13] Wei Y, Du S, Ito Y. Enantioseparation of lomefloxacin hydrochloride by high-speed counter-current chromatography using sulfated-β-cyclodextrin as a chiral selector[J]. Journal of Chromatography B, 2010, 878(28): 2937-2941.
[责任编辑:蒋海龙]
IsolationandPurificationofthreeSesquiterpenoidLactonesfromEupatoriumLindleyanumDCEthylAcetateFractionbyHigh-speedCounter-currentChromatography
YAN Gui-long1,2,3, Ji Li-lian2, LUO Yu-ming2, HU Yong-hong3
(1.Jiangsu Key Laboratory for Biomass-based Energy and Enzyme Technology, Huaiyin Normal University, Huaian Jiangsu 223300, China)(2.Jiangsu Key Laboratory for Eco-Agricultural Biotechnology around Hongze Lake, Huaiyin Normal University, Huaian Jiangsu 223300, China)(3.College of Life Science and Pharmaceutical Engineering, Nanjing University of Technology, Nanjing Jiangsu 210009, China)
A high-speed counter-current chromatography(HSCCC) method was established for the separation of three sesquiterpenoid lactones from Eupatorium lindleyanum DC. n-butanol fraction. The two-phase solvent system composed of n-hexane-ethyl acetate-methanol-water (1:4:2:3) was selected. From 900 mg of n-butanol fraction of Eupatorium lindleyanum DC, 6.5mg of 3β-Hydroxy-8β-[4′-hydroxytigloyloxy]-costunolide, 28.5 mg of eupalinolide A and 29.3 mg of eupalinolide B were obtained in one-step HSCCC separation, with the purity of 92.5%, 91.7% and 93.9%, respectively, as determined by HPLC. Their structures were further identified by ESI-MS and1H NMR.
eupatorium lindleyanum DC; high-speed counter-current chromatography; sesquiterpenoid lactone; separation
R284.2
A
1671-6876(2012)03-0261-05
2012-07-02
江苏省研究生科研创新计划项目(CX10B-182Z); 江苏省生物质能与酶技术重点实验室课题项目(JSBEET1222)
鄢贵龙(1975-), 男, 江西临川人, 讲师, 博士生, 研究方向为发酵工程及天然产物应用开发.
