抗病毒分散片质量标准研究
2012-11-06李其凤冯柏康
肖 飞,陈 桦,李其凤,冯柏康
(广州中医药大学科技产业园有限公司,广东 广州 510445)
抗病毒分散片由连翘、板蓝根、石膏、知母、石菖蒲、广藿香等中药加辅料组成,具有清热祛湿、凉血解毒之功效,主治风热感冒、温病发热及上呼吸道感染、流行性感冒、腮腺炎等病毒感染性疾病[1]。本试验在抗病毒分散片优选制备工艺基础上,进行产品质量控制方法研究,建立了连翘、板蓝根、知母、石菖蒲薄层色谱鉴别方法,并用高效液相色谱法测定连翘苷的含量。该方法结果准确、操作简便,可作为抗病毒分散片的质量控制方法。
1 仪器与试药
Waters 2695-2996型高效液相色谱系统,包括2695溶剂处理系统、2996二极管阵列检测器、Empower色谱处理系统,(美国Waters公司);BP221S型电子天平(d=0.1 mg),M215S型电子天平(d=0.01 mg),均为德国Sartorius公司产品。抗病毒分散片为广州中医药大学科技产业园有限公司自制;连翘苷对照品(批号为11082200406)、菝葜皂苷元对照品(批号为0744-200005)、连翘对照药材(批号为120908-200305)、板蓝根对照药材(批号为121177-200305)、知母对照药材(批号为121070-200306)、石菖蒲对照药材(批号为121098-200402),均购自中国药品生物制品检定所;阴性样品(自制);乙腈为色谱纯,水为超纯水,其他试剂均为分析纯。
2 方法与结果
2.1 薄层色谱(TLC)鉴别
连翘[2-3]:取本品适量,研细,称取4 g,加水30 mL,加热回流30 min,滤过,滤液用乙酸乙酯充分振摇提取3次,每次30 mL,合并乙酸乙酯液,蒸干,残渣加甲醇2 mL使溶解,作为供试品溶液;另取缺连翘的阴性对照品4 g,同法制成阴性对照品溶液;再取连翘对照药材2 g,同法制成对照药材溶液。照薄层色谱法[2010年版《中国药典(一部)》附录ⅥB]试验,吸取上述3种溶液各5μL,分别点于同一以羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以三氯甲烷-乙酸乙酯(9∶1)为展开剂,展开,取出,晾干,喷以10%的硫酸乙醇溶液,100℃加热至斑点显色清晰。供试品溶液色谱中,在与对照药材溶液色谱相应位置上显相同颜色的斑点,阴性对照品溶液无干扰(图1 A)。
板蓝根[4-5]:取本品适量,研细,取3 g,加水50 mL,加热回流30min,离心,取上清液置分液漏斗中,用乙醚提取2次,每次30mL,合并乙醚液,蒸干,残渣加乙酸乙酯0.5 mL使溶解,作为供试品溶液;另取缺板蓝根的阴性对照品3 g,同法制成阴性对照品溶液;再取板蓝根对照药材2 g,同法制成对照药材溶液。照薄层色谱法[2010年版《中国药典(一部)》附录ⅥB]试验,吸取上述3种溶液各10μL,分别点于同一以羧甲基纤维素钠为黏合剂的硅胶GF254薄层板上,以苯-三氯甲烷-丙酮(5∶4∶1)为展开剂,展开,取出,晾干,置紫外光灯(254 nm)下检视。供试品溶液色谱中,在与对照药材溶液色谱相应位置上显相同颜色的斑点,阴性对照品溶液无干扰(图1 B)。
知母[6]:取本品适量,研细,称取6 g,加水50 mL,加热回流30 min,放冷,滤过,滤液用水饱和的正丁醇提取2次,每次40 mL,合并正丁醇液,蒸干,残渣加乙醇10 mL,盐酸1 mL,加热回流1 h后浓缩至约5 mL,再加水10 mL,用石油醚(60~90℃)30 mL振摇提取,石油醚提取液用0.5%氢氧化钠溶液20 mL洗涤,弃去碱液,再用水20 mL洗涤,弃去水液,石油醚液蒸干,残渣加乙醇0.5 mL使溶解,作为供试品溶液;另取缺知母的阴性对照品6 g,同法制成阴性对照品溶液;再取知母对照药材2 g,同法制成对照药材溶液;取菝葜皂苷元对照品,加无水乙醇制成每1 mL含3 mg的溶液作为对照品溶液。照薄层色谱法[2010年版《中国药典(一部)》附录ⅥB]试验,吸取上述4种溶液各5μL,分别点于同一以羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以苯-丙酮(19∶2)为展开剂,展开,取出,晾干,喷以8%香草醛无水乙醇溶液和硫酸溶液(7→10)的混合溶液(0.5∶5),100℃加热至斑点显色清晰。供试品溶液色谱中,在与对照品溶液和对照药材溶液色谱相应位置上显相同颜色的斑点,阴性对照品溶液无干扰(图1 C)。
石菖蒲[6-7]:取本品20片,粉碎过40目筛,加水50 mL,超声处理30 min,滤过,滤液用石油醚(30~60℃)提取2次,每次50 mL,提取液水浴蒸干,残渣加乙酸乙酯1 mL使溶解,作为供试品溶液;另取缺石菖蒲的阴性对照品12 g,同法制成阴性对照品溶液;再取石菖蒲对照药材1 g,加石油醚(30~60℃)50 mL,超声60 min,滤过,滤液水浴蒸干,残渣加乙酸乙酯1 mL使溶解,作为对照药材溶液。照薄层色谱法[2010年版《中国药典(一部)》附录ⅥB]试验,吸取上述3种溶液各5μL,分别点于同一以羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以苯-乙酸乙酯(12∶1)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。供试品溶液色谱中,在与对照药材溶液色谱相应位置上显相同颜色的荧光斑点,阴性对照品溶液无干扰(图1 D)。
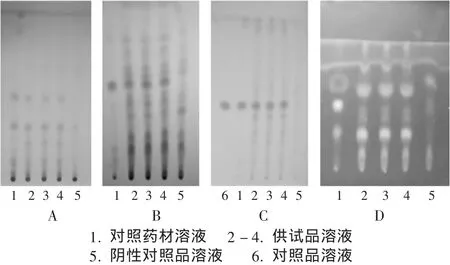
图1 薄层色谱图
2.2 含量测定[8]
2.2.1 色谱条件及系统适用性试验
色谱柱:Merk-C18柱(250 mm×4.6 mm,5μm);流动相:乙腈-水(20∶80);流速:1.0 mL/min;柱温:30℃;检测波长:277 nm。在上述色谱条件下,连翘苷在24 min出峰,理论板数按连翘苷计算 n=9 523;供试品溶液色谱在对照品溶液色谱相应保留时间上出现一色谱峰,连翘苷峰与其他峰的分离度大于1.5。
2.2.2 溶液制备
称取连翘苷对照品8.04 mg,精密称定,用甲醇溶解并定容至10 mL,作为对照品贮备液;精密吸取贮备液1 mL,用甲醇稀释至10 mL,作为对照品溶液。取本品10片,研细,取4 g,精密称定,置具塞锥形瓶中,精密加入甲醇15 mL,称定质量,浸渍过夜,超声处理25 min,放冷,再称定质量,用甲醇补足减失的质量,摇匀,滤过,精密量取续滤液5 mL,蒸至近干,加中性氧化铝1 g拌匀,加置中性氧化铝柱(200-300目,1 g,内径 1.5 cm)上,用70%乙醇100 mL洗脱,收集洗脱液,浓缩至干,残渣用50%甲醇溶解,转移至5 mL量瓶中,并稀释至刻度,摇匀,滤过,取续滤液,即得供试品溶液。取缺连翘的阴性对照品4 g,同供试品溶液制备方法制成阴性对照品溶液。
2.2.3 方法学考察
专属性考察:取连翘苷对照品溶液、供试品溶液及阴性对照品溶液,照2.2.1项下色谱条件测定。结果表明其他成分对连翘苷含量测定无干扰。高效液相色谱图见图2。
线性关系考察:精密吸取对照品溶液 2,6,8,10,20 μL,注入液相色谱仪,按上述色谱条件测定峰面积,以对照品进样量 X(μg)为横坐标、峰面积值 Y为纵坐标作标准曲线图,连翘苷回归方程为Y=553 564X-6 457.3,r=0.999 9(n=5)。结果表明,连翘苷进样量在0.160 8~1.608 0μg范围内与峰面积具有良好的线性关系。
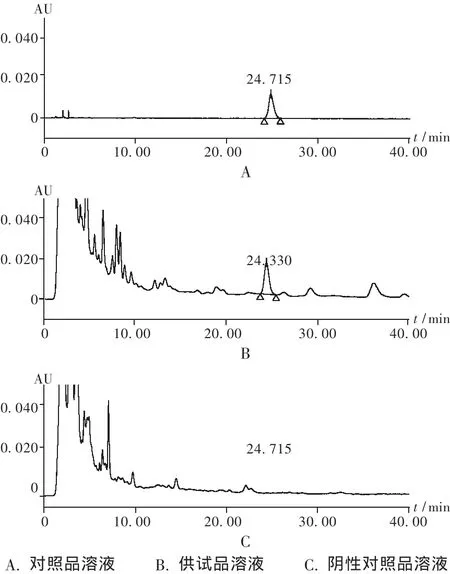
图2 高效液相色谱图
精密度试验:精密吸取对照品溶液,重复进样5次。结果连翘苷峰面积的 RSD为0.82%(n=5),表明仪器精密度良好。
重复性试验:取同一批样品(批号为100321),精密称取6份,分别照含量测定法制备供试品溶液并测定。结果连翘苷的平均含量为0.037 2%,RSD为2.3%(n=6),表明方法重复性较好。
稳定性试验:精密量取同一供试品溶液,在室温下,分别在0,2,4,6,8 h时测定连翘苷峰面积。结果的 RSD为 1.4%(n=5),表明样品中连翘苷在测定的8 h内稳定。
加样回收试验:取同一批样品(批号为100321),精密称取6份,分别精密加入连翘苷对照品贮备液1 mL,将甲醇挥干,分别照含量测定法制备供试品溶液,测定含量。结果见表1。

表1 连翘苷加样回收试验结果(n=6)
2.2.4 样品含量测定
精密称取本品,照含量测定法测定,标准曲线法计算样品中连翘苷含量。结果批号分别为100321,100403,100411的3批样品中连翘苷含量分别为0.28,0.27,0.28 mg/片。根据2010年版《中国药典(一部)》规定,连翘药材以连翘苷(C27H34O11)计,不得少于0.15%;抗病毒分散片以转移率60%计,每粒含连翘苷(C27H34O11)应不低于0.20 mg。故暂订本品每片含连翘以连翘苷(C27H34O11)计,应不低于0.20 mg。
3 讨论
本研究中抗病毒分散片的提取工艺与部颁标准中抗病毒栓以及新药转正标准中抗病毒口服液、抗病毒胶囊、抗病毒糖浆、抗病毒片等不完全相同,因此质量控制指标及方法不尽相同。此外,本试验还按照2010年版《中国药典(一部)》附录片剂项下规定,进行了质量差异、溶出度、分散均匀性及微生物限度等检测,均符合规定。
本试验对抗病毒分散片中广藿香的薄层色谱鉴别方法进行了研究,以广藿香对照药材、百秋李醇对照品作对照,效果均不理想,试验方法还有待进一步研究,故暂不列入质量标准。
[1]肖 飞,于 伟.抗病毒分散片的制剂工艺研究[J].湖北中医学院学报,2006,8(2):34-35.
[2]王小龙,邢海英,王琳静.薄层色谱法鉴别抗病毒口服液的前处理改进[J].中国药师,2003,6(12):833.
[3]张秀丽.连翘败毒丸的薄层层析鉴别[J].中国当代医药,2010,17(3):111.
[4]徐云友,徐连江.抗病毒质量标准研究[J].人参研究,2004,16(2):44.
[5]陈明江,汪 勋.复方南板蓝根片的薄层色谱鉴别[J].中国药业,2009,18(2):32.
[6]黄晓玲,刘乡乡.抗病毒口服液的质量标准研究[J].中药新药与临床药理,2004,15(3):182.
[7]黎奕明,眭道顺.石菖蒲的薄层鉴别及β-细辛醚的含量测定[J].中药新药与临床药理,2009,20(4):369-370.
[8]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010:159.
