高效液相色谱法测定转化糖电解质注射液中转化糖含量
2012-11-06咸瑞卿陈德俊徐玉文
咸瑞卿,陈德俊,徐玉文
(山东省食品药品检验所,山东 济南 250101)
转化糖电解质注射液是由葡萄糖与果糖等分子混合制成的同时含有电解质的复方制剂,适用于临床需要非口服途径补充水分或能源及电解质患者的补液治疗,尤其适用于作为糖尿病患者的能量及电解质补充剂,烧、创伤,术后及感染等胰岛素抵抗患者的能量及电解质补充剂[1-2]。目前YBH05732005,YBH21112005、第34版《美国药典》[3]测定转化糖含量的方法是利用果糖和葡萄糖的还原性,定量地将碱性酒石酸铜还原成氧化亚铜,从而通过测定生成的氧化亚铜质量计算出转化糖的含量。但该方法不能分别测定两种单糖的含量,而且操作烦琐,重现性差。笔者采用高效液相色谱-紫外光检测器(HPLC-UV)法同时测定葡萄糖和果糖的含量,简便快速,分离效果、重现性、精密度良好,在常规质量分析中能更好地控制该制剂的质量,现报道如下。
1 仪器与试药
Agilent 1200型高效液相色谱仪;CP225D型电子天平。D-无水葡萄糖对照品(中国食品药品检定研究院,批号为110833-200904,含量100.0%);果糖对照品(中国食品药品检定研究院,批号为100231-200904,含量100.0%);磷酸为色谱纯,水为纯化水;转化糖电解质注射液(规格为250 mL:果糖6.25 g葡萄糖6.25 g,青岛华仁药业有限公司,批号分别为B1104001,B1104002,B1104003)。
2 方法与结果
2.1 色谱条件与系统适用性试验
色谱柱:Sugar SH1011柱(8.0 mmID×300 mL);流动相:0.04 mol/L的磷酸溶液;流速:0.5 mL/min;检测波长:195 nm;进样量:20μL;柱温:50℃。在此条件下,色谱图见图1。空白对照品溶液色谱图在对照品溶液峰位置无干扰峰,葡萄糖与果糖分离度良好(大于1.9),保留时间葡萄糖约为13.54 min、果糖约为14.47 min,理论板数均达15 000,表明该系统适用性良好。
2.2 溶液制备
分别精密称取 D-无水葡萄糖、果糖对照品49.98 mg和50.05 mg,置10 mL量瓶中,用流动相溶解并稀释至刻度,摇匀,作为对照品溶液。精密量取样品适量(约相当于转化糖100 mg),置10 mL量瓶中,用流动相稀释至刻度,摇匀,作为供试品溶液。取辅料适量,按处方比例配制,按供试品溶液制备方法制备空白对照品溶液。
2.3 方法学考察
线性关系考察:精密量取对照品溶液 5,10,15,20,30,40,50μL进样。以进样量为横坐标、峰面积为纵坐标作图,用最小二乘法进行线性回归。结果表明,葡萄糖进样量在24.99~249.90μg范围内,果糖在25.25~252.50μg范围内分别与相应峰面积呈良好线性关系。葡萄糖和果糖的回归方程分别为Y1=8.665X1+6.366(r1=1.000 0)和Y2=43.963X2+17.547(r2=1.000 0)。
加样回收试验:精密量取已知准确含量的同一样品适量(约相当于转化糖50 mg),共取9份,分成3组,分别置10 mL量瓶中;另分别精密称取 D-无水葡萄糖和果糖对照品0.501 0,0.504 8 g,置100 mL量瓶中,加流动相溶解并稀释至刻度,摇匀,分别精密量取3,5,7 mL,各3份,置样品的量瓶中加流动相稀释至刻度,摇匀。进样20μL,按外标法测定含量,计算回收率。结果见表1。
稳定性试验:取同一供试品溶液,分别在 0,1,2,5,10 h时进样,依法测定。结果葡萄糖与果糖峰面积的 RSD分别为0.52%和0.68%,表明供试品溶液在10 h内稳定。

表1 加样回收试验测定结果(n=9)
精密度试验:取同一对照品溶液,连续进样6次。结果葡萄糖与果糖峰面积的 RSD分别为0.72%和0.57%,表明仪器精密度良好。
重复性试验:取同一批样品适量(约相当于转化糖100 mg,批号为B1104001)共6份,分别置10 mL量瓶中,用流动相稀释至刻度,摇匀,依法测定。结果葡萄糖与果糖峰面积的 RSD分别为0.44%和0.42%,表明分析方法重复性良好。
2.4 样品含量测定
取样品3批,分别按2.2项下方法制备供试品溶液,精密量取对照品溶液和供试品溶液各20μL,注入液相色谱仪,依法测定。结果见表2。
3 讨论
国内标准YBH05732005和YBH21112005参照第34版《美国药典》[3]采用重量法测定转化糖的含量,不能分别测定果糖与葡萄糖的含量,且过滤需用的G4垂熔坩埚(国内市售)不耐碱,导致回收率、重现性差。另采用高效液相色谱-蒸发光散射检测法[4]、高效液相色谱-示差折光检测法[5]等方法虽能分别测定葡萄糖和果糖的含量,但存在仪器昂贵、适用性不强等问题。
采用高效液相色谱-紫外光检测器(HPLC-UV)法分别测定转化糖电解质注射液中葡萄糖和果糖的含量,方法学考察结果表明,方法的重现性好,测定结果准确,为该制剂的质量控制与检测提供了一种更加准确、方便、科学的方法。
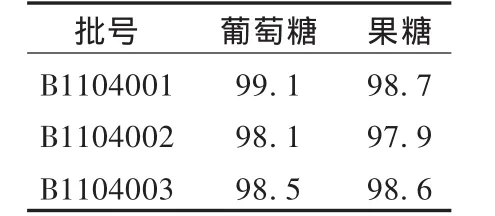
表2 样品含量测定结果(%)
[1]王欧明.含果糖制剂的临床合理应用[J].中国医院药学杂志,2009,29(4):330-331.
[3]Multiple Electrolytes and Invert Sugar Injection.《美国药典》[M].第34版.2011:2 674-2 677.
[4]杨 俊,刘江生,蔡继宝,等.高效液相色谱-蒸发光散射检测法测定烟草中的水溶性糖[J].分析化学研究简报,2005,33(11):1 596-1 598.
[5]孙守兵.高效液相色谱法测定转化糖电解质注射液中果糖和葡萄糖的含量[J].中国新药与临床杂志,2010,29(12):916-918.
