GC法测定肛安栓中冰片的含量
2012-10-25徐丽华
高 辉,徐丽华
(山东省食品药品检验所,山东济南250101)
肛安栓是由地榆炭、五倍子、盐酸小檗碱、人工麝香、冰片等5味中药组成的复方制剂,具有凉血止血,清热解毒,燥湿敛疮,消肿止痛功效,临床上用于湿热下注所致的内痔、混合痔以及炎性外痔。本品是烟台荣昌制药有限公司独家生产的品种,现行标准为国家食品药品监督管理局国家药品标准WS3-129(Z-129)-2001(Z)。冰片是肛安栓中的主要有效成分之一,具有清热止痛的作用,且冰片在制备、储存的过程中易挥发损失。为更好的控制肛安栓的内在质量,研究建立冰片的GC的含量测定方法。
1 仪器与试药
Agilent 6890N气相色谱仪(Agilent公司,美国),Sartorius CP225D电子天平(Sartorius公司,德国);冰片由中国药品生物制品检定所提供,含量测定用,批号为110743-200504;样品和阴性对照均由烟台荣昌制药有限公司提供,样品批号为090501、090502、100101。乙酸乙酯为分析纯。
2 方法与结果[1~4]
2.1 色谱条件 色谱柱:Agilent HP-FFAP石英毛细管柱(0.25 mm ×30.0 m,0.25 μm),柱温 130 ℃,进样口温度 180℃;检测器温度230℃;氢离子火焰检测器;恒流;分流比40∶1。冰片出峰后采用程序升温,以减少其他杂质在色谱柱中的残留。

表1 程序升温
2.2 溶液的制备 对照品溶液的制备:精密称取冰片对照品11.60 mg,加乙酸乙酯溶解并稀释至10 mL,作为对照品溶液(浓度为:1.16 mg·mL-1)。
供试品溶液的制备:取重量差异项下的本品,切细,取约2 g,精密称定,置具塞锥形瓶中,精密加入乙酸乙酯25 mL,超声处理(功率500 W,频率40 kHz)10 min,摇匀,滤过,滤液于4℃的冷藏室中放置3 h,取出,迅速滤过,取续滤液,即得。
2.3 线性关系的考察 分别精密吸取对照品溶液(C对为0.29 mg·mL-1)0.2、1、2、3、4、5 μL,注入气相色谱仪,分别测定峰面积。以冰片对照品的进样量为横坐标X,龙脑峰、异龙脑峰面积之和为纵坐标Y,进行线性回归,得回归方程Y=389.101X+16.285,相关系数 r=0.999 97。表明冰片进样量在0.058~1.450 0 μg之间与峰面积呈良好的线性关系。
2.4 仪器精密度试验 精密吸取冰片对照品溶液(C对为0.58 mg·mL-1)1 μL,注入气相色谱仪,连续进样 6 次,测定龙脑、异龙脑的峰面积之和,RSD为0.25%。结果表明仪器精密度良好。
2.5 样品稳定性试验 取2.2项下的供试品溶液,精密吸取1 μL,注入气相色谱仪,每隔2 h进样一次,测定龙脑、异龙脑的峰面积之和,共考察10 h,RSD为0.28%。表明供试品溶液在10 h内稳定性良好。
2.6 重复性试验 取肛安栓(山东荣昌制药股份有限公司,批号090502)约2 g,照2.2项下供试品溶液的制备方法,平行制备6份样品,按上述方法和条件进行测定,计算含量,结果平均含量为6.16 mg/粒,RSD为1.70%,表明本品含量测定方法的重复性良好。
2.7 加样回收率试验 取已测知含量的本品(山东荣昌制药股份有限公司,批号为090502,含量6.16 mg/粒,平均粒重1.004 6 g)约1 g,精密称定,共取6份,置具塞锥形瓶中,各分别精密加入冰片对照品5 mg,精密加入乙酸乙酯25 mL,超声处理(功率500 W,频率40 kHz)10 min,摇匀,滤过,滤液于4℃的冷藏室中放置3 h,取出,迅速滤过,取续滤液,即得。按上述条件进行测定,分别计算加样回收率,结果见表2。
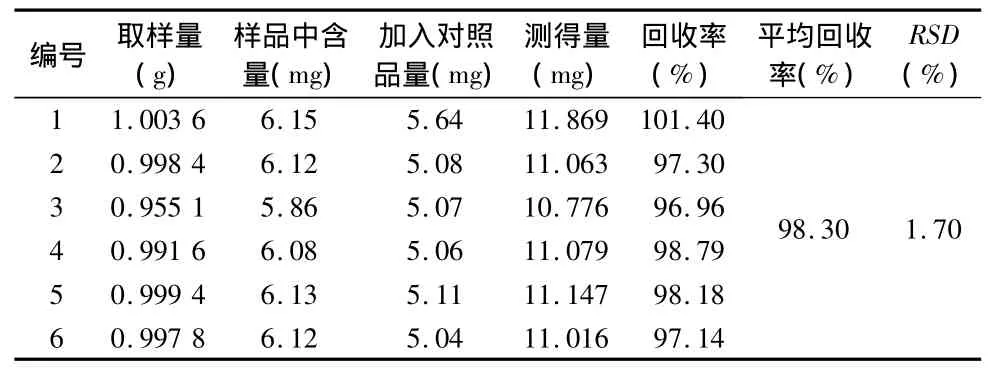
表2 加样回收率试验结果
2.8 专属性试验 取处方中除去冰片的其他药味,按处方比例制成缺冰片的阴性对照样品。取阴性对照样品约2 g,同供试品溶液的制备方法制成阴性对照溶液。
分别精密吸取上述对照品溶液、供试品溶液及阴性对照溶液各1 μL,注入气相色谱仪进行测定。结果供试品色谱中,在与对照品色谱保留时间相同的位置上,有相应色谱峰,而阴性对照无干扰,结果见图1、2。
2.9 样品测定 按供试品溶液的制备方法及上述色谱条件对3批样品进行测定,结果分别为 6.0 mg/粒、6.2 mg/粒、6.0 mg/粒。
3 讨论
3.1 供试品溶液的制备 过程中考察了不同提取溶剂(环乙烷、乙酸乙酯和甲醇),结果表明,乙酸乙酯提取冷藏后,基质凝固均匀,易除去,测得含量较高。故最终确定提取溶剂为乙酸乙酯。
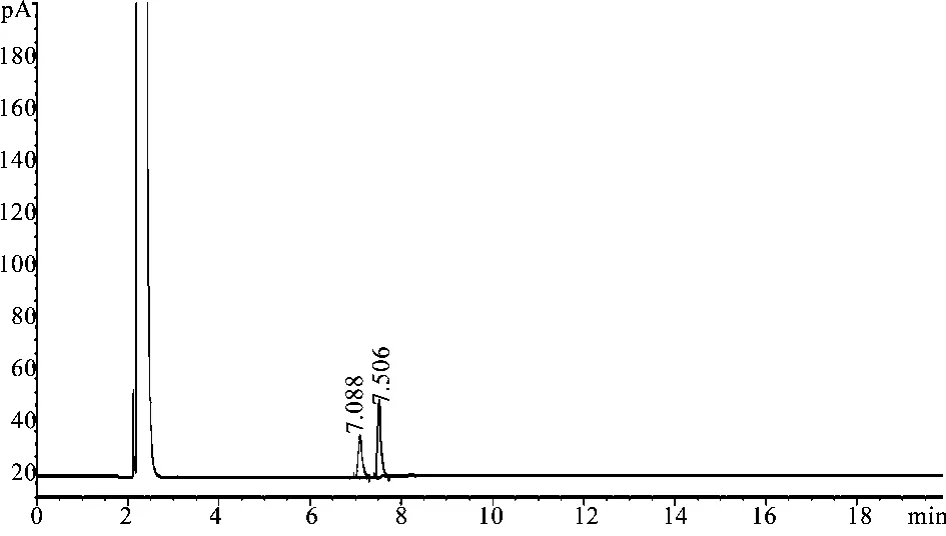
图1 冰片对照品的GC色谱图
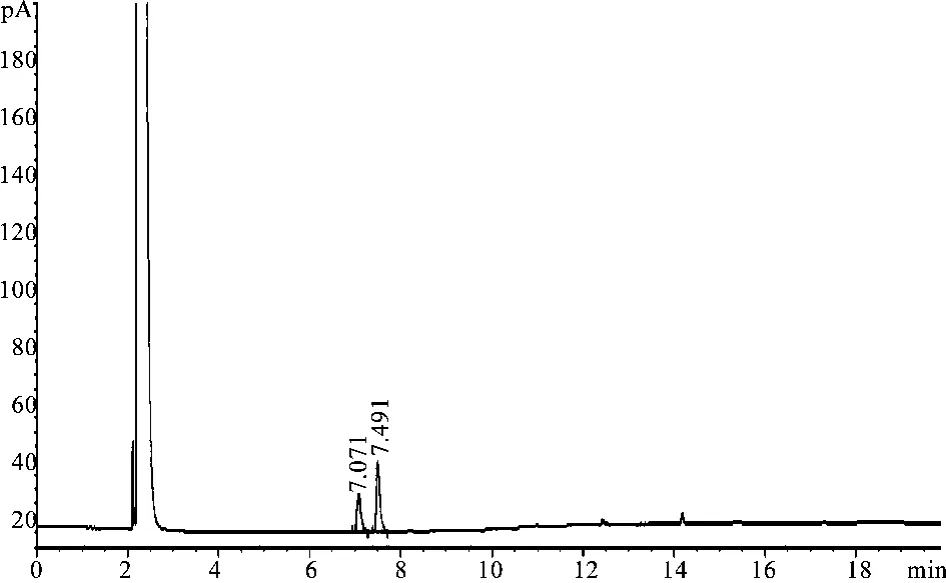
图2 供试品的GC色谱图
3.2 实验中考察了不同提取方式(超声后直接冷藏3 h、超声后滤过,-7℃冷冻30 min及超声后滤过,分别冷藏2 h、3 h和过夜)。结果表明,冷藏3 h基质凝固均匀,易滤过除去,且测得含量略高,故选之。
3.3 考察不同取样量(1.0、2.0、3.0 g),结果表明,取1.0 g、2.0 g测得含量结果无显著性差异,3.0 g测得含量略低。结合溶液含冰片的浓度及考虑样品的均一性,确定取样量为2.0 g。
3.4 实验考察了两种色谱柱 Agilent HP-FFAP(0.25 mm×30.0 m,0.25 μm)键合和改性的交联聚乙二醇毛细管柱;Agilent INNOWAX(0.25 mm ×30.0 m,0.25 μm)键合/交联聚乙二醇固定相毛细管柱。按上述确定的方法和条件进行测定,两种色谱柱的测定结果表明用该色谱条件测定冰片,对称因子、分离度和理论板数等均能基本符合2010年版《中国药典》对气相色谱分析的有关要求,选择该色谱条件测定冰片,对色谱柱选择性不强,适用范围广。
[1]国家药典委员会.中华人民共和国药典2010年版(一部)[S].北京:中国医药科技出版社,2010:附录38.
[2]蔡铝铝,潘金火,金芝兰.GC测定镇江巴布膏中冰片、薄荷脑、樟脑和水杨酸甲酯的含量[J].现代中药研究与实践,2011,25(1):54 -57.
[3]秦臻,彭绍忠,陈海明.抗流感滴丸中新莪术二酮的含量测定[J].中国实验方剂学杂志,2011,17(2):43-45.
[4]张淼,袁浩,冯丽.GC法测定拨云散眼药中龙脑、异龙脑的含量[J].中国药事,2011,25(1):79-80.
