HPLC法测定复方青黛胶囊中靛玉红的含量
2012-10-25胡安青
徐 斐,胡安青
(镇江市药品检验所,江苏镇江212003)
复方青黛胶囊收载于国家药品标准[1],处方由青黛、马齿苋、白芷、土茯苓、紫草、贯众、蒲公英、丹参、粉萆薢、白皮、乌梅、五味子(酒制)、山楂(焦)、建曲组成。具有清热解毒,化瘀消斑,祛风止痒的功能。临床用于热挟瘀、热毒炽盛证;进行期银屑病、玫瑰糠疹、药疹等治疗。但在控制产品的质量方面,原标准采用薄层扫描法测定复方青黛胶囊中靛玉红的含量,其操作过程复杂,重现性、稳定性、精密度均较高效液相色谱法差。而笔者以高效液相色谱法测定复方青黛胶囊中靛玉红含量,结果表明,方法简便,专属性强,可用于复方青黛胶囊的质量控制。
1 仪器与试药
1.1 仪器 SK250LH超声波清洗器 (上海科导超声仪器有限公司);Waters高效液相色谱仪系统(1525泵、2487紫外可见光光度检测器、Empower工作站);BP211D型电子天平(赛多利士)。
1.2 试药 靛玉红对照品(中国药品生物制品检定所,批号110717-200204);复方青黛胶囊(陕西医药控股集团XX制药有限责任公司,批号:110202,101204,100406);甲醇为色谱纯(Merck KgaA,Germany);水为纯化水,其他均为分析纯。
2 方法与结果
2.1 色谱条件 色谱柱:Kromasil C18(4.6 mm×250 mm,5 μm);流动相[2]:甲醇 - 水(70∶30);流速:1.0 mL·min-1;检测波长:292 nm;柱温:室温。
2.2 溶液的制备
2.2.1 对照品溶液的制备 精密称取靛玉红对照品9.90 mg,置于100 mL量瓶中,加三氯甲烷-甲醇(1∶9)混合溶液使溶解并稀释至刻度,摇匀,即得靛玉红对照品贮备液(含靛玉红 99.0 μg·mL-1)。精密量取 1 mL,置于10 mL 量瓶中,加三氯甲烷-甲醇(1∶9)溶液稀释至刻度,摇匀,即得对照品溶液(含靛玉红 9.90 μg·mL-1)。
2.2.2 供试品溶液的制备[3]取本品10粒的内容物,精密称定,研细,精密称取适量(约相当于4粒内容物的重量),置具塞锥形瓶中,加乙醚20 mL,超声处理30 min,滤过,用适量的乙醚洗涤滤渣和滤器两次,合并洗涤液和滤液,再用10%氢氧化钠溶液洗涤4 次(15 mL、15 mL、15 mL、10 mL),弃去氢氧化钠溶液,取乙醚层挥干,残渣加三氯甲烷-甲醇(1∶9)混合溶液使溶解,转移至5 mL量瓶中,并稀释至刻度,摇匀,用微孔滤膜(0.45 μm)过滤,取续滤液即得。
2.3 专属性考察 按标准处方量及制法制得不含青黛的阴性样品,按供试品溶液制备方法制备阴性对照溶液,进样测定,结果阴性对照色谱在与对照品色谱相应位置上无色谱峰出现,表明阴性对照对测定结果无干扰,方法专属性良好,结果见图1(C)。

图1 靛玉红色相图 (A)靛玉红对照品;(B)供试品;(C)阴性对照
2.4 线性关系 精密吸取靛玉红贮备液 1.0、2.0、3.0、4.0、5.0 mL,分别置于10mL量瓶中,加三氯甲烷-甲醇(1∶9)混合溶液使溶解并稀释至刻度,摇匀。按上述色谱条件测定,分别进样10 μL,记录峰面积。以对照品进样量为横坐标,峰面积为纵坐标,绘制标准曲线。结果进样量在9.90~49.50 μg范围内与峰面积呈良好的线性关系,回归方程 Y=534.834X+0.010(r=0.999 9)。
2.5 精密度试验 取同一对照品溶液,依法操作,连续进样5次,每次10 μL。结果靛玉红对照品峰面积的 RSD为1.0%,表明精密度良好。
2.6 重现性试验 取同一样品5份,按2.2.2项下的方法制备供试品溶液,分别进样,依法测定峰面积,计算含量。结果靛玉红对照品含量的RSD为0.5%(n=5),表明方法重现性较好。
2.7 稳定性试验 在本试验条件下,将样品溶液每隔2 h进样10 μL。靛玉红峰面积的RSD为0.7%。
2.8 加样回收率试验 精密称取已知含量的同一批样品(110202)约相当于2粒内容物的重量,共6份。分别加入靛玉红贮备液(含靛玉红 99.00 μg·mL-1)2.0、2.5、3.0 mL,混匀,同供试品溶液制备,照样品测定方法测定,计算回收率,结果见表1。
2.9 样品含量测定 取3批样品,按供试品溶液制备方法制备溶液,进样10 μL,记录峰面积,按外标法计算靛玉红含量,结果见表2。
3 讨论
3.1 在样品溶液制备中,我们对比了回流提取、索氏提取和超声提取等方法,以超声提取时间短,提取完全,杂质较少;提取溶液用10%氢氧化钠溶液洗涤后杂质明显减少,有利于色谱的测定。
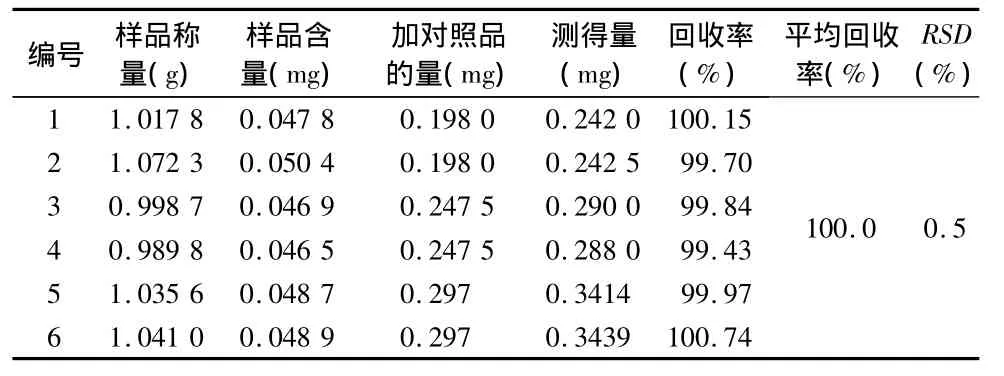
表1 回收率试验结果(n=6)

表2 样品含量测定结果(n=3)
3.2 试验表明,本法在一定浓度的范围内线性、精密度、稳定性和回收率结果可靠,方法简便,快速,重现性好,可作为该制剂质量控制方法。
[1]国家药品监督管理局.国家药品标准新药转正标准(第63册)[S].北京:人民卫生出版社,2009:70-72.
[2]国家药典委员会.中华人民共和国药典2010年版(一部)[S].北京:中国医药科技出版社,2010:185.
[3]张俊燕.RP-HPLC法测定消炎退热颗粒中靛玉红的含量[J].药学与临床研究,2007,15(2):163 -164.
