离子液体中纳米金催化剂的制备及其催化活性
2012-09-25徐静,张金峰,于长顺,薛润苗,陈丽凤,安庆大
徐 静, 张 金 峰, 于 长 顺, 薛 润 苗, 陈 丽 凤, 安 庆 大
( 1.大连工业大学 轻工与化学工程学院, 辽宁 大连 116034;2.大连工业大学 纺织与材料工程学院, 辽宁 大连 116034 )
0 引 言
自Haruta等[1]报道负载型金催化剂对CO优先氧化具有优异催化活性以来,金催化剂以其特有的低温催化活性、活性随湿度增加而增加以及价格相对低廉等优点,引起了各国学者的关注。离子液体作为一种新型的绿色溶剂[2-3]和稳定剂,具有许多独特的物理化学性质和鲜明的特色,环境友好且可循环使用。由于离子液体的电子效应和位阻效应,金属纳米粒子在其中具有一定的溶解度,可以在一定程度上防止纳米粒子的团聚,因此已成功应用于制备某些特殊金属纳米粒子[4]。本文以自制的离子液体1-己基-3-甲基咪唑六氟化磷([C6mim]PF6)为分散剂和溶剂,用溶胶-凝胶法一步合成出了复合纳米Au/SiO2催化剂,并考察了其在甲烷催化实验中的催化活性。
1 实 验
1.1 试剂与仪器
实验试剂:N-甲基咪唑,溴己烷,六氟合磷酸钾,二氯甲烷,丙酮,硝酸银,氯金酸,水合肼(质量分数80%),无水乙醇,氢氧化钠,硅酸乙酯,三氟乙酸(TFA),三氟乙酸酐(TFAA),K2S2O8,以上试剂均为分析纯。
实验仪器:D/Max-3B型X射线衍射仪,Tecnai G2Spirit透射电子显微镜(TEM),PE2000红外-可见分光光度计,Micromertics ASAP 2020型比表面和孔隙率测定仪,Agilent GC6820型气相色谱仪,Agilent GC-MS 7890A,Bruker DRX-400型核磁共振仪。
1.2 [C6mim]PF6的制备
称适量[C6mim]Br和KPF6[n([C6mim]Br)∶n(KPF6)=1∶1],以丙酮为溶剂,在室温下搅拌24 h,过滤取滤液,蒸馏除去丙酮,得到无色透明黏稠油状液体产品[C6mim]PF6。
1.3 Au/SiO2的制备
将氢氧化钠与硅酸乙酯按比例混合,制备SiO2质量分数为30%的硅溶胶。取5 mL的HAuCl4(0.01 mol/L)溶液置于100 mL磨口三口瓶,在搅拌条件下加入一定量离子液体[n([C6mim]Br)∶n(HAuCl4)=1∶1、3∶2、2∶1、5∶2]和5 mL硅溶胶,混合均匀后向溶液中加入6 mL水合肼(0.01 mol/L),常温搅拌3 h,得到蓝紫色凝胶,抽滤,40 ℃老化12 h,干燥后经500 ℃焙烧,得到产品为紫红色粉末。
1.4 液相催化氧化甲烷实验
将一定量纳米金催化剂置于100 mL高压釜反应器中,加入K2S2O81.77 g,TFA 6.5 mL,TFAA 1.95 mL,以甲烷标准气体(氩气为内标)置换3次,再加压至2 MPa后,将反应釜置于油浴中加热到90 ℃并搅拌反应20 h。反应结束后对反应釜中液相进行蒸馏,收集43 ℃的馏分作为液相产品。
2 结果与讨论
2.1 Au/SiO2表征
2.1.1 Au/SiO2的XRD表征
由图1可以看出,在22.24°出现的宽化衍射峰为纳米SiO2,38.08°、44.26°、64.50°出现的3个衍射峰为金的特征衍射峰,分别与面心立方(FCC)结构Au(111)、(200)、(220)晶面相对应。由于金的含量很低,因此衍射峰的强度低而噪声高,难以通过谢乐公式来计算其大致尺寸。
2.1.2 吸附性能测试结果
对于不同离子液体用量合成的Au/SiO2样品的N2吸附-解吸曲线及孔径分布分析表明,样品N2吸附-脱附曲线(图2)符合BDDT中的第Ⅵ类等温线,有明显的滞后环,滞后环属于de Boer的E类型,显示其具有墨水瓶型介孔结构,N2吸附量随p/p0增加而急剧增加,这是由样品的介孔毛细凝聚所引起的。

图1 Au/SiO2的XRD图
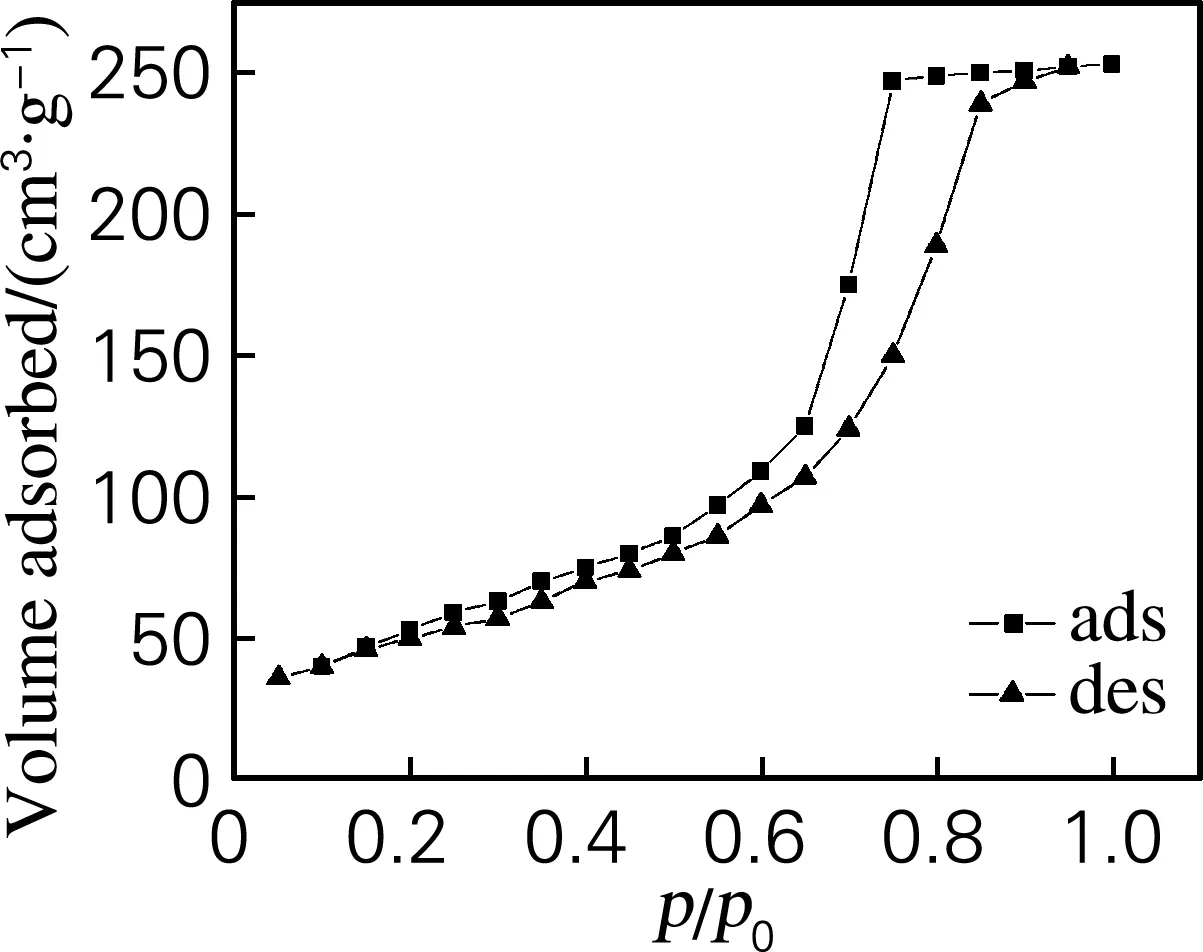
(a) n([C6mim]Br)∶n(HAuCl4)=1∶1
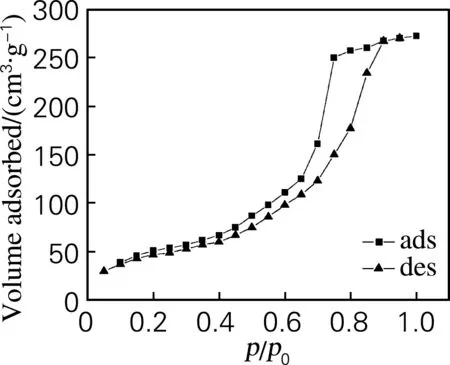
(b) n([C6mim]Br)∶n(HAuCl4)=3∶2
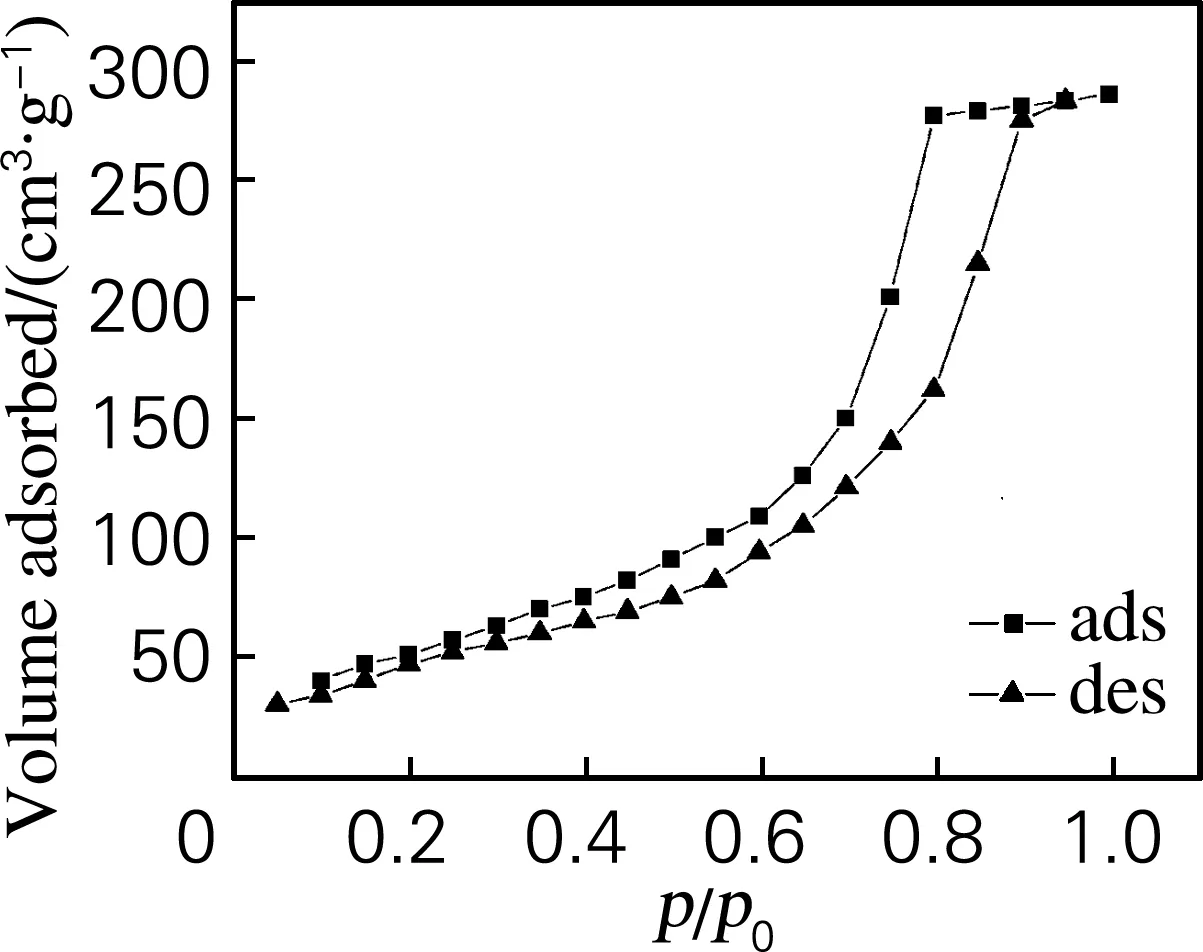
(c) n([C6mim]Br)∶n(HAuCl4)=2∶1
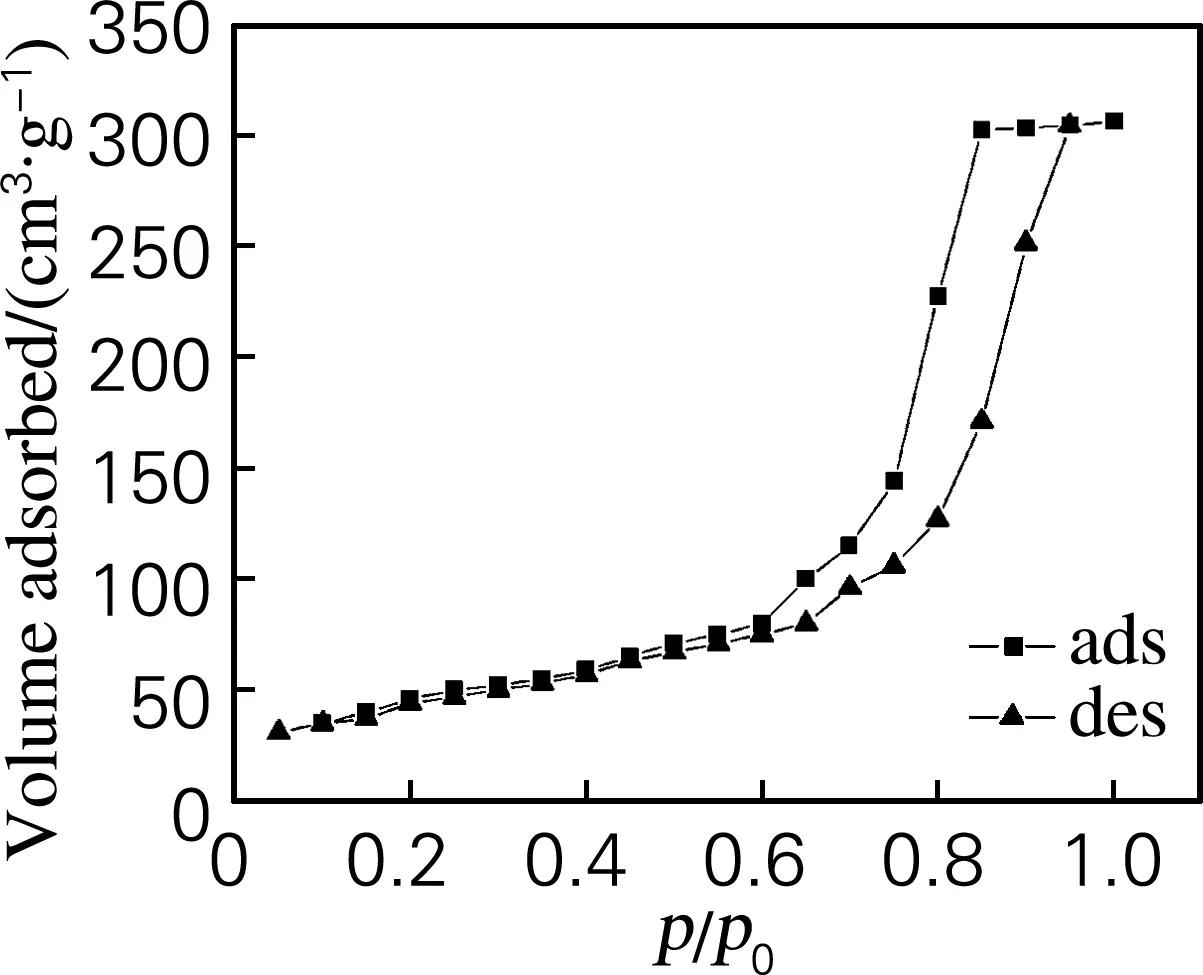
(d) n([C6mim]Br)∶n(HAuCl4)=5∶2
Fig.2 N2adsorption-desorption isotherms at different ionic liquids dosage
在p/p0低于0.5的低压段,曲线相对平缓,N2分子以单层到多层吸附于介孔内表面。
表1 不同摩尔比离子液体合成样品煅烧后的结构数据
Tab.1 Textural data of the support calcined at different ionic liquids dosage
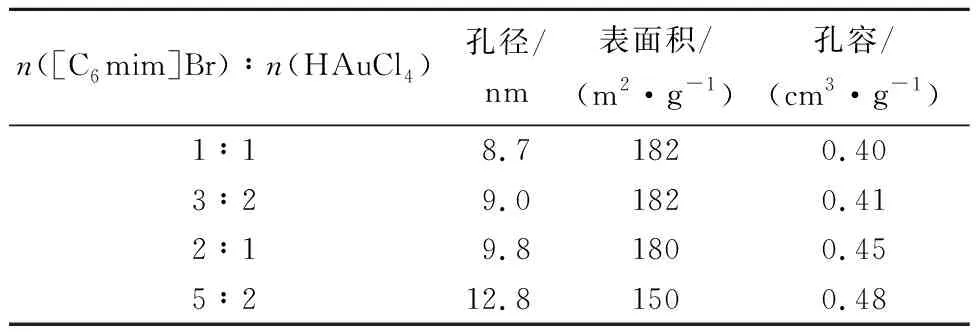
n([C6mim]Br)∶n(HAuCl4)孔径/nm表面积/(m2·g-1)孔容/(cm3·g-1)1∶13∶22∶15∶28.79.09.812.81821821801500.400.410.450.48
由表1可见,随着离子液体用量的增加,Au/SiO2的孔径增大,孔容增大。当离子液体用量n([C6mim]Br)∶n(HAuCl4)由1∶1增至2∶1时,Au/SiO2的表面积基本不变;当离子液体用量n([C6mim]Br)∶n(HAuCl4)增加到5∶2时,Au/SiO2的表面积急剧减小。表明离子液体在Au纳米粒子之间起着空间位阻作用,阻止了Au纳米粒子的团聚,确切地说是离子液体中的咪唑阳离子起着电子体阻隔稳定化作用。
2.1.3 透射电子显微镜分析
图3是所得Au/SiO2样品中n([C6mim]Br)∶n(HAuCl4)=2∶1时的透射电镜图。图中显示产物Au/SiO2中金颗粒的形貌为球形,颗粒尺寸比较均匀,其粒子(如图上箭头所指)为Au颗粒,粒径为2~3 nm。离子液体同时起到了分散剂和修饰剂的作用,阻止了纳米微粒的团聚。

图3 Au/SiO2样品的TEM图
2.2 催化剂应用
将离子液体和制备的Au/SiO2[n([C6mim]Br)∶n(HAuCl4)=2∶1]催化剂应用于甲烷氧化的反应中,通过测定甲烷反应前后的气相色谱计算转化率,由此来检测Au/SiO2的催化性能。
表2中是以离子液体为催化剂和离子液体及纳米金催化剂[n([C6mim]Br)∶n(HAuCl4)=2∶1]共同为催化剂,循环反应3次催化甲烷氧化的转化率。由表中的数据可知,仅以离子液体为催化剂时对甲烷的转化率很低,并且随着循环反应次数的增加明显降低,而以离子液体及纳米金催化剂共同为催化剂时,第3次转化率仍然能够达到21.8%,与第2次相比并无明显的下降。这表明Au/SiO2有良好的催化能力和稳定性,可以循环使用。

表2 甲烷催化转化率
3 结 论
通过使用自制的离子液体成功地合成了纳米Au/SiO2催化剂,表征结果显示,Au/SiO2中金颗粒有良好的分散度,呈球形,粒径在2~3 nm。离子液体在Au纳米粒子之间起着空间位阻作用,阻止了Au纳米粒子的团聚。将催化剂应用到甲烷氧化过程表明,Au/SiO2有良好的催化活性,甲烷的转化率最高可以达到24.9%,并可以循环使用。
[1] HARUTA M, TSUBOTA S, KOBAYASHI Y, et al. Low-temperature oxidation of CO over gold supported on TiO2,α-Fe2O3,and Co3O4[J]. Journal of Catalysis, 1993, 144(1):175-192.
[2] 邹汉波,董新法,林维明. 富氢气体中CO选择性氧化的研究进展[J]. 化学世界, 2005(6):367-370.
[3] SHI Jia-hua, SUN Xun, YANG Chun-he, et al. Electrochemical synthesis of polythiophene in a ionic liquid[J]. Chinese Chemical letters, 2002, 13(4):306-307.
[4] CHEN Yu-xi, FAN Qing-ming, LIU Ying-xin, et al. Advance in preparation and catalytic applications of metal nanoparticles stabilized by ionic liquids[J]. Technology & Development of Chemical Industry, 2008, 37(2):21-26.
