大马士革玫瑰花中非环单萜衍生物的研究
2012-05-07王辉
王 辉
(宝鸡文理学院化学化工系,陕西 宝鸡 721013)
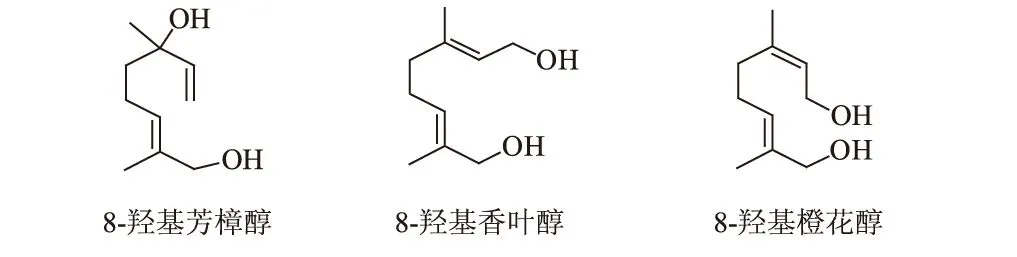
玫瑰(Rosa)为蔷薇科蔷薇属植物,在世界范围内种植很广,主要分布于北半球,以保加利亚、土耳其、摩洛哥、法国、俄罗斯等国家为主,我国亦有栽培[1]。玫瑰的品种繁多,有重瓣玫瑰、大马士革玫瑰、百叶玫瑰、香水月季、墨红、白玫瑰、木香花等,其中保加利亚的大马士革玫瑰含精油最多[2,3]。目前对大马士革玫瑰花的研究主要集中在玫瑰精油上,较少研究大马士革玫瑰花中的萜类化合物及其它化合物的生物合成途径。8-羟基芳樟醇(E-3,7-二甲基-1,6-辛二烯-3,8-二醇)、8-羟基香叶醇[(2E,6E)-3,7-二甲基-2,6-辛二烯-1,8-二醇]和8-羟基橙花醇[(2Z,6E)-3,7-二甲基-2,6-辛二烯-1,8-二醇]属单萜类化合物,具有较强的生物活性和浓郁的香气,是医药、化妆品和食品工业的重要原料,其中8-羟基香叶醇在萜类化合物的生物合成途径中具有非常重要的作用,是药用价值广泛的单萜吲哚类生物碱(如利血平、喜树碱等)生物合成的关键中间体,也是具有诸多生物活性的重要单萜化合物(如环烯醚萜苷)生物合成的重要前体[4,5]。这3个化合物在国产的大马士革玫瑰花中未见报道。
作者在此以陕西渭南产大马士革玫瑰花为研究对象,采用溶剂萃取法、柱层析分离法和高效液相色谱法分离大马士革玫瑰花中的化学成分,并利用GC-EI-MS和1HNMR分析鉴定大马士革玫瑰花中是否含有8-羟基芳樟醇、8-羟基香叶醇、8-羟基橙花醇。
1 实验
1.1 材料、试剂与仪器
大马士革玫瑰花(R.damascena)采自渭南白杨区玫瑰精油厂种植区。
8-羟基芳樟醇、8-羟基香叶醇、8-羟基橙花醇,Alfa Aesar公司;氯仿(分析纯)、乙醚(分析纯)、正丁醇(分析纯)、75%乙醇(工业品),天津富宇精细化工厂;甲醇(分析纯),西安化学试剂厂;石油醚(分析纯),成都联合化工试剂研发所;乙酸乙酯(分析纯),天津化学试剂有限公司;甲醇(色谱纯),Burdick & Jackson公司;柱层析硅胶G(200目),青岛海洋化工集团公司。
Shimadzu GC2010型气质联用色谱仪,日本岛津公司;rts-5ms型色谱柱,RESTEK公司;2695型高效液相色谱仪、2696型紫外检测器,Waters 公司;HC-C18色谱柱,Agilent公司;BP221S型微量电子天平,Sartorius公司;DT-1000型电子天平,北京医用天平厂;RE-52A型旋转蒸发仪,上海亚荣生化仪器厂;SHB-3型循环水多用真空泵,郑州长城科工贸有限公司;WG71型电热鼓风干燥箱,天津泰斯特仪器有限公司;INOVA型核磁共振仪(400 MHz),美国Varian公司。
1.2 大马士革玫瑰花中化学成分的提取分离
取新鲜大马士革玫瑰花10 kg,用75%乙醇于室温提取2次,每次提取7 d,合并2次提取液,减压浓缩成浸膏后加水混悬,依次用石油醚、乙酸乙酯、正丁醇萃取,再将石油醚和乙酸乙酯萃取物合并,减压蒸发得浸膏后分散于水中,用乙醚萃取,分离出乙醚层。
将乙醚浸膏(约16 g)经过硅胶色谱柱,用氯仿-甲醇梯度洗脱得到10个组分(Fr1~Fr10)。将Fr2(2.2 g)反复经硅胶色谱柱,用石油醚-乙酸乙酯(5∶1~2∶1)梯度洗脱得化合物Ⅰ(10 mg);将Fr2(3.0 g)反复经硅胶色谱柱,用石油醚-乙酸乙酯(3∶1~1∶1)梯度洗脱,得一混合物,经HPLC进一步分离得化合物Ⅱ(6 mg)和化合物Ⅲ(7 mg)。通过GC-EI-MS和1HNMR分析化合物Ⅰ、Ⅱ、Ⅲ。
大马士革玫瑰花中化学成分的分离提取流程见图1。

图1 大马士革玫瑰花中化学成分的分离提取流程
1.3 GC-EI-MS条件
GC条件:rts-5ms毛细管色谱柱(30 m× 0.25 mm,0.25 μm);载气为高纯氦气(99.999%),氦气流速1.0 mL·min-1;进样方式为分流进样;进样口温度320 ℃;柱箱温度60 ℃;压力100 kPa;总流量35.2 mL·min-1;柱流量1.61 mL·min-1;线速度46.3 cm·s-1;吹扫流量3.0 mL·min-1;分流比19.0。程序温度:初始60 ℃,保持2 min;以5 ℃·min-1升至300 ℃,保持10 min。
质谱条件:电子源为EI;EI电子能量为70 eV;离子源温度180 ℃;接口温度300 ℃。
1.4 HPLC条件
检测波长210 nm;上样量50 μL(1 mmol·L-1);流速0.75 mL·min-1;流动相:流动相A为甲醇,流动相B为水,0 min,50%A→20 min,90%A→30 min,50%A→35 min,50%A。
2 结果与讨论
2.1 化合物Ⅰ的鉴定
化合物Ⅰ的1HNMR(400 MHz,CDCl3),δ,ppm:5.88(1H,dd,J=10.754 Hz,10.751 Hz,H-2),5.39(1H,t,H-6),5.21(1H,dd,J=17.3 Hz,1.2 Hz,H-1b),5.05(1H,dd,J=10.8 Hz,1.2 Hz,H-1a),3.98(2H,s,H-8),2.06(4H,m,H-4,H-5),1.66(3H,s,Me-C3),1.29(3H,s,Me-C7)。
化合物Ⅰ在GC上的保留时间为17.528 min。
在相同的GC-EI-MS条件下,标准品8-羟基芳樟醇的保留时间为17.575 min,且化合物Ⅰ的MS图与其MS图相似度为98%(图2),再结合1HNMR数据确定化合物Ⅰ为8-羟基芳樟醇。

图2 8-羟基芳樟醇标准品(a)与化合物Ⅰ(b)的MS图谱
2.2 化合物Ⅱ的鉴定
化合物Ⅱ的1HNMR(400 MHz,CDCl3),δ,ppm:5.40(2H,m,H-2,H-6),4.16(2H,d,J=7.0 Hz,H-1),3.99(2H,s,H-8),2.17(2H,m,H-5),2.08(2H,m,H-4),1.74(3H,s,Me-C3),1.68(3H,s,Me-C7)。
化合物Ⅱ在GC上的保留时间为21.500 min。
在相同的GC-EI-MS条件下,标准品8-羟基香叶醇的保留时间为21.680 min,且化合物Ⅱ的MS图与其MS图相似度为98%(图3),再结合1HNMR数据确定化合物Ⅱ为8-羟基香叶醇。

图3 8-羟基香叶醇标准品(a)与化合物Ⅱ(b)的MS图谱
2.3 化合物Ⅲ的鉴定
化合物Ⅲ的1HNMR(400 MHz,CDCl3),δ,ppm:5.35(2H,m,H-2,H-6),4.00(2H,d,J=7.3 Hz,H-1),3.91(2H,s,H-8),2.07(4H,m,H-4,H-5),1.67(3H,s,Me-C3),157(3H,s,Me-C7)。
化合物Ⅲ在GC上的保留时间为21.093 min。
在相同的GC-EI-MS条件下,标准品8-羟基橙花醇的保留时间为21.192 min,且化合物Ⅲ的MS图与其MS图相似度为95%(图4),再结合1HNMR数据确定化合物Ⅲ为8-羟基橙花醇。

图4 8-羟基橙花醇标准品(a)与化合物Ⅲ(b)的MS图谱
3 结论
利用GC-EI-MS 和1HNMR鉴定出大马士革玫瑰花中所含的3个非环单萜类化合物分别为:8-羟基芳樟醇、8-羟基香叶醇、8-羟基橙花醇。为研究玫瑰花中萜类化合物的生物合成途径提供了有效的工具,也为大马士革玫瑰花中主要香气成分的分析提供了新的方法。
参考文献:
[1] 李万英,王文中.我国玫瑰资源初探[J].园艺学报,1983,10(3):211-215.
[2] 王威,王春利.天然玫瑰鲜花应用的研究[J].农牧产品开发,1999,(10):24-26.
[3] 马希汉,王永红,胡亚云,等.精油玫瑰研究[J].西北林业学院学报,2004,19(4):138-141.
[4] Oudin A,Courtois M,Rideau M,et al.The iridoid pathway inCatharanthusroseusalkaloid biosynthesis[J].Phytochem Reviews,2007,6(2-3):259-276.
[5] Galvez M,Martin-Cordero C,Ayuso M J.Pharmacological activities of iridoids biosynthesized by route Ⅱ[J].Studies Nat Prods Chem,2005,32:365-394.
