甲氨喋呤联合来氟米特治疗活动性类风湿关节炎疗效观察
2012-04-11王贯虹孟力平
赵 颖 ,王贯虹,孟力平
(大同市第五人民医院风湿免疫科,山西大同037006)
类风湿关节炎(rhemmatid arthritis,RA)是一系统性炎性疾病,主要侵犯关节的滑膜,使滑膜过度增殖并破坏软骨、骨和韧带等关节结构。RA致残机会较大,生命存活期往往缩短。RA患者确诊时关节已有损害造成不可逆的程度,有报道未及时诊治的RA患者,2年致残率达50%,3年致残率达70%。与同龄人相比,平均寿命缩短10~15年,故RA的治疗,强调早期、联合用药及个体化方案的原则。本实验通过对活动性RA患者进行为期12周和24周的甲氨蝶呤联合来氟米特与单用甲氨蝶呤对比,观察两组的疗效及安全性。
1 资料与方法
1.1 病例选择
200901-201001大同市第五人民医院门诊及病房收治的RA患者90例,年龄18~65岁,随机分为两组,联合用药组45例,单药组45例。纳入标准包括:①入选患者均符合美国风湿病学学会(ACR)于1987年修改后的诊断标准;②处于活动期标准即满足以下4条:晨僵持续时间60 min;3个或以上关节肿胀;8个或以上关节触痛;红细胞沉降率(ESR)≥28 mm/h或c反应蛋白(CRP)≥正常上限的1.5倍;③入选前1月未使用任何慢作用药物(DMARDS),使用激素则必须持续在强的松剂量10 mg/d以下,使用非甾类抗炎药(NSAIDS)则稳定持续给予相同剂量4周;④排除标准:合并有其他风湿性疾病如系统性红斑狼疮、干燥综合征等;近5年内有恶性肿瘤;患急慢性感染患者;肝肾功能异常者及患有心肺脑疾病的患者;过敏体质者;入选前4周内使用过肌肉注射或静脉滴注糖皮质激素;4周内使用过生物制剂者。
1.2 治疗方法
联合用药组:MTX每周7.5~10 mg 1次,口服,LEF每日20 mg 1次,口服。单用MTX组:MTX每周10~15 mg 1次。同时患者可以继续给予相同或不同的消炎镇痛药及小剂量糖皮质激素。严禁使用其他DMARDS药物及生物制剂(如抗TNF-a制剂和抗 IL-1Ra 制剂)。
1.3 观察项目
观察28组关节:颈颌、胸锁、肩锁、肩、肘、腕、掌指、拇指、远端指间、近端指间、髋、膝、踝、近端/远端趾间关节。治疗第12周、24周后记录上述28组关节关节肿胀计数、病人疼痛、晨僵时间、病人对疾病活动性的整体评价 (VAS)、医生对疾病活动性总体评价 (VAS)、健康评估问卷(HAQ)、血沉(ESR)、C 反应蛋白(CRP)。
1.4 实验室指标
定期检测血、尿常规,肝肾功能,ESR,CRP。
1.5 疗效评价
①评估RA的改善用美国风湿病学会推荐的RA改善标准:a.肿胀关节数;b.压痛关节数;c.急性期反应物(ESR和CRP);d.疼痛度(使用目测对数表VAS);e.VAS疾病严重性综合评估。 f.功能评估(使用健康调查评估问卷),如果病人在4个方面改善了20%、50%或70%,即病人达到ACR20、ACR50或ACR70改善标准。②主要疗效评价即指治疗12周及24周时两组分别达到ACR20改善标准的患者百分数;③次要疗效评价即指治疗12周及24周时两组分别达到ACR50改善标准的患者的百分数以及具体各项目,包括关节疼痛指数、关节肿胀数目、晨僵时间、患者对疼痛的评价 (VAS)、患者对疾病活动性的总体评价 (VAS)、医生对疾病活动的总体评价(VAS)、健康评估问卷 (HAQ),以及急性期反应物(ESR、CRP)。
1.6 安全性评价
观察在试验期间的药物不良反应,分析不良反应与药物的因果关系,并根据不良反应的发生率及严重性,比较所用药物的安全性及耐受性。
1.7 统计学处理
所有结果均采用SPSS13.0进行统计分析,计数资料采用x2检验,组间比较采用单因素方差分析,检验水准为P=0.05。
2 结果
2.1 一般情况
90例RA入选患者有2例联合用药组12周化验肝功能明显异常,期间减少药物剂量2周,之后恢复正常用量。2组均有部分患者口服小剂量泼尼松(10 mg/d)治疗,两组之间口服泼尼松患者比率无统计学差异。
2.2 疗效评价
主要疗效评价即ACR20结果见表1~3。
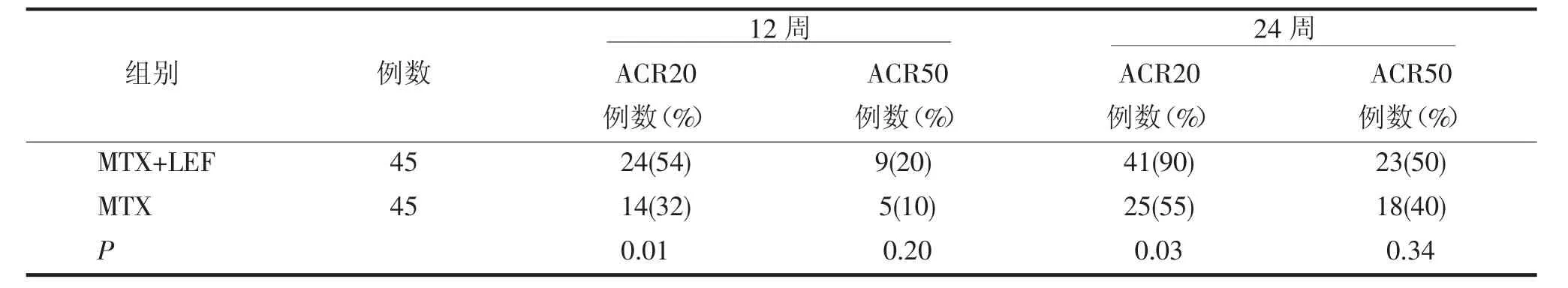
表1 两组ACR评估指标比较
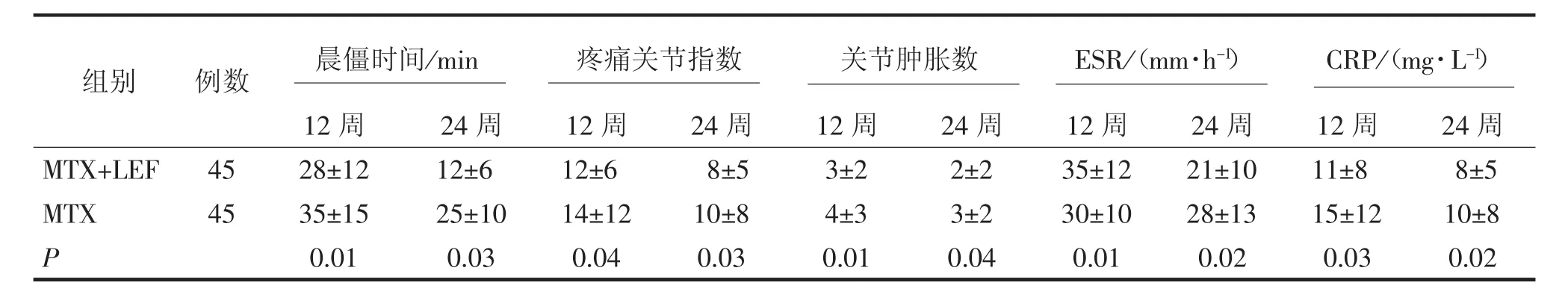
表2 治疗后两组临床症状及炎性指标比较(x2±s)
2.3 药物安全性
在24周入选期间,未发现明显的不良反应如严重感染、骨髓抑制(如白细胞及血小板减少)、皮疹、胃溃疡,出现的主要不良反应包括胃肠道症状(食欲减退、腹泻、恶心、胃炎)、肝酶升高、口腔溃疡、可逆性脱发、白细胞减少,给予对症处理均好转。其中导致减药的重要不良反应为肝酶升高,2例MTX+LEF出现肝酶上升达正常值2倍以上,减少药物剂量同时给予保肝药后观察2周,恢复正常。出现的不良反应无统计学差异。
3 讨论
RA最终治疗目标是阻止骨质的破坏进程,改善已经破坏的骨质,MTX可减慢骨破坏进展,但对于缓解骨质的破坏并不是一个理想的药物,因此多主张与DMARDS药物联合使用。由于MTX是单独使用最有效的药物,因此成为联合用药核心[1]。
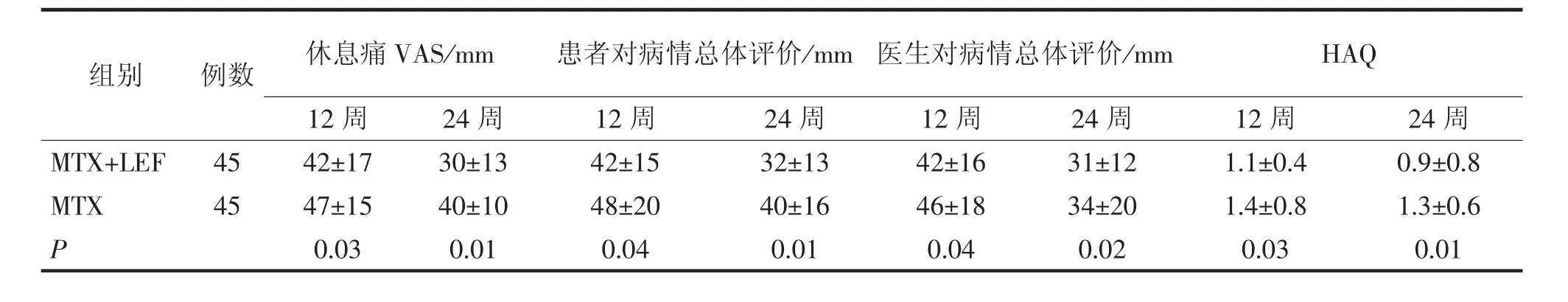
表3 治疗后两组病情评价比较(x2±s)
MTX是叶酸类似物,对二氢叶酸还原酶有高度亲和力,结合后抑制该酶活性,阻止二氢叶酸还原为四氢叶酸,使胸腺嘧啶核苷酸和嘌呤核苷酸的合成原料耗竭,阻断DNA和RNA合成。有抗炎及抗免疫作用,抑制参与免疫或炎症反应的细胞增殖和诱导凋亡是作用第一步,持续抗炎作用的关键在于对单核或淋巴细胞因子的抑制。
2002年ACR的RA治疗指南中将MTX作为治疗RA的基础药物。2007年Verstappen[2]等在一项为期2年的多中心开放性研究中发现,早期RA患者在给予MTX治疗后,2年内有37%~50%的患者可达到疾病缓解。Van Dongen等[3]报道在疾病早期给予MTX治疗可有效减缓RA患者关节损害的放射学进展。Braun等[4]也报道MTX治疗RA具有良好的疗效。在我们的实验两组药物对比中,发现单用MTX治疗后,患者的临床症状及急性炎症指标均有所改善,治疗24周后ACR50达40%,与上述文献报道相一致。
传统的治疗方案称为金字塔疗法,治疗一般从金字塔底开始,即最初给予单一的DMARDS药物,根据疗效再逐一增加药物,此时往往造成治疗时机的错失,故只注意治疗药物的副反应,而较少注意DMARDS药物对疾病严重后果进展的阻止。从20世纪的后10年,注意到DMARDS的早期使用及联合治疗,这些药物之间或产生协同作用,或作用于疾病病理生理过程不同环节,使得总体副反应降低。
LEF是异恶唑衍生物,具有免疫调节和抗增殖活性,1998年被FDA批准用于类风湿关节炎的治疗。LEF的活性代谢产物A77 1726抑制线粒体酶——二氢乳酸盐脱氢酶(DHODH),此酶在嘧啶核苷酸尿苷-磷酸的合成中有重要作用,进一步阻止淋巴细胞聚集足够嘧啶,从而影响DNA的合成,最终淋巴细胞的增殖受抑制。另外A77 1726可以抑制酪酸激酶活性,从而影响G0/G1期T、B淋巴细胞活性。
LEF可以抑制嘧啶的合成,调节淋巴细胞的增殖,而甲氨蝶呤抑制细胞因子的产生和嘌呤的生物合成并且需要腺苷的释放。由于MTX和LEF作用于不同的环节,二者联合使用将产生协同作用。本实验的数据表明:MTX联合LEF治疗RA可显著改善患者的疾病总体活动度,24周ACR20达90%,ACR50达50%,较单用MTX高,且ACR20有统计学差异。具体观察项目中临床症状即治疗后关节肿胀数及关节压痛指数较单用MTX组有显著差异。炎性实验室指标ESR、CRP下降,改善患者关节功能状态,通过健康评估问卷显示患者的生活质量有提高,且疗效优于单用MTX。治疗第12周及24周,次要疗效指标中各具体项目均有改善且联合用药组改善较单药组高,相比有统计学差异。
国外有学者[5]将MTX与LEF联合治疗类风湿关节炎后发现其有效性优于单用MTX,但考虑到合用后可能增加不良事件的发生率,他们相应的减少了2种药物的治疗剂量,结果发现严重不良事件的发生率与单药相比无明显增加。提示MTX,LEF对改善RA的病情有相互协同的作用。
本实验最终结果也表明,MTX联合LEF治疗RA中尽管有不良反应,但并不是很严重,具有较好的安全性和耐受性。与单用MTX相比,治疗后出现相关的不良反应发生率差异无统计学意义,无明显骨髓抑制、感染、肿瘤、皮疹等发生,不良反应最常见为胃肠道反应 (腹泻、恶心、胃炎)、肺部症状(咳嗽、呼吸困难、感染)、肝酶异常、口腔溃疡、可逆性脱发、白细胞减少,多数不良反应较轻,且为一过性,给予相应对症处理后缓解。本实验亦发现胃肠道反应为常见不良反应,主要表现为食欲下降、上腹部不适、恶心,严重者为呕吐,上述症状多在服药最初出现,持续时间达3~4 d,严重者可持续1周,且给予口服叶酸片10 mg qd,以及肌注胃复安,1~2 d后上述症状均可消失,之后继续用药中会逐渐较少。另外常见不良后果为肝酶异常,减少两药剂量同时加用保肝药可好转。本实验有2例联合用药者出现肝酶增高达正常值2倍,减少两药剂量及给予保肝治疗,观察2周后恢复正常,继续给予原剂量药物,未再出现肝酶增高。
目前有多个临床试验显示MTX联合LEF治疗RA安全性好,疗效比单独应用MTX或LEF更突出[6]。
[1]蒋明,林孝义,朱立平.中华风湿病学[M].北京:科学出版社,2004.
[2]Verstappen S M M,Jacobs J W G,Van der Veen M J,et a1.Intensive treatment with methotrexate in early rheumatoid arthritis:aiming for remission.Computer Assisted Management in Early RheumatoidArthritis(CAMERA.an open-label strategy trial)[J].AnnRheum Dis,2007,66(11):1443-1449.
[3]Van Dongen H,Van Aken J,Lard L I L,et a1.Efficacy of methotrexate treatment in patients with probable rheum atoidarthritis:a double-blind,randomized,placebo-controlled trial[J].Arthritis Rheum,2007,56(5):1424-1432.
[4]Braun J,kaslner P,Flaxenberg P,et a1.Comparison of the Clinical efficacy and safety of subcutaneous vergus oral administration of methotrexate in patients with active rheumatoid arthritis:resuits of a six-month,multicenter,randomized,double-blind,controlled,phaseⅣtrial.Arthritis Rheum,2008,58(1):73-81.
[5]Kremer J M,Genovese M C,Grant W,el a1.Concomitant leflunomide therapy in patients with active rheumatoid arthritis despite stable doses of methortexate[J].Ann Intem Med,2002,137(9):726-733.
[6]朱霞.类风湿关节炎的治疗进展[J].广西医学,2006,28(1):15-16.
