IMRT治疗颈段和胸上段食管癌的临床探讨
2012-02-09白玉,王颖
白 玉,王 颖
(重庆市肿瘤研究所放疗科 400030)
颈段及胸上段食管癌由于其解剖位置的特殊性,三维适形放射治疗常常不能兼顾满足肿瘤靶区照射剂量的同时很好地保护脊髓、肺等周围正常组织,而涉及照射野的衔接时更是容易造成剂量冷点或热点。适形调强放射治疗(intensity modulated radiation therapy,IMRT)是近几年发展起来的一项先进放射治疗技术,通过调整其照射野内各点的输出剂量率,实现高剂量的等剂量线面与靶区形状在三维空间上的一致,而靶区之外的剂量急剧下降,从而实现正常组织的最低剂量照射,肿瘤的照射剂量提高,进而提高局部控制率,真正达到精确放疗的目的。现将本科IMRT治疗颈段和胸上段食管癌的疗效报道如下。
1 资料与方法
1.1 一般资料 2006~2009年49例经病理学确诊为食管癌患者,卡氏评分均大于或等于70分,其中,男35例,女14例;年龄30~75岁,中位年龄45岁。鳞癌45例,腺癌4例,综合超声内镜、胸部CT、MRI、食管吞钡片及临床其他检查进行分期:Ⅰ期3例,Ⅱ期25例,Ⅲ期21例。
1.2 治疗方法 医用直线加速器为美国瓦里安23EX,所有49例患者均不愿或不适宜手术,全部患者均同意接受根治性放射治疗剂量。
1.3 体位固定和CT扫描 患者在CT模拟机上取仰卧位,双手上举抱肘,置于头颅两侧,采用热塑体膜、个体化塑料枕头固定头、颈部并做好标记。采用增强CT扫描,层厚3mm;扫描范围为环状软骨至胃底部。
1.4 靶区勾画 依据国际辐射学单位委员会(ICRU)50号文及62号文报道,在所有CT层面上逐层勾画,肿瘤范围(gross tumor volume,GTV)包括原发病灶(GTV-T)和肿大转移淋巴结(GTV-N)[1];临床靶区(clinical target volume,CTV)包括原发病灶临床靶区(CTV-T)、肿大转移淋巴结临床靶区(CTVN)及预防照射淋巴引流区(CTV-N1),范围为在GTV基础上横向外扩0.8~2cm,纵向外扩3~5cm,肿大转移淋巴结周围外放1.5~2.0cm;计划靶区(planning target volume,PTV)是在临床靶区基础上各个方向外放0.5~0.8cm,主要是考虑治疗过程中器官运动、照射野误差及摆位误差等[2-4]。同时由于原发肿瘤大小不一,个别情况下需适当缩小外扩范围以保护周围危及组织器官(如脊髓及肺等)。
1.5 靶区剂量的优化及评价指标 食管原发肿瘤及肿大转移淋巴结处方剂量为64~68Gy共32~34次,2Gy/次,5次/周。通过VARiAN系统剂量体积直方图(dose volume histogram,DVH)观察并优化肿瘤靶区和危及器官的剂量体积关系,95%(D95)剂量体积范围包绕CTV。通过照射适形指数(radiation conformal index,RCI)来观察照射野的适形程度,RCI=GTV体积/V95%,V95%为95%等剂量曲线包绕的体积。同时计算各个靶区的剂量分布,尤其是对危及器官进行剂量优化,包括最大、最小剂量和平均剂量及相关剂量参数等,因为危及器官的耐受剂量将影响整个治疗计划。治疗前,每例患者均须进行质量控制和质量保证的验证。
2 结 果
2.1 各个IMRT治疗靶区的实际受量 见表1。
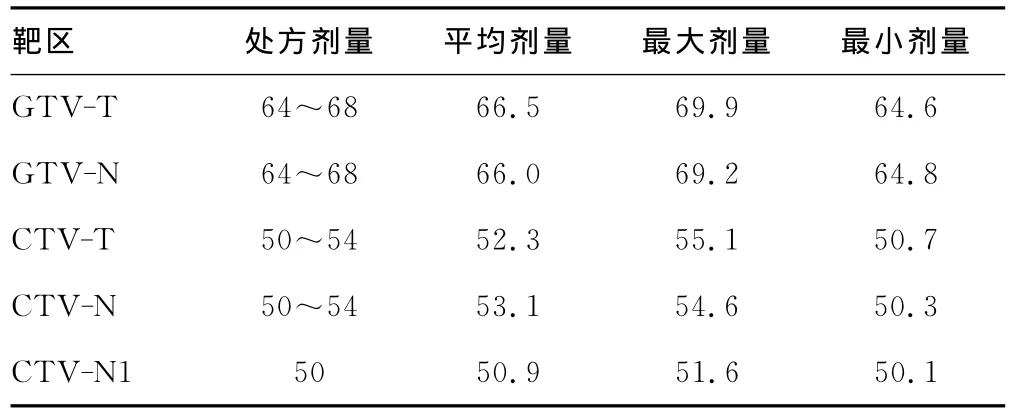
表1 靶区的处方剂量及实际剂量(Gy,n=49)
2.2 周围重要组织器官实际受量 以脊髓最大受照剂量40 Gy作为评价脊髓受量的参考指标,以V20(肺受照剂量为20 Gy所覆盖的肺的体积)及V5作为评价肺受照体积和剂量的参考指标。从表2可以看出所有危及器官受量均在比较理想的耐受剂量范围内。
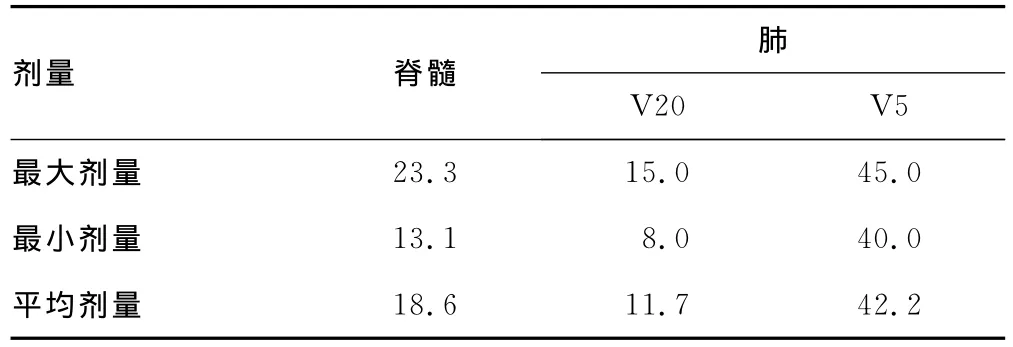
表2 脊髓和肺的指标(Gy)
2.3 疗效评价及观察指标 放疗期间按照肿瘤放射治疗协作组(radiation therapy oncology group,RTOG)急性放射反应评分标准对患者不良反应进行评价。治疗后3个月按实体瘤近期疗效客观评价标准进行评价,分为完全缓解(CR)、部分缓解(PR)及无变化(NC)[5]。完全缓解(CR)即食管原发肿瘤和肿大转移淋巴结完全消退,持续4周以上;部分缓解(PR)即食管原发灶和肿大转移淋巴结缩小50%以上;无变化(NC)即食管原发灶和肿大转移淋巴结增大大于25%或出现新病灶。所有患者均有吞咽疼痛、进食困难等症状,部分患者出现刺激性干咳或痰难咳出等症状,未出现放射性肺炎发生患者。其中,34例为1~2级,15例为3~4级,其中5例出现严重黏膜炎症而暂停放疗5~8d,所有患者均完成全部放疗计划。近期疗效:CR 41例,PR 8例,总有效率(CR+PR)=100%。采用门诊随访和电话随访结合方式,失访3例,随访时间8~20个月。
3 讨 论
3.1 IMRT优势 是通过对照射野内的各点输出剂量率的调整,使其在三维空间体积上高剂量等剂量线面与靶区剂量分布完全一致,即靶区边缘剂量分布锐利,使靶区之外剂量迅速降低,这样既能使肿瘤靶区得到高剂量照射,而邻近正常组织器官又能得到很好保护。与常规放射治疗比较,IMRT在局部控制率上得到极大提升,同时由于周围正常组织器官受照射剂量减低,患者对急性放射治疗反应的耐受也有较大提高,近期疗效也较常规放射治疗好。
3.2 靶区的准确勾画 GTV包括食管原发灶和肿大转移淋巴结。原发灶靶区的勾画依靠CT或MRI以及临床各种资料来确定。由于颈段及上段食管解剖位置的特殊性,影响靶区确定的因素较多,同时因IMRT具有在靶区与周围正常组织间剂量曲线锐利的特点,为避免漏照及严重不良反应,靶区由放疗科医师和放射诊断学医师共同确认。CTV是在GTV基础上外放一定的范围,由于食管癌常为多中心起源以及跳跃式转移,因此,CTV范围原则上应在GTV基础上横向外扩0.8~2 cm,纵向外扩3~5cm,肿大转移淋巴结周围外放1.5~2.0 cm。但由于上段食管解剖的特殊性以及周围危及器官的因素,CTV并不是单纯的外放一定距离,作者根据食管癌的放射治疗经验,在不影响危及器官的条件下,尽量扩大靶区的照射面积;PTV是在CTV基础上各个方向外放1cm,但处理原则仍按照CTV的勾画原则,兼顾靶区照射面积和危及器官的保护,尤其是淋巴结的预防照射区充分考虑到隐性转移灶,因而,在危及器官剂量允许范围内给予最大的预防照射范围以充分包括淋巴结区。靶区勾画范围的不充分常是导致局部复发的根源之一。
3.3 总剂量与剂量分割问题 Wang等[6]报道了7例颈段及胸上段食管癌患者行IMRT后的不良反应,其治疗剂量每次为59.4~66.0Gy,1.8~2.3Gy/次,结果4例存活患者中有2例出现食管狭窄,1例出现食管气管瘘。Lee[7]研究结果显示,食管癌放射治疗后食管狭窄的发生率与其所受照射的总剂量密切相关。作者采用总剂量64~68Gy共32~34次,每次2 Gy,在随访时间内未出现食管狭窄及食管气管瘘患者。在评估总剂量及剂量分割上,充分利用DVH来优化,同时参考最大剂量、最小剂量、平均剂量及照射适形指数等来一起评价整个治疗计划,力求使靶区获得最大的治疗效应,而正常组织得到最大的保护。但最佳治疗剂量仍有待进一步深入研究。
3.4 设野问题 多篇文献报道IMRT在治疗食管癌上较3DCRT具有明显优势,无论是适形性,还是靶区剂量分布上,因
此,IMRT能获得更高的肿瘤控制率。Woudstra等[8]报道4野IMRT计划优于4野3D-CRT计划,而7野或9野IMRT计划可获得较好的靶区剂量分布和肺及脊髓的保护。傅卫华等[9]对2例上段食管癌患者实行加量调强放射治疗计划的研究报道指出,5、7、9野计划适形度及脊髓的保护上优于3野计划,尤以9野为甚;而4置于计划对于肺平均受量相近,差异无统计学意义,但9野计划明显减少了V20和V30。Nieder等[10]得到类似结果。在野数设置上,作者根据患者实际情况主要采用了7野和9野计划,并充分利用DVH来优化整个计划,以期获得最佳治疗效果。
3.5 危及器官受量问题 由于周围重要危及器官对整个IMRT治疗计划起着相当的影响作用,因此,在设定治疗方案时要充分考虑各相关组织器官本身的运动以及摆位误差。由于部分层面脊髓离靶区较近以及包括了较大范围肺组织,因此,对于靶区的外放距离进行了适当的缩小,但在缩野计划时充分考虑该部位的总剂量,以使得每个靶区得到完全的治疗剂量,即对于每个治疗计划要进行取舍、评估及优化[10]。
[1] Mizowaki T,Shimada Y.Optimal size criteria of malignant lymph nodes in the treatment planning of radiotherapy for esophageal cancer:evaluation by computed tomography and magnetic resonance imagine[J].Int J Radiat Oncol Biol Phys,1996,36(5):1091-1098.
[2] 王军,祝淑钗,韩春,等.1 162例食管癌病理标本亚临床病灶范围的研究[J].中华放射肿瘤学杂志,2007,16(5):629-632.
[3] Lorchel F,Dumas JL.Esophageal cancer:determination of internal target volume for conformal radiotherapy[J].Radiother Oncol,2006,80(3):327-332.
[4] 王澜,韩春,祝淑钗,等.食管癌常规照射与三维适形放疗的剂量学研究[J].中华放射肿瘤学杂志,2006,15(2):176-178.
[5] 孙燕.内科肿瘤学[M].北京:人民卫生出版社,2001:994-995.
[6] Wang SL,Liao Z,Liu H,et al.Intensity-modulated radiation therapy with concurrent chemotherapy for locally advanced cervical and upper thoracic esophageal cancer[J].World J Gastroenterol,2006,12(34):5501-5508.
[7] Lee NY.Intensity-modulated radiotherapy for head and neck cancer of unknown primary:toxicity and preliminary efficacy[J].Int J Radiat Oncol Biol Phys,2008,70(4):1100-1107.
[8] Woudstra E,Heijmen BJ,Storchi PR.Automated selection of beam orientations and segmented intensity-modulated radiotherapy(IMRT)for treatment esophagus tumors[J].Radio Oncol,2005,77(3):254-261.
[9] 傅卫华,王绿化,周宗玫,等.上段食管癌SIB-IMRT治疗计划比较[J].中国医学科学院学报,2003,25(3):337-342.
[10]Nieder CL,Milas K,Ang K.Tissue tolerance to radiation[J].Semin Radiat Oncol,2000,10(2):200-202.
