复方双氯芬酸辣椒巴布贴微生物限度检查方法的验证
2012-01-25郑汉平廖祥茹
王 薇,郑汉平,廖祥茹
复方双氯芬酸辣椒巴布贴含有双氯芬酸二乙胺、辣椒碱、冰片等,有较强的抗菌作用。依据《中国药典》2010年版[1],本文采用薄膜过滤法对复方双氯芬酸辣椒巴布贴进行细菌、霉菌及酵母菌计数的验证,去除其抑菌成分,使加菌回收达到满意的效果。
1 验证材料
1.1 样品 复方双氯芬酸辣椒巴布贴:规格: 1%,批号:20090118、20090510、20091115,广州军区武汉总医院药剂科制剂室生产。
1.2 仪器 HTY-2000集菌仪、可拆卸式薄膜过滤器(杭州高得医疗器械有限公司),微孔滤膜:孔径0.45 μm(杭州泰林生物技术设备有限公司),SW-CJ-IFD/T型洁净工作台、BSC-1300ⅡA2型生物安全柜(苏净集团安泰公司生产),PYX-DHS隔水式电热恒温培养箱(上海市跃进医疗器械厂),SPX-250B-Z生化培养箱(上海博讯实业有限公司医疗设备厂)。
1.3 培养基 营养琼脂培养基(批号:101130)、玫瑰红钠琼脂培养基(批号:100114)、营养肉汤培养基(批号:101213)、胆盐乳糖增菌液(批号: 091029)、改良马丁培养基(批号:1010122)、溴化十六烷基三甲铵琼脂培养基(批号:081219),北京三药科技开发公司,甘露醇氯化钠琼脂培养基(国药集团化学试剂有限公司,批号:20090713),蛋白胨(天津市英博生化试剂有限公司,批号: 051209)。
1.4 稀释剂 pH 7.0无菌氯化钠蛋白胨缓冲液、0.9%无菌氯化钠溶液,按中国药典2010年版二部附录方法配制。
1.5 菌种 大肠埃希菌(Escherichia coli)[CMCC(B)44102]第4代,金黄色葡萄球菌(Staphylococcus aureus)[CMCC(B)26003]第4代,枯草芽孢杆菌(Bacillus subtilis)[CMCC(B)63501]第4代,白色念珠菌(Candida albicans)[CMCC(F) 98001]第3代,黑曲霉(Aspergillus niger)[CMCC (F)98003]第4代,铜绿假单孢菌(Pseudomonas aeruginosa)[CMCC(B)10104]第3代。
2 菌液制备方法
接种大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌、铜绿假单胞菌的新鲜培养物至营养肉汤培养基中,置30~35℃培养18~24 h,分别取上述培养物1 mL,加0.9%无菌氯化钠溶液9 mL,10倍递增稀释制成每1 mL含菌数为50~100 cfu的菌悬液;接种白色念珠菌的新鲜培养物至改良马丁培养基中,置23~28℃培养24~48 h,取培养物1 mL,加0.9%无菌氯化钠溶液9 mL,10倍递增稀释制成每1 mL含菌数为50~100 cfu的菌悬液;接种黑曲霉的新鲜培养物至改良马丁琼脂斜面培养基中,置23~28℃培养5~7 d,加入5 mL含0.05%聚山梨酯80用0.9%无菌氯化钠溶液,将孢子洗脱。吸出孢子悬液至无菌试管内,取原液1 mL,加含0.05%聚山梨酯80的0.9%无菌氯化钠溶液9 mL,10倍递增稀释制成每1 mL含孢子数为50~100 cfu的孢子悬液。
3 供试液制备
取样品100 cm2,去掉贴剂的保护层,置于无菌玻璃片上,粘贴面朝上。用无菌纱布覆盖贴剂的粘贴面,避免贴剂粘贴在一起。将其置于适宜体积并含有聚山梨酯80的0.9%无菌氯化钠溶液中,用力振荡至少30 min,作为1∶10供试液,备用。
4 菌落计数方法的验证
4.1 常规平皿法、培养基稀释法
4.1.1 试验组 取1∶10供试液1、0.5 mL与各试验菌液(大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌、白色念珠菌、黑曲霉)1 mL,分别注入平皿中,立即倾注营养琼脂培养基和玫瑰红钠琼脂培养基,每株试验菌平行制备2个平皿,分别置30~35℃培养3 d、23~28℃培养5 d,按平皿法测定其菌数。
4.1.2 菌液组 分别取上述稀释的试验菌液1 mL注入平皿内,每种试验菌平行制备2个平皿,测定所加的试验菌数。
4.1.3 供试品对照组 取1∶10供试液1 mL,按“4.1.1”项下操作,不加菌液,测定供试品的本底菌数。
4.1.4 稀释剂对照组 取稀释剂1 mL,按“4.1.1”项下操作。
4.1.5 结果 见表1、表2。可见常规平皿法3次试验5株菌株均受到了不同程度抑制,而用培养基稀释法每皿0.5 mL,部分菌仍受到抑制,说明常规平皿法和培养基稀释法均不能有效去除其抑菌成分,须重新建立细菌、霉菌及酵母菌计数方法的验证。

表1 常规平皿法回收率测定结果(%)

表2 培养基稀释法回收率测定结果(%)
4.2 薄膜过滤法
4.2.1 试验组 取1∶10供试液10 mL加入含100 mL稀释液的薄膜过滤器中全量过滤,用冲洗液(100 mL/次)冲洗4次。在最后一次加入1 mL (50~100 cfu)各试验菌(大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌、白色念珠菌、黑曲霉),取出滤膜,菌面朝上贴于已制备的营养琼脂培养基平板或玫瑰红钠琼脂培养基平板上,平行制备2皿,置30~35℃培养3 d或23~28℃培养5 d。逐日观察,按平皿法测定其菌数。
4.2.2 菌液组 分别取上述试验菌液1 mL注入薄膜过滤器内过滤,贴膜。每种菌平行制备2张滤膜,分别测定所加的试验菌数。
4.2.3 供试品对照组 取1∶10供试液10 mL,按“4.2.1”项下操作,不加菌液,测定样品本底数。
4.2.4 稀释剂对照组 取稀释剂1 mL,按“4.2.1”项下操作。重复试验3次。
4.2.5 结果 见表3。由表3可见,用400 mL冲洗时,各试验菌株的回收率均达70%以上。说明薄膜过滤法可用于复方双氯芬酸辣椒巴布贴的细菌、霉菌及酵母菌计数,冲洗量定为400 mL。
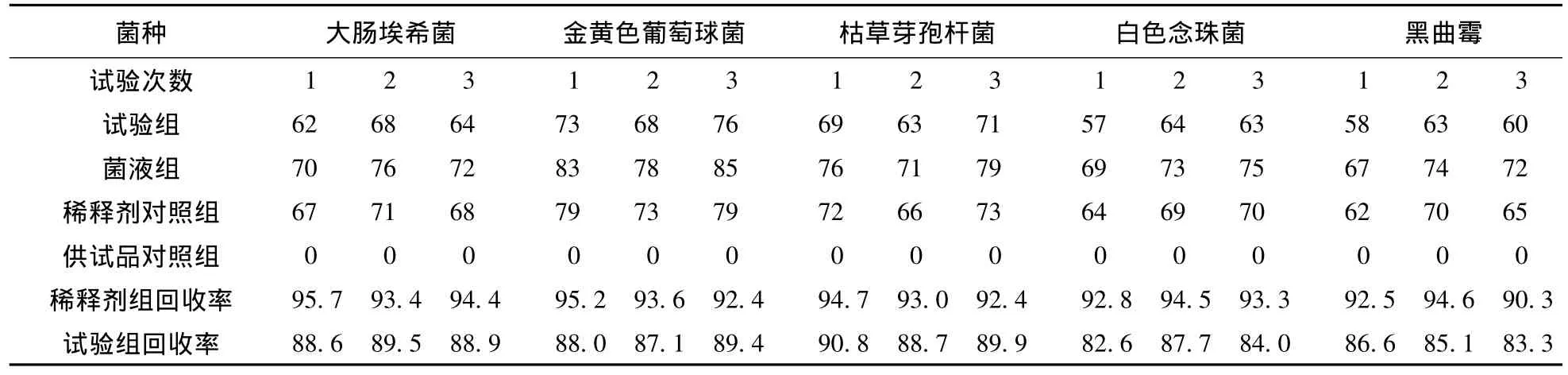
表3 薄膜过滤法回收率测定结果(%)
5 控制菌检查方法的验证
5.1 铜绿假单胞菌检查方法验证
5.1.1 试验组 取1∶10的供试液10 mL及铜绿假单胞菌菌液1 mL,接种至200 mL胆盐乳糖增菌培养基内,于35℃培养24 h。取上述培养物,划线接种于溴化十六烷基三甲胺琼脂培养基平板上,培养24 h,按相应控制菌检查法进行检查。
5.1.2 阴性菌对照组 取1∶10的供试液10 mL及大肠埃希菌菌液1 mL,接种至200 mL胆盐乳糖增菌培养基内,方法同“5.1.1”项。
5.1.3 结果 见表4。由表4可见,试验组检出铜绿假单胞菌,阴性菌对照组未检出大肠埃希菌。说明200 mL胆盐乳糖增菌培养基可以用于复方双氯芬酸辣椒巴布贴铜绿假单胞菌的检查。

表4 控制菌铜绿假单胞菌验证结果
5.2 金黄色葡萄球菌检查方法验证
5.2.1 试验组 取1∶10的供试液10 mL及金黄色葡萄球菌菌液1 mL,接种至300 mL营养肉汤培养基内,于35℃培养24 h。取上述培养物,划线接种至甘露醇氯化钠琼脂培养基的平板上,培养24~72 h,按相应控制菌检查法进行检查。
5.2.2 阴性菌对照组 取1∶10的供试液10 mL及大肠埃希菌菌液1 mL,接种至300 mL营养肉汤培养基内,方法同“5.2.1”项。
5.2.3 结果 见表4。试验组检出金黄色葡萄球菌,阴性菌对照组未检出大肠埃希菌。说明300 mL营养肉汤培养基可以用于复方双氯芬酸辣椒巴布贴金黄色葡萄球菌的检查。
6 讨论
6.1 稀释剂对照组的菌回收率均大于70%,说明采用含适量聚山梨酯80的pH 7.0无菌氯化钠-蛋白胨缓冲液作为稀释液对试验不产生干扰。
6.2 细菌、霉菌及酵母菌计数采用薄膜过滤法,取1∶10供试液10 mL加入含100 mL稀释液的薄膜过滤器中全量过滤,用冲洗液(100 mL/次)冲洗4次。此法可有效去除复方双氯芬酸辣椒巴布贴的抑菌成分。控制菌检查采用培养基稀释法,取1∶10的供试液10 mL分别接种至200 mL胆盐乳糖增菌培养基或300 mL营养肉汤培养基中,依法进行检查。
[1] 国家药典委员会.中华人民共和国药典(二部)[S].北京:人民卫生出版社,2010:附录107-116.
