龙胆泻肝丸溶出特性研究
2012-01-25周永全顾佳莹张宁
周永全,顾佳莹,张宁
(上海中医药大学,上海201203)
龙胆泻肝汤是收载于《医方集解》中的著名经典方,由龙胆、柴胡、黄芩、栀子和泽泻等十味药组成,具有清肝胆实火,泻下焦湿热的功效。用于治疗肝胆湿热,头晕目赤,耳鸣耳聋,耳肿疼痛,胁痛口苦,尿赤涩痛,湿热带下等症。该方的特点是泻中有补,降中寓升,去邪而不伤正,泻火而不伐胃[1]。目前临床上多使用的是丸剂、胶囊剂等固体剂型。固体制剂是通过药物中有效成分的溶出、溶解并被吸收后发挥作用。各有效成分的溶出情况是影响药物疗效发挥的重要因素。丸剂是中药传统剂型之一,丸剂释药多以缓慢释放为特点,复方中药中多种成分由于其理化性质不同,其溶出速率存在着明显差异,研究复方中药中有效成分的溶出特性,对于复方中药剂型选择具有积极意义。本实验对龙胆泻肝丸中主要药味中有效成分的溶出进行研究,并与胶囊剂的溶出进行比较,通过溶出模型拟合,探讨其释药机理,从而为诠释该制剂的药剂学内涵提供实验依据。
1 仪器与试药
Zb—lc型智能崩解仪(天津大学精密仪器厂);FA2004N型电子天平(上海精密科学仪器有限公司);CP225D型电子天平(Sartorius AG,上海精密科学仪器有限公司);Agilent—1200高效液相色谱系统(美国安捷伦公司);Thermo ODS—2 HYPERSIL C18色谱柱(4.6 mm×250 mm,5 μm)(上海安谱科学仪器);Rcz—6C2型药物溶出度仪(上海黄海药检仪器有限公司)。
栀子苷对照品(批号110749-200714)、龙胆苦苷对照品(批号110772-201013)、黄芩苷对照品(批号110715-201016)、阿魏酸对照品(批号110773-200611)上述对照品均购自中国药品生物制品检定所,定量测定用;龙胆泻肝丸(洛阳顺势药业有限公司,批号:20100902)、龙胆泻肝胶囊(湖北福人药业股份有限公司,批号:20101101)。
2 方法与结果
2.1 色谱条件
2.1.1 龙胆苦苷、黄芩苷、栀子苷[2]Thermo ODS-2 HYPERSIL C18色谱柱(4.6 mm×250 mm,5 μm);检测波长254 nm;流动相为1%冰醋酸水溶液为流动相A、乙腈为流动相B;体积流量1.0 mL/min;柱温为室温;进样量20 μL。
梯度洗脱流动相配比变化如表1所示。

表1 梯度洗脱流动相配比变化Tab.1 Variety of the mobile phase in gradient elution
龙胆泻肝丸溶出液中龙胆苦苷、黄芩苷、栀子苷等成分色谱图见图1。
2.1.2 阿魏酸色谱柱(Thermo ODS-2 HYPERSIL C18柱4.6 mm×250 mm,5 μm);检测波长321 nm;流动相为甲醇-1%冰醋酸(46∶54);体积流量1.0 mL/min;柱温为室温;进样量20 μL。龙胆泻肝丸溶出液中阿魏酸色谱图见图2。

图1 龙胆泻肝丸中栀子苷、龙胆苦苷、黄芩苷测定图谱Fig.1 Chromatogram of jasminoidin,gentiopicrin and baicalin in Longdan Xiegan Pills
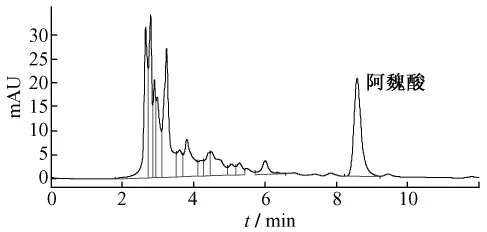
图2 龙胆泻肝丸中阿魏酸测定图谱Fig.2 Chromatogram of ferulic acid in Longdan Xiegan Pills
2.2 系统适用性试验
2.2.1 线性范围考察分别精密称取栀子苷、龙胆苦苷、黄芩苷的干燥对照品,加甲醇配制成每1 mL含栀子苷、龙胆苦苷、黄芩苷96.0、59.6、58.0 μg的混合对照品溶液;精密称取阿魏酸的干燥对照品,加甲醇配制成每1 mL含阿魏酸40.0 μg的对照品溶液。
精密吸取混合对照品溶液,用甲醇依次稀释制备其2倍、4倍、8倍、16倍、32倍和64倍系列质量浓度的对照品稀释溶液,按2.1.1项测定;吸取阿魏酸对照品溶液5 mL,同前法用甲醇稀释制备其2倍、4倍、8倍、16倍、32倍、64倍、128倍系列质量浓度的对照品稀释溶液,按色谱条件2.1.2项测定。以各成分质量浓度C为横坐标,相应峰面积A为纵坐标进行回归,栀子苷、龙胆苦苷、黄芩苷、阿魏酸的回归方程分别为A=12.46C-7.577、A=16.89C-3.789、A=21.28C-15.25、A=108.6C-9.697;相关系数分别为0.999 9、0.999 4、0.999 8、0.999 7;线性范围分别为1.50~96.0 μg/mL、0.931~59.6 μg/mL、0.906~58.0μg/mL、0.313~40.0 μg/mL。
2.2.2 精密度试验精密吸取上述各对照品溶液20 μL,分别注入高效液相色谱仪,重复测定6次,记录各成分的峰面积值,算得栀子苷、龙胆苦苷、黄芩苷、阿魏酸的RSD值分别为1.34%、1.65%、1.57%、0.83%。
2.2.3 稳定性试验精密吸取各对照品溶液20 μL,分别在0、2、4、6、8、10、12、24、36、48 h注入高效液相色谱仪测定,记录各成分的峰面积值,算得栀子苷、龙胆苦苷、黄芩苷、阿魏酸的RSD值分别为1.94%、1.77%、3.27%、1.75%。
2.2.4 丸和胶囊中4种成分的溶出量测定结合参考文献,本实验采用直接测定成分含有量的方法而最终计算出该值[3]。称取龙胆泻肝丸和胶囊,分别约为0.5 g和0.25 g,精密称定,置具塞锥形瓶中,精密加入50%的甲醇50 mL,密塞,称定质量。超声处理(250 W,50 kHz)20 min,放冷,再称质量,补足减失的质量,摇匀,以0.22 μm微孔滤膜滤过,取续滤液,参照2.1项进行测试。
龙胆泻肝丸中栀子苷、龙胆苦苷、黄芩苷、阿魏酸的质量分数分别为4.24、5.59、4.98、1.56mg/g;龙胆泻肝胶囊中栀子苷、龙胆苦苷、黄芩苷、阿魏酸的质量分数分别为6.36、7.00、1.01、2.66 mg/g。
2.3 溶出度考察
2.3.1 溶出条件的选择参考《中国药典》2010年版(二部)溶出度测定法,采用浆法;温度恒定在(37±0.5)℃,转速为100 r/min;4 h内的溶出介质采用新配的人工胃液。
2.3.2 溶出度的测定与结果龙胆泻肝丸:取新配制的人工胃液,超声,精密量取675 mL加入溶出杯中,恒温至(37±0.5)℃。取4份龙胆泻肝丸,每份约4 g,精密称定后放入溶出杯中,盖紧杯盖,启动转浆,转速100 r/min。分别在开启后15、30、45、60、90、120、180、240 min时,迅速吸取约2 mL溶出液(同时补充溶出介质2 mL),以0.22 μm微孔滤膜过滤后进HPLC检测。
龙胆泻肝胶囊:取龙胆泻肝胶囊8粒(含药约2 g)于溶出杯中,溶出条件、取样点、样品处理方法同龙胆泻肝丸。
对上述每个时间点累积溶出量进行校正后除以百分之百溶出量得相对累积溶出率,结果见表2、表3。

表2 龙胆泻肝丸中各成分相对累积溶出率(%,n=4)Tab.2 Cumulative dissolution percentage of the 4 compounds in Logdan Xiegan Pills(n=4)

表3 龙胆泻肝胶囊中各成分相对累积溶出率(%,n=3)Tab.3 Cumulative dissolution percentage of the 4 compounds in Longdan Xiegan Capsules(n=3)
由表2和表3可见,胶囊中各成分的溶出较丸剂快;丸剂中栀子苷和龙胆苦苷溶出比黄芩苷和阿魏酸快,2 h时,栀子苷和龙胆苦苷溶出约85%、黄芩苷和阿魏酸溶出约45%,之后溶出速度有所减缓;胶囊剂在0~30 min溶出较快,30 min以后溶出曲线趋于平缓,至2 h时溶出率达到99%(除阿魏酸)。
龙胆泻肝丸中,各指标成分的溶出情况比较结果见图3。

图3 龙胆泻肝丸中主要药效成分溶出曲线Fig.3 Dissolution curves of the effective composition in Longdan Xiegan Pills
从4种成分4 h的释放曲线可以看出,栀子苷和龙胆苦苷的溶出行为较为接近,明显比黄芩苷和阿魏酸释放的快且完全,这表明栀子和龙胆中的这两种成分更容易被吸收、起效。
龙胆泻肝丸剂与胶囊剂中各指标成分的溶出情况比较结果见图4~图7。
从丸剂与胶囊剂溶出情况看,丸剂中4种成分的溶出速度均比胶囊剂的慢,但至4 h时,丸剂中栀子苷、龙胆苦苷的溶出程度基本与胶囊剂相同而黄芩苷、阿魏酸的溶出程度明显低于胶囊剂。
2.3.3 溶出模型拟合本实验采用Excel(DEBS法)[4],从目前常用于缓控释制剂的释药动力学方程中,选择以下5种溶出模型对龙胆泻肝丸的释放分别进行拟合:
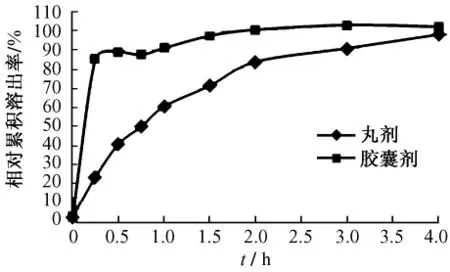
图4 栀子苷溶出度比较曲线图Fig.4 Dissolution curves of jasminoidin
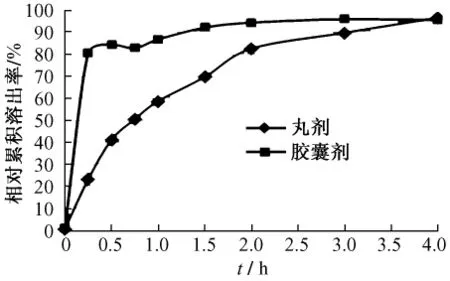
图5 龙胆苦苷溶出度比较曲线图Fig.5 Dissolution curves of gentiopicrin
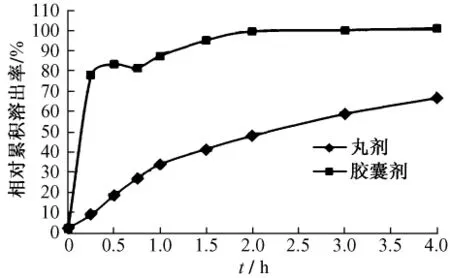
图6 黄芩苷溶出度比较曲线图Fig.6 Dissolution curves of baicalin

图7 阿魏酸溶出度比较曲线图Fig.7 Dissolution curves of ferulic acid
零级反应模型:Mt/M0=kt+b(k、b为所求参数)
一级反应模型:Mt/M0=1-EXP(-kt+b)(k、b为所求参数)
Higuchi模型:Mt/M0=k×t1/2+b(k、b为所求参数)
Ritger-Peppas模型:Mt/M0=k×tm+b(k、b、m为所求参数)
Weibull模型:Mt/M0=1-EXP(-(t-τ)m/t0)(τ、t0、m为所求参数)
其中,Mt/M0为溶出百分率、t为时间。
拟合结果如表4所示(表中的时间t均以min为单位):
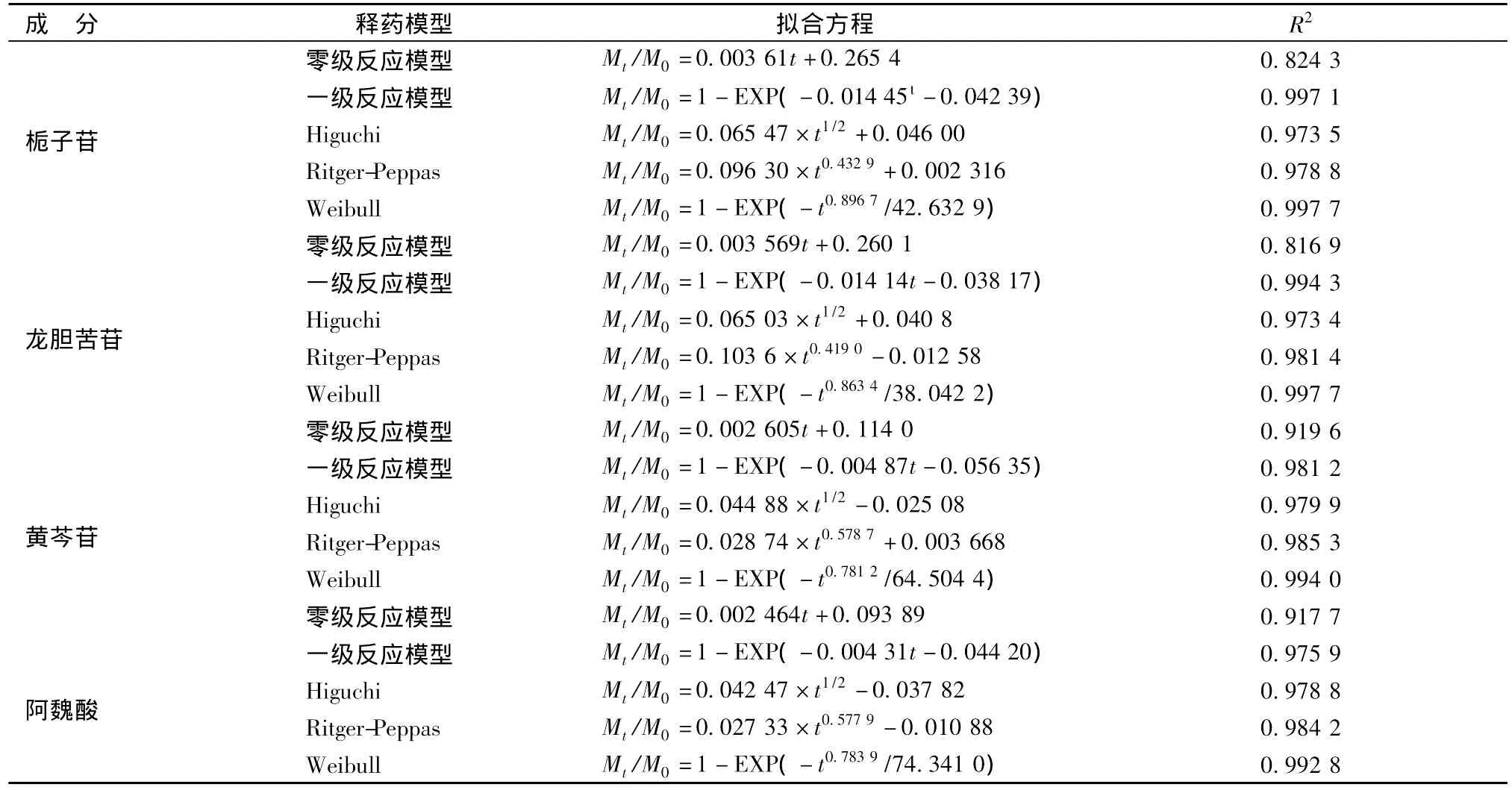
表4 龙胆泻肝丸4种成分溶出模型拟合结果Tab.4 Results of fitting dissolution models for 4 compounds in Longdan Xiegan Pills
由拟合结果可知,上述4种成分的溶出以用Weibull模型拟合最好,但一级反应模型、Higuchi模型、Ritger-Peppas模型拟合的相关系数也较高;据Ritger-Peppas模型数据判断,上述4种成分的溶出过程均不符合完全的骨架溶蚀机制(m>0.89者),黄芩苷和阿魏酸为非Fick's扩散(0.45<m<0.89者,扩散与溶蚀并存);栀子苷和龙胆苦苷为Fick's扩散(m<0.45者)。
3 讨论
本实验对龙胆泻肝丸中4种有效成分的体外溶出度进行了研究,结果表明:4 h时,丸中龙胆苦苷、栀子苷溶出较完全,而黄芩苷、阿魏酸分别溶出66.51%、61.68%,可见龙胆苦苷、栀子苷的溶出快于黄芩苷和阿魏酸。
溶出模型拟合结果表明:上述4种成分的溶出均以用Weibull模型拟合效果最佳,提示其溶出速率常数与扩散系数成正比,且随时间变化而变化,而介质的温度、体积等在溶出过程中均未改变,据上述可推测龙胆泻肝丸的溶出机制可能为非溶蚀的Fick's扩散。Ritger-Peppas模型拟合结果也表明龙胆苦苷和栀子苷按Fick's扩散机制溶出而黄芩苷和阿魏酸为非Fick扩散(扩散与溶蚀并存),但前两者溶出较快(栀子苷、龙胆苦苷的Td值分别为65.7、67.6 min,黄芩苷、阿魏酸的Td值207、235min),这4种成分的水溶性也有所不同:栀子苷易溶于水(溶解度大于10 g)、龙胆苦苷可溶于水(溶解度约为7.65 g)[5],其油水分配系数较小;黄芩苷、阿魏酸(主要是反式阿魏酸)的溶解度则较小(溶解度均小于0.1 g)[6-7],且两者均显酸性[8],其在酸性环境下的溶解度较小。而目前一般认为药物的溶解速率与药物溶解度成正相关[9],这可能是栀子苷、龙胆苦苷溶出更快的原因之一。
另外,Ritger-Peppas模型中的位置参数τ的意义是溶出延迟时间,其取值应在0~15 min(第1次取样时)之间,但研究发现:其取负值时相关系数更高,且在4个成分中有共性,这可能与取样等操作占用时间、各成分有一定水溶性等因素有关。
采用f2因子法考察溶出相似度,结果显示:丸剂中,栀子苷与龙胆苦苷的f2值为90,栀子苷与黄芩苷、阿魏酸的f2值分别为29、27,龙胆苦苷与黄芩苷、阿魏酸的f2值分别为30、27,黄芩苷与阿魏酸的f2值分为72,可以认为栀子苷与龙胆苦苷的溶出具有高度相似性、释放同步,黄芩苷与阿魏酸的溶出具有相似性、释放同步。
中药传统丸剂由于发挥作用慢,一般被认为是“缓释”制剂,在对龙胆泻肝丸及胶囊中4个成分释药行为的研究中发现,丸剂中上述成分在开始阶段溶出速率均慢于胶囊,但有些成分在后续阶段的溶出度与胶囊接近(如龙胆苦苷和栀子苷),可能是由于丸剂中加入的辅料阻碍了这些成分向水中扩散而影响其溶出,使该溶出过程与现代药剂学中某些由“骨架材料”制备的缓释制剂的溶出有类似之处,这也证实了中医药理论中“丸者缓也”的论述。实验中还发现丸中各种成分的溶出具有不同步性,这种差异与溶解度相关。
中药是复杂体系,丸剂作为中药传统剂型,其溶出特点有必要进行深入研究,本实验仅选择4种成分,有一定局限性,尚应借鉴一些新技术和方法(如定量指纹图谱、Kalman滤波法等基于组分学说的模糊类评价的方法等[10])以建立多个活性部位成分溶出(或释药)行为的考察。此外,本实验只是对药物在胃内溶出的一个体外模拟实验,与体内吸收存在一定差异性,药物在体内的吸收还与成分状态、多种酶的作用、跨生物膜性质、肠道吸收状况等多种因素有关。例如黄芩苷在碱性的肠道中溶出量理论上较大,但呈离子态增多而吸收减少,故黄芩苷的吸收主要在胃内,而其水溶性、脂溶性均较差,故其生物利用度较低[11];而龙胆苦苷、栀子苷溶出虽较为顺利,但由于其水溶性大、龙胆苦苷透膜性差而栀子苷存在首过效应,故这两者的口服绝对生物利用度也较低(小于10%)[12-13]。因此在体外溶出度研究的基础上,还应结合药理效应或生物效应等指标,才能解析中药丸剂剂型的科学内涵。
[1]谢鸣.方剂学[M].北京:人民卫生出版社,2002:124-126.
[2]郝福,蒋晔,李艳荣,等.HPLC法测定龙胆泻肝丸中龙胆苦苷、黄芩苷和栀子苷[J].中草药,2006,37(12):1808-1809.
[3]刘瑞新,张转建,孟祥乐,等.龙胆泻肝丸的溶出度研究及中药溶出度研究探讨[J].中医研究,2009,22(6):20-23.
[4]苏银法,陈洁华,白学敏,等.Excel规划求解法在药物溶出模型拟合和优选中的应用[J].中国医院药学杂志,2007,27(6):839-8841.
[5]赵文娜,尚平平,孙文基.HPLC法测定龙胆苦苷的表观油水分配系数[J].药物分析杂志,2009,29(7):1093-1095.
[6]欧水平,王森,张海燕,等.黄芩苷溶解性能的测定与表征[J].现代生物医学进展,2009,9(20):3954-3957.
[7]周彩荣,石晓华,王海峰,等.反式阿魏酸在溶剂中的溶解度[J].化工学报,2007,58(11):2705-2709.
[8]王弘,陈济民,张清民.黄芩苷的物化常数测定[J].沈阳药科大学学报,2000,17(2):105-106.
[9]刘汉清,李建新.中药固体制剂溶解速率要略[J].中成药研究,1986,9(1):42-43.
[10]翟羽,沈岚.中药固体制剂溶出度/体外释放度评价方法的研究进展[C]//2011年上海市研究生学术论坛“中医药创新与发展”论文集.上海:上海市学位委员会,上海中医药大学,2011:76-83.
[11]王玉英.黄芩苷的吸收及药动学研究进展[J].中国现代实用医学杂志,2005,4(9):44-45.
[12]王长虹,程雪梅,王峥涛.龙胆泻肝汤中龙胆苦苷和黄芩苷大鼠体内药物代谢动力学研究[C]//2006第六届中国药学会学术年会论文集.2006.
[13]杨明,陈晓燕,张海燕,等.栀子苷4种不同给药途径的药动学研究[J].中国新药杂志,2010,19(9):746-754.
