珍龙醒脑胶囊对小鼠脑缺氧及脑缺血再灌注损伤的保护作用
2012-01-06张会鲜孙建云山东大学药学院药理教研室山东济南250012
高 伟 张会鲜 孙建云 焦 波 (山东大学药学院药理教研室,山东 济南 250012)
脑缺血一定时间恢复血液供应后,其功能不仅不能恢复,却出现更加严重的脑功能障碍,造成脑缺血再灌注损伤(CIR)〔1〕。珍龙醒脑胶囊是治疗脑血管疾病的经典藏药验方,主要由珍珠、天竺黄、西红花、丁香、人工牛黄、麝香、余甘子等中药组成,临床上用于治疗缺血性脑血管疾病〔2〕,但其机制尚未有报道。本研究观察珍龙醒脑胶囊对脑缺氧、脑缺血再灌注后丙二醛(MDA)、超氧化物歧化酶(SOD)、Na+-K+-ATP酶、Ca2+-ATP酶活力的影响,探讨该药抗CIR的机制。
1 材料与方法
1.1 材料
1.1.1 药品 珍龙醒脑胶囊,青海金诃藏药药业股份有限公司,批号20090413。脑心通胶囊,陕西步长制药有限公司,批号110336。均以1%羧甲基纤维素钠(CMC-Na)制成混悬液。SOD、MDA及ATP酶试剂盒均购自南京建成生物工程研究所。
1.1.2 仪器 紫外分光光度计,TU-1810,北京普析通用公司。
1.1.3 动物 昆明种小鼠,18~22 g,雄性Wistar大鼠,250~300 g,雄性;均由山东大学实验动物中心提供,合格证号:SCXK(鲁)20090001。
1.2 方法
1.2.1 珍龙醒脑胶囊对小鼠常压缺氧的影响 将小鼠随机分为空白组(1%CMC-Na)、脑心通组(900 mg/kg)、珍龙醒脑组(100、200、400 mg/kg)。每天给药1次,给药前禁食12 h不禁水,连续7 d。于末次给药后2 h,将小鼠置于含5 g有钠石灰的密封250 ml广口瓶中,以呼吸停止为指标,观察小鼠死亡时间。1.2.2 珍龙醒脑胶囊对小鼠断头缺血缺氧的影响 小鼠分组及给药同1.2.1,于末次给药后2 h,将小鼠断头,以张口为指标,观察断头后喘息时间。
1.2.3 珍龙醒脑胶囊对结扎颈总动脉致小鼠脑缺血缺氧的影响 将小鼠随机分为假手术组(1%CMC-Na)、模型组(1%CMC-Na),脑心通组(900 mg/kg)、珍龙醒脑组(100、200、400 mg/kg)。每天给药1次,给药前禁食12 h不禁水,连续7 d。末次给药后2 h,将小鼠麻醉后,分离双侧颈总动脉,夹闭10 min,再灌注10 min,反复2次。再灌注后缝合皮肤(假手术组分离出颈总动脉,不夹闭血管,然后缝合)。24 h断头取脑,在低温下分取左、右脑。取左脑称重后置80℃烘烤2 h,称干重,计算脑组织含水量。脑组织含水量(%)=(左脑湿重-左脑干重)/左脑湿重×100%。将右脑组织充分匀浆,采用考马斯亮蓝蛋白定量法测定蛋白含量,按照试剂盒要求测定SOD、Na+-K+-ATP酶和Ca2+-ATP酶活力和MDA含量。
1.3 统计学方法 应用SPSS13.0统计软件进行分析,数据结果以x±s表示,采用单因素方差分析,组间比较采用t检验。
2结果
2.1 珍龙醒脑胶囊对小鼠常压缺氧的影响 动物置密封广口瓶中后,呼吸逐渐减弱,直至消失。用药后各组与空白对照组〔(42.1±8.5)min〕比较,动物存活时间有所延长,珍龙醒脑低、中剂量组小鼠存活时间为〔(45.3±9.1)、(49.9±10.6)min〕,其中脑心通〔(56.7±10.5)min〕、珍龙醒脑高剂量组〔(53.0±11.0)min〕,能明显延长小鼠存活时间(P<0.05)。
2.2 珍龙醒脑胶囊对小鼠断头缺血缺氧的影响 动物被断头后,张口呼吸动作仍会持续。用药后,可以明显延长断头后呼吸维持时间。珍龙醒脑高剂量〔(22.1±3.3)s〕和中剂量组〔(22.3±3.3)s〕以及脑心通组〔(23.2 ±3.6)s〕与空白组〔(19.1±2.7)s〕相比,均能明显延长小鼠断头喘息时间(P<0.05);珍龙醒脑低剂量组断头喘息时间〔(20.3±3.5)s〕虽略延长,但无显著差异(P>0.05)。
2.3 珍龙醒脑胶囊对结扎颈总动脉致小鼠脑缺血缺氧的影响
缺血24 h后,与假手术组比较,模型组小鼠脑含水量明显增加,珍龙醒脑有明显的降低脑含水量的作用(P<0.05或P<0.01)。同时,模型组小鼠脑组织中MDA含量明显升高,SOD、Na+-K+-ATP酶、Ca2+-ATP酶活力显著降低(P<0.01),珍龙醒脑可明显降低 MDA含量,并升高 SOD、Na+-K+-ATP酶、Ca2+-ATP酶的活力。见表1,表2。
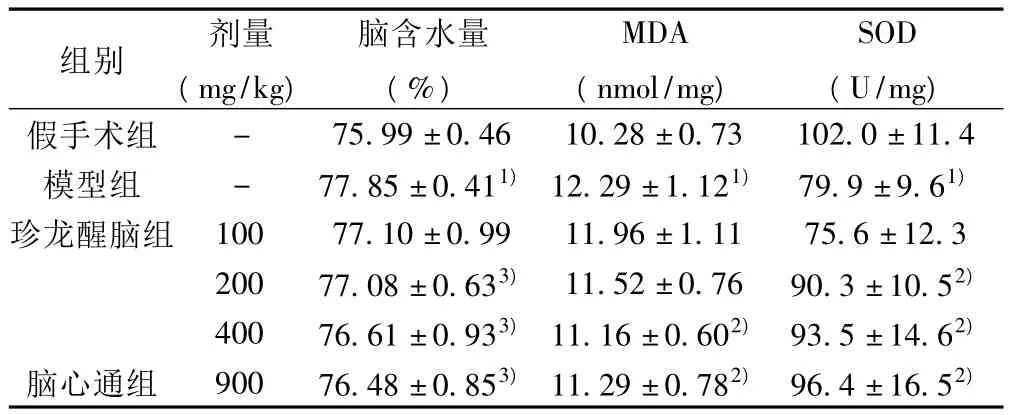
表1 珍龙醒脑胶囊对缺血再灌注小鼠脑组织含水量、MDA和SOD的影响(x ± s,n=9)
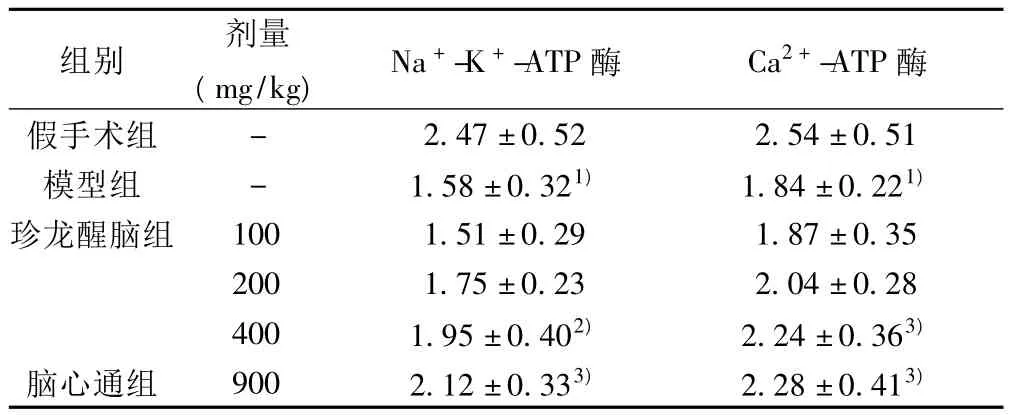
表2 珍龙醒脑胶囊对缺血再灌注小鼠脑组织酶活力的影响(x ±s,n=9,μmol·mg-1·h-1)
3讨论
脑缺血时,组织氧和能量代谢的物质供应不足,ATP生成减少,能量功能障碍,Na+,K+-ATP酶活性降低,使大量 Na+内流、K+外流,使Cl-和水被动进入细胞内,引起神经细胞急性渗透性肿胀死亡。Na+和K+浓度改变,导致细胞膜去极化,进而电压依赖性 Ca2+通道开放,Ca2+大量内流。Ca2+可抑制ATP合成,使能量生成障碍〔1〕,同时细胞内钙超载,细胞内游离Ca2+异常增多,使细胞膜结构受损〔3〕,进一步加重脑损伤。同时由于K+、蛋白激酶C及递质释放等作用,受体依赖性 Ca2+通道开放,Ca2+大量内流,造成细胞内钙超载,进而导致氧自由基产生增加、花生四烯酸代谢增强、兴奋性氨基酸递质(EAA)释放增加等,导致神经元坏死。ATP酶活性下降还可激活Na+泵依赖性EEA载体,使EAA大量释放,开放Ca2+通道,加重脑损伤〔4,5〕。本实验结果发现,珍龙醒脑胶囊可明显提高Na+-K+-ATP酶、Ca2+-ATP酶的活力,有效降低脑含水量。提示珍龙醒脑胶囊可以对抗脑缺氧的能量代谢障碍,并能够降低脑水肿的脑含水量。
脑缺血可以造成氧自由基增加〔6〕。氧化应激损伤是脑缺血再灌注的重要环节之一,氧自由基在CIR中有重要作用。氧自由基可作用于多价不饱和脂肪酸,发生脂质过氧化,诱导DNA、RNA、多糖和氨基酸等大分子物质交联,蛋白质变性、多核苷酸链断裂、碱基重新修饰,造成细胞结构的完整性破坏、膜的通透性、离子转运、膜屏障功能均受到严重影响,从而导致细胞死亡。自由基还能导致 EAA释放增加,促使CIR发生〔1〕。SOD可清除自由基,提高SOD活性可以提高抗氧化作用及组织缺氧能力〔7,8〕。双侧颈总动脉结扎后导致增加脂质过氧化反应,MDA生成增加,SOD活性下降〔9〕。本实验发现珍龙醒脑组可明显降低MAD的量,并且有效提高SOD的活力,提示可对抗CIR的氧自由基损伤。
珍龙醒脑胶囊为传统藏药,主要由珍珠、天竺黄、西红花、丁香、人工牛黄、麝香、余甘子等中药组成,具有活血化瘀、安神护脑、祛风化痰、养阴活血、化痰通络等功效,用于痰瘀阻络所致的中风,语言蹇涩,半身不遂,口眼歪斜。现代药理研究表明,珍珠富含多种氨基酸,还含有微量元素、小分子活性肽、卟啉及金属卟啉等,可以减轻自由基损伤;西红花的化学成分主要是胡萝卜素及其多糖苷类,可以增强记忆、降血压、抗血栓;诃子含三萜类、酚酸类、脂肪族化合物,具有强心、抗氧化和抗动脉粥样硬化等作用;麝香含多种氨基酸和微量元素,麝香酮具有兴奋动物呼吸的作用,可以使动物呼吸频率和深度增加;人工牛黄含牛磺酸、牛胆粉、去氧胆酸、胆红素、微量元素,拮抗血小板聚集与血栓形成。该药可以溶解血栓,消除动脉粥样硬化斑块,解除血管平滑肌痉挛,扩张血管,改善微循环,增加血流速度,降低血液黏度,扩张微小动静脉,降低脑血管通透性。最终减少自由基损伤、提高脑灌注、保护脑细胞、提高脑功能、改善脑梗死的预后〔2〕。
综上所述,本实验初步证明珍龙醒脑胶囊通过降低MDA含量,升高SOD、Na+-K+-ATP酶、Ca2+-ATP酶活力,有效降低脑含水量,对小鼠脑缺氧及CIR具有保护作用,其抗CIR作用与保护脑组织ATP酶活性、抑制脂质过氧化反应和减轻自由基损伤有关。
1 刘启锋,刘 明,刘玉河,等.脑缺血再灌注损伤机制研究进展〔J〕.中华神经外科疾病研究杂志,2006;5(6):566-8.
2 杨延林,张义智.珍龙醒脑胶囊治疗脑梗死临床观察〔J〕.中国当代医药,2010;17(17):95-6.
3 lexandratou E,Yova D,Loukas S.A confocal microscopy study of the very early cellular response to oxidative stress induced by zinc phthalocyanine sensitization〔J〕.Free Radic Biol Med,2005;39(9):1119-27.
4 鲁 宏,孙善全.脑水肿机制的研究进展〔J〕.重庆医科大学学报,2002;27(4):494-6.
5 王晓良.应用分子药理学〔M〕.北京:中国协和医科大学出版社,2005:215.
6 Chan PH.Role of oxidants in ischemic brain damage〔J〕.Stroke,1996;27(6):1124-9.
7 朱 怡,陈 霞,黄 屏,等.丹参川芎嗪对大鼠脑缺血再灌注损伤的保护作用〔J〕.现代中西医结合杂志,2011;20(7):802-4.
8 Sasaki T,Shimizu T,Koyama T,et al.Superoxide dismutase deficiency enhances superoxide levels in brain tissues during oxygenation and hypoxia-reoxygenation〔J〕.J Neurosci Res,2011;89(4):601-10.
9 Nade VS,Kawale LA,Dwivedi S,et al.Neuroprotective effect of Hibiscus rosa sinensis in an oxidative stress model of cerebral post-ischemic reperfusion injury in rats〔J〕.Pharm Biol,2010;48(7):822-7.
