聚丙烯纤维滤材气溶胶样品的浸取-灰化-消解前处理方法
2012-01-04唐寒冰刘龙波刘蜀疆周国庆李冬梅张利兴
唐寒冰,刘龙波,刘蜀疆,周国庆,李冬梅,张利兴
西北核技术研究所,陕西 西安 710024
放射性核素核查是《全面禁止核试验条约》(Comprehensive Nuclear-Test-Ban Treaty,CTBT)所规定的4种监测技术之一,可以为核事件的性质提供无可争辩的证据。在国际监测系统(international monitoring system,IMS)台站中,一般采用过滤法进行大流量气溶胶采样、滤材压片后使用γ谱仪测量相关放射性核素的方法[1]。当用γ无损分析技术无法得到可疑样品的足够信息时,《全面禁止核试验条约》组织(Comprehensive Nuclear-Test- Ban Treaty organization,CTBTO)的临时技术秘书处(provisional technical secretariat,PTS)可能指定条约规定的某些实验室对样品进行前处理后进行适当的放射化学分析[2]。
这种气溶胶滤材样品与一般气溶胶样品的主要差异在于:(1)样品量大;根据经验,分样后滤材基体约5 g,颗粒物质量约1.5 g,而一般的气溶胶样品中,基体通常很少,颗粒物质量也小于0.5 g;(2)相关核素多;用于事件性质判断的重要相关核素有:95Zr、134Cs、136Cs、140Ba、140La、141Ce、143Ce和147Nd等[3],这些核素(元素)的化学性质差异很大。因此,单独使用某一种样品前处理方法,如灰化法、湿消解法和熔融法等[4]均难以达到目的。
李冬梅等[5]的研究表明,微波密闭浸取或微波密闭消解方法对此类样品中的易挥发及难溶核素均可以高效率回收,但单次样品处理量较小。在此基础上,本工作考虑联合使用多种前处理方法。考虑到Cs等易挥发性核素的溶解性较好,拟先用微波密闭浸取法将易挥发性核素浸出;然后将浸取残渣灰化除去滤材基体,最后用微波密闭消解的方法将难溶核素彻底溶解。这样可以在保证相关核素回收率的前提下,有效除去滤材基体。此种方法目前尚未见国内外文献报道。本工作中用Cs代表易挥发核素,Ce代表稀土核素,Zr代表难溶核素,均使用稳定同位素代替相应的放射性核素,滤材使用常用的聚丙烯纤维滤材。
1 实验部分
1.1 样品制备和实验仪器
聚丙烯纤维滤材,邢台华邦非织造有限公司;Cs、Ce、Zr标液,国家标准物质研究中心;HCl(w=36%~38%)、HNO3(w=65%~68%),天津科密欧化学试剂开发中心;HF(w=40%),天津富宇精细化工有限公司;w=2%HCl,由w=36%~38%HCl配制。
由于目前尚无标准样品或参考样品,本实验自行制备了两类样品,分别称为A类和B类。A类样品的制备方法为:取聚丙烯纤维滤材5 g,定量滴加Cs、Ce和Zr标液,只用于滤材浸取条件的选择。B类样品为取样(大气气溶胶)后的聚丙烯纤维滤材,定量滴加Cs、Ce和Zr标液,用于研究全流程实验条件。
XT-9900型微波消解仪,海新拓微波溶样测试技术有限公司;ICP-MS,德国Finnigan Mat Element公司;SX2-25-10型马弗炉,上海实验电炉厂。
1.2 实验流程
在微波密闭浸取中,为了避免与滤材基体反应,本实验选用了无氧化性的w=2%HCl溶液为浸取剂。聚丙烯纤维滤材与水溶液之间浸润性差,且比重小,因此滤材会浮于浸取剂上层或表面,严重影响浸取的效率。本实验中制作了在溶样杯中使用的聚四氟乙烯(PTFE)压杆,将压杆置于滤材与溶样杯密封碗之间,压杆底部为一打有均匀小孔的圆盘,既便于液体的流动,又可保证滤材全部浸于溶液中。处理前将滤材切成小块,使用微波消解仪进行浸取,分别对浸取压力、功率、时间进行了考察[5-6]。
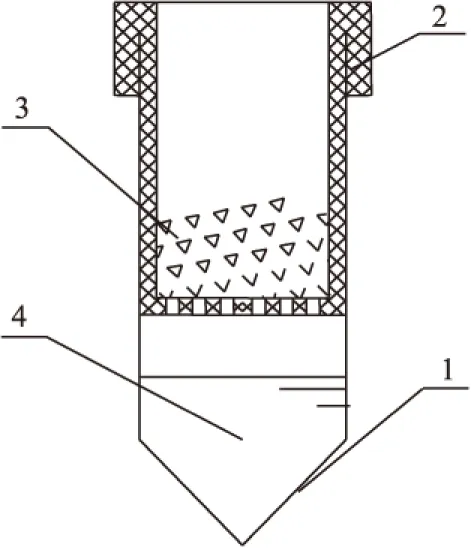
图1 离心装置示意图
浸取后的滤材碎块体积大、松散且比重小,无法用普通的离心管过滤或抽滤。本实验自制了套于离心管内的过滤装置(图1)。将一底部有小孔的PTFE内管(图1中2所示)套于离心管内,将浸取后溶液连同滤材碎块转移至内管中,离心分离即可将滤材小块和浸取液分离。浸取液经过滤后用ICP-MS测量,得到浸取回收率。
在灰化中,将滤材小块装入坩埚,电炉加热至冒烟完毕,转移至马弗炉中灰化。灰化前后对坩埚进行称重。由于滤材样品质量不一,因此使用灰化剩余率(灰质量除以滤材质量)来表征灰化对滤材基体的去除效果。根据聚丙烯纤维滤材热失重曲线,失重温度为310~450 ℃,因此选择灰化温度350、400、450 ℃,灰化时间分别为1.0、1.5、2.0 h,考察灰化效果。
灰化残渣用微波密闭消解。建立了不同的消解流程,消解后将溶液蒸至约1 mL,用w=2%HCl溶出并稀释定容,过滤后用ICP-MS测量。
2 结果与讨论
2.1 浸取条件
用A类样品来做滤材浸取条件实验。微波密闭浸取的压力范围为0.1~4 MPa(表压),微波满功率为800 W。w=2%HCl溶液在此压力范围内的温度与水接近,即120~250 ℃[7],由于聚丙烯的熔点为170~175 ℃[8],因此浸取压力(表压)不大于0.7 MPa(170 ℃)。选择不同压力、功率及时间进行了初步实验,结果列于表1。由表1可看出,为确保滤材物理性质不变,最终选定浸取压力0.1 MPa,功率为70%满功率。考察不同浸取时间对回收率的影响,结果列于表2。由表2可看出,5 min与10 min的浸取回收率明显优于15 min与20 min。结合表1分析原因可能为浸取时间的延长导致部分滤材物理性质发生了变化,内部可能有结块或变硬的现象。因本实验中样品量较大,为保证浸取效果,选定浸取时间为10 min。用较符合实际样品情况的B类样品进行了验证。结果表明,B类样品中Cs和Ce均可定量回收,且回收率明显高于A类样品。分析原因为,B类样品中含有大量颗粒物,其表面的浸润性较好,与浸取液接触充分,浸取效果好。
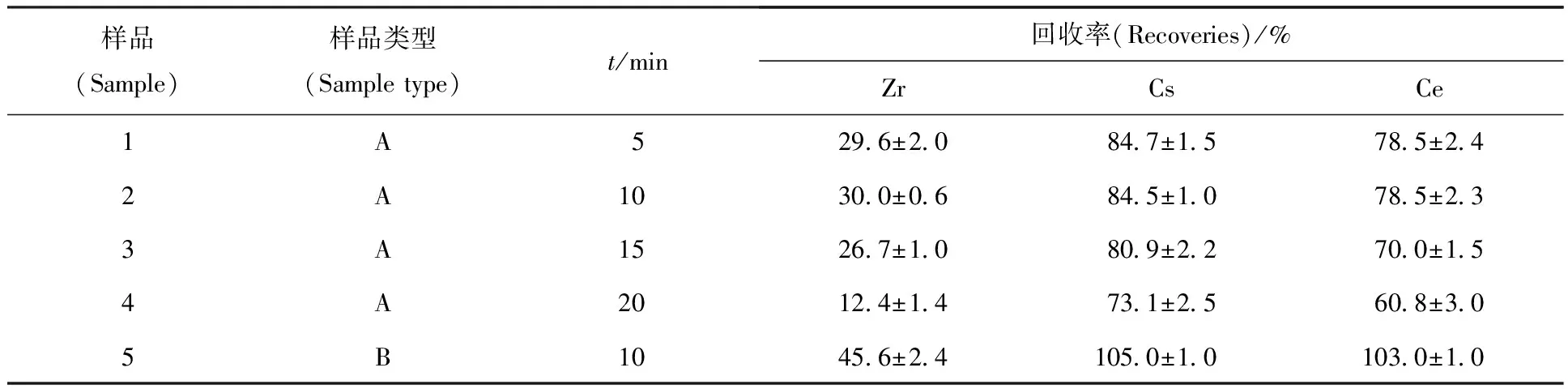
表2 不同浸取时间的回收率
注(Note):A,n=3;B,n=5
2.2 灰化条件
实验考察了灰化温度和时间对滤材基体去除效率的影响,图2为不同灰化温度和时间下的聚丙烯纤维滤材的灰化剩余率R,纵坐标为对数坐标,图中数据为两次实验的平均值。
由图2可知,350 ℃时,滤材剩余率均大于10%,在400 ℃和450 ℃时均低于1%,450 ℃时剩余率最低。从样品灰化后的剩余量来看,450 ℃ 2 h灰化后,残灰质量在0.3 mg以下,表明灰化基本完全。从减小样品量的角度来看,450 ℃ 2 h效果最好。
2.3 消解条件
根据气溶胶成分和被分析对象,分别选取2个体系进行消解[9-11]:HCl+HNO3+HF和HNO3+HF,设定消解程序为:压力1.5 MPa保持时间20 min,再升压力至2.0 MPa,保持时间5 min。消解结束后,观察到HNO3+HF体系的消解效果好。选定消解溶剂后,又对HNO3、HF用量及配比进行了考察,结果列于表3。
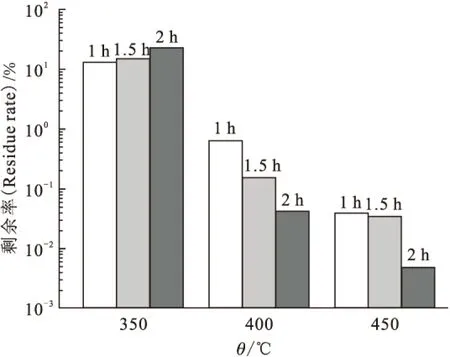
图2 聚丙烯纤维滤材在不同条件下的灰化剩余率

表3 消解体系及用量
注(Note):w(HCl)=36%~38%,w(HNO3)=65%~68%,w(HF)=40%
根据以上实验结果最终确定B类样品消解条件为:压力1.5 MPa,保持时间20 min,再升压力至2.0 MPa,保持时间5 min;消解液:HNO3(7 mLw=65%~68%)+HF(2 mLw=40%)。
2.4 流程总回收率
用以上建立的实验流程对B类样品进行前处理实验,流程中各步骤及总回收率列于表4。由表4可看出,B类样品中的Cs、Ce浸取完全,剩余的Zr经过微波消解可以完全回收。这一结果验证了最初的设想,即易挥发性和易溶元素可以用微波密闭浸取的方法回收,难溶元素灰化损失小,且可以用微波密闭消解的方法回收,中间采用灰化除去滤材基体则弥补了微波密闭消解法处理样品量小的缺点,达到了目的。下一步将考虑扩大核素的范围,验证该流程的通用性。
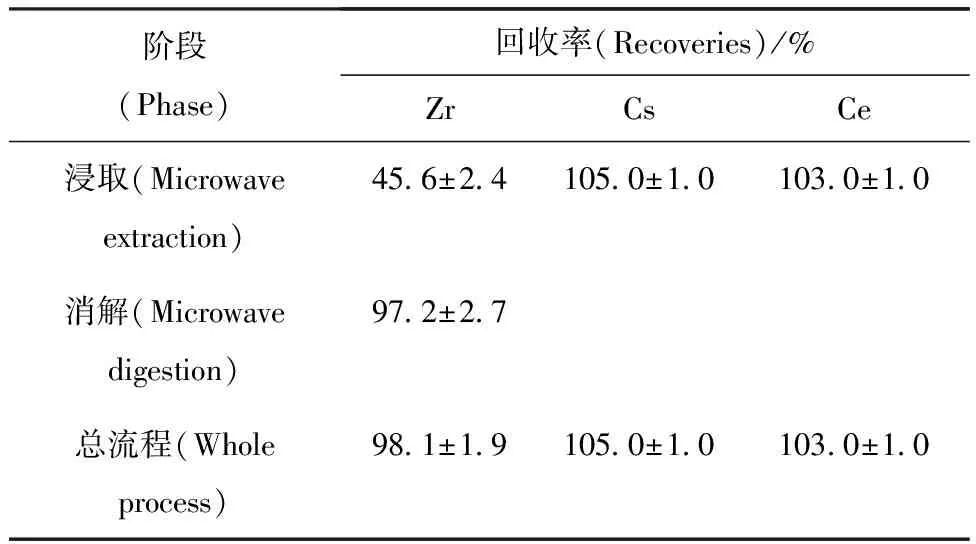
表4 流程回收率
注(Note):n=5
3 结 论
(1)本工作确定了滤材基体为5 g、颗粒物含量约为1.5 g的气溶胶样品的最佳前处理流程:首先将滤材进行微波密闭浸取,浸取条件为压力0.1 MPa,功率70%,时间10 min,浸取剂为2%HCl;浸取残渣进行灰化处理,温度450 ℃,时间2 h;灰化后的残渣进行微波密闭消解,消解程序为压力1.5 MPa,保持时间20 min,再升压力至2.0 MPa,保持时间5 min,消解液:HNO3(7 mLw=65%~68%)+HF(2 mLw=40%);最终将消解液蒸发至约1 mL,用2%HCl溶出。
(2)实验结果表明,对于气溶胶滤材样品,易挥发性和易溶元素可以用微波密闭浸取的方法回收,难溶元素灰化损失小,可用微波密闭消解的方法回收,中间采用灰化除去滤材基体弥补了微波密闭消解法处理样品量小的缺点。此方法解决了气溶胶样品基体质量大、待测元素多且化学性质差异大、单用某一种前处理方法难以保证回收率的问题。本工作提出的流程对于外加标液的模拟样品中的Cs、Ce和Zr可定量回收。
[1]Padoani F,Karhu P,Medici F,et al.Setting up and Implementation of a Global Atmospheric Radioactivity Monitoring Network for CTBT Verification Purposes[J].J Radioanal Nucl Chem,2005,263(1): 183-188.
[2]Werzi R.The Operational Status of the IMS Radionuclide Particulate Network[J].J Radioanal Nucl Chem,2009,282: 749-754.
[3]张利兴,王旭辉.禁核试核查技术导论[M].北京:国防工业出版社,2005.
[4]Mester Z,Angelone M,Brunori C,et al.Digestion Methods for Analysis of Fly Ash Samples by Atomic Absorption Spectrometry[J].Analytica Chimica Acta,1999(395): 157-163.
[5]Li D M,Zhang L X,Wang X H,et al.Ashing and Microwave Digestion of Aerosol Samples With a Polypropylene Fibrous Filter Matrix[J].Analytica Chimica Acta,2003,482(1): 129-135.
[6]Wang Chu-Fang,Yang Jenq-Yann,Ke Cheng-Hsiung.Multi-Element Analysis of Airborne Particulate Matter by Various Spectrometric Methods After Microwave Digestion[J].Analytica Chimica Acta,1996 (320): 207-216.
[7]陈敏恒,丛德滋,方图南,等.化工原理[M].北京:化学工业出版社,2009.
[8]何曼君,陈维孝,董西侠.高分子物理[M].上海:复旦大学出版社,1990.
[9]袁东,但德忠,罗方若.微波消解在环境分析中的应用及进展[J].现代科学仪器,2000,3:42-44.
[10]Ivanov A J,Djingov A R,Ammer S K,et al.On the Microwave Digestion of Soils and Sediments for Determination of Lanthanides and Some Toxic and Essential Elements by Inductively Coupled Plasma Source Mass Spectrometry[J].Talanta,2001(54): 567-574.
[11]邹明强,王大宇,贾睿,等.家用微波炉消解土壤样品[J].吉林大学自然科学学报,1995,3:73-76.
