6,6′-二(5,6-二乙基-1,2,4-三嗪-3-基)-2,2′-联吡啶萃取分离镅与镧系元素
2012-01-04叶国安唐洪彬
洪 哲,叶国安,唐洪彬,何 辉
1.中国原子能科学研究院 放射化学研究所,北京 102413;2.环境保护部 核与辐射安全中心,北京 100082
乏燃料经过后处理,大部分铀、钚(一般水法流程对铀的回收率可达99.8%以上,对钚的回收率可达99.5%以上[1])被回收,同时,大部分的裂变产物(FP)与次锕系元素(Am、Cm)进入高放废液(HLLW)。HLLW的安全处理与处置成为公众高度关注的问题,也成为制约核能发展的关键因素。分离-嬗变的路线成为解决这一问题的较好途径。
目前,对HLLW组分离研究较多的有以下几个流程:国外有美国的TRUEX流程[2]、日本的DIDPA流程[3]、法国的DIAMEX流程[4]、瑞典的CTH流程[5-6],国内的有TRPO流程[7]、酰胺荚醚流程[8-10],都取得了不错的分离效果。在这些流程中均可实现次锕系元素与裂片元素的分离,且将三价锕系与镧系元素分在一组。但由于Am、Cm与镧系元素化学性质非常相似,分离困难[11-12],因此它们一起作为α废物排出。为进一步减少α废物体积以及今后嬗变的需要,需将Am、Cm与镧系元素分离[13]。
含N类软配体萃取剂对三价锕系的亲和力大于对镧系元素的亲和力,其中,6,6′-二(5,6-二烷基-1,2,4-三嗪-3-基)-2,2′-联吡啶(R-BTBP)对三价锕系元素的萃取分配比较高[14],而且可以在1 mol/L HNO3体系中应用,便于和组分离流程的衔接。萃取剂中R基越长,其在有机溶剂中的溶解性能越好,但其对Am的萃取分配比却无直接关系,6,6′-二(5,6-二乙基-1,2,4-三嗪-3-基)-2,2′-联吡啶(C2-BTBP)对Am/Ln的分离性能好且研究较少。因此,本工作拟以C2-BTBP为萃取剂,对C2-BTBP分离镅与镧系元素的行为进行研究。
1 实验部分
1.1 仪器与试剂
GL-88B漩涡混合器,海门市其林贝尔仪器制造有限公司;800型离心机,上海手术器械厂;LS-6000LL型低本底α-β液体闪烁谱仪,美国Beckman公司;ICP-AES分析仪,美国Thermo公司。
C2-BTBP,本实验室合成,经MS、IR、1H NMR鉴定,其结构示于图1;氯仿(CHCl3),分析纯,北京益利精细化学品有限公司;241Am,中国原子能科学研究院产品;其它试剂均为分析纯。

图1 C2-BTBP的结构图
1.2 实验方法
稀土料液的配置:称取一定量的金属硝酸盐溶于1 mol/L硝酸中,其浓度列于表1。
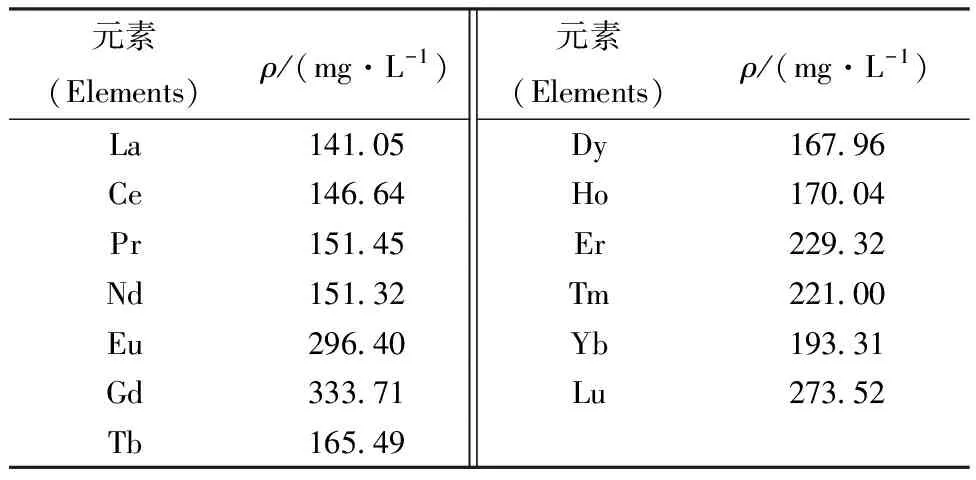
表1 混合稀土料液中各元素的质量浓度
萃取平衡时间测定:在室温下,将水相料液与C2-BTBP/CHCl3按一定体积比加入到塑料离心管中,测量振荡不同时间后水相和有机相中241Am的放射性活度,当其不随时间而改变时,则认为萃取达到平衡。
萃取实验:将等体积的有机相和含放射性的水相混合接触,振荡时间t(t为萃取达平衡的时间,min),离心分相,取样测量有机相和水相中的放射性计数。
1.3 分析方法
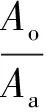


2 结果与讨论
2.1 稀释剂的选择
C2-BTBP为黄色固体粉末,萃取前须找到合适的溶剂将其溶解。因此考察了C2-BTBP在烷烃、氯代烷烃、酯、醇类中的溶解情况。
研究发现,C2-BTBP在正十二烷中基本不溶,液相为无色透明溶液;在正辛醇、乙酸乙酯中溶解度很小,不利于进行萃取行为研究;在二氯甲烷、三氯甲烷、1,1,2,2-四氯乙烷中溶解度良好。
在液体氯代烃中,1,1,2,2-四氯乙烷的毒性最大,对身体危害最大,故不用它作为稀释剂。二氯甲烷的饱和蒸汽压远大于三氯甲烷的饱和蒸汽压,表明二氯甲烷相对三氯甲烷更易挥发,不便于生产使用。因此,综合考虑溶解性能、毒性和溶剂的挥发性,选择三氯甲烷作为研究C2-BTBP基本性能的稀释剂,以了解此萃取剂的性能。
2.2 C2-BTBP对镅的萃取研究
2.2.1振荡时间对两相活度比的影响 图2给出了在一定振荡强度下C2-BTBP萃取Am时振荡时间对两相活度比的影响。从图2可以看出,Am的分配比在10 min左右基本达到萃取平衡。所以后续实验选择两相混合时间为10 min。
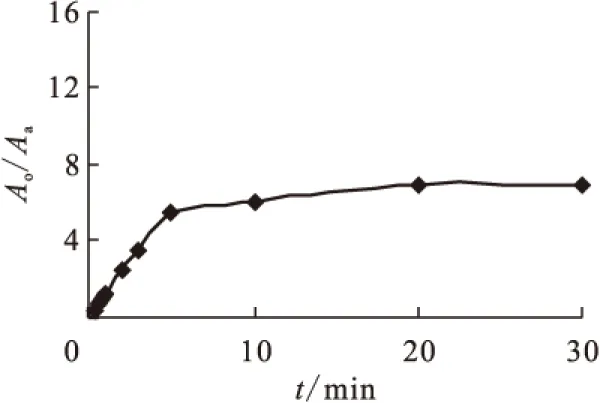
图2 C2-BTBP萃取Am时两相活度比随时间的变化
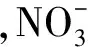

图3 初始水相酸度对D(Am)的影响
2.2.3萃取剂浓度对D(Am)的影响 根据文献[15]对C2-BTBP萃取行为的研究,C2-BTBP对Am(Ⅲ)的萃取反应方程式可表示为:

(1)
(1)式中,S代表萃取剂。萃取平衡常数为:
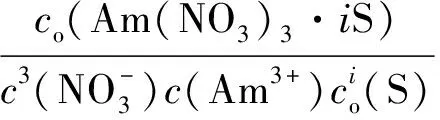
(2)
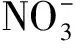
(3)
根据分配比定义:
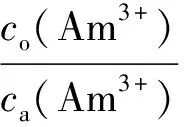
(4)
将(2)式代入(4)式得Am3+的分配比为:

(5)
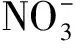
lgD(Am3+)=ilgco(S)+
(6)
由于在一定温度和离子强度下,Kex恒定,固定其他条件不变,改变萃取剂浓度,可以得到:
lgD(Am3+)=ilgco(S)+C
(7)
式中,C为常数。可通过图解法求i值。由(7)式知,固定其他条件,测量不同萃取剂浓度对萃取分配比的影响,以lgD(Am3+)对lgco(S)作图,则直线斜率为i。其lgD(Am3+)-lgco(C2-BTBP)关系示于图4。从图4可以看出,当萃取剂的浓度比较低时,lgco(C2-BTBP)的值低于-1.46(萃取剂浓度低于0.035 mol/L)时,直线的斜率是1.6,根据斜率分析法,可以判断萃和物中有Am(NO3)3·C2-BTBP和Am(NO3)3·2(C2-BTBP)两种结构,两种结构的比例大致为1∶1,反应如式(8)和(9)所示。当萃取剂的浓度增大时,lgco(C2-BTBP)的值大于-1.40(萃取剂浓度高于0.04 mol/L)时,直线的斜率是2.0,根据斜率分析法,可判定萃合物结构为Am(NO3)3·2(C2-BTBP),反应式如式(9)所示。
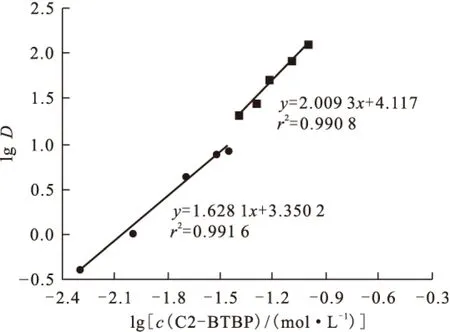
图4 萃取剂浓度对Am分配比的影响
Am(NO3)3·C2-BTBPo
(8)
Am(NO3)3·2(C2-BTBP)o
(9)
2.2.4相比对萃取率(E)的影响 在固定水相酸度、萃取剂浓度等条件下研究了不同相比时C2-BTBP对Am的萃取率的影响,其结果列于表2。从表2可以看出,相比对萃取率的影响较大,故可通过增大相比来提高Am的萃取率,但增大相比同时也会增加有机废物量。因此,单级萃取实验选用1∶1的相比,在流程设计中采用1∶2的相比,可以减少萃取剂用量,同时也减少有机废物量。
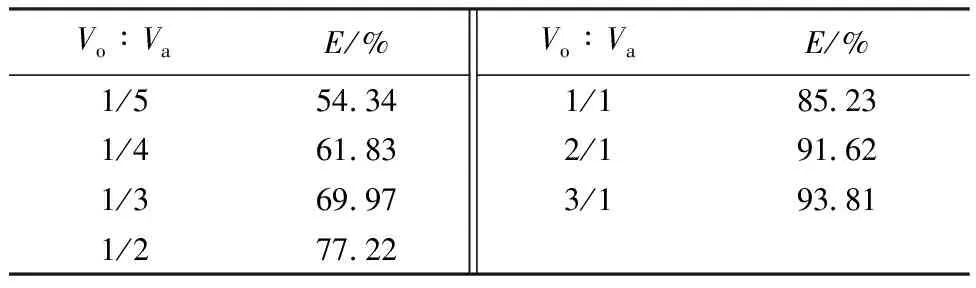
表2 相比对萃取率的影响
注(Notes):c0(HNO3)=1 mol/L,c(C2-BTBP/CHCl3)=0.035 mol/L,θ=12 ℃,t=10 min
2.3 C2-BTBP对镧系元素的萃取行为研究
2.3.1两相接触时间对13种镧系元素萃取行为的影响 图5为C2-BTBP对13种镧系元素萃取时时间对两相分配比的影响。由图5可以看出,La、Ce两种元素在萃取30 min内有机相中的浓度低于仪器的检测下限,表明La、Ce的萃取率非常低;Pr、Nd、Eu、Gd几种元素在萃取5 min内达到平衡(Nd、Eu、Gd在2 min内萃取达到平衡),萃取动力学较快;Tb、Dy几种元素在萃取10 min时达到平衡;而Ho、Er、Tm、Yb、Lu在萃取30 min时仍未达到平衡。综上,随着原子序数的增加,萃取达到平衡所需的时间增加。由于Am在10 min时萃取达到平衡,本工作目的是进行锕系与镧系元素的分离,镧系的分配比越低越好,因此,可利用二者的萃取动力学差异,最终选择萃取时间为10 min。
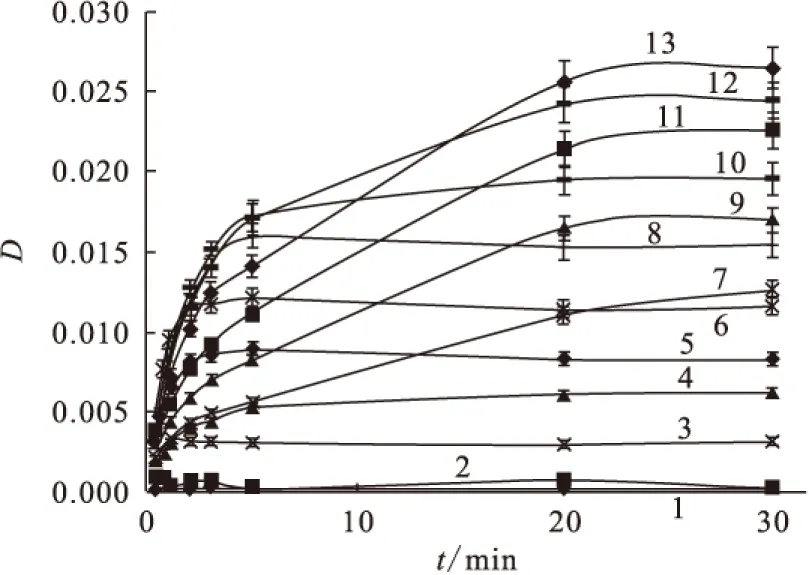
图5 两相接触时间对萃取镧系元素的影响
2.3.2酸度对分配比的影响 图6为C2-BTBP对13种镧系元素萃取时酸度对两相分配比的影响。由图6可知,在0.05~4 mol/L酸度范围内,La基本不被萃取,其余12种镧系元素的萃取分配比先增高后降低,均在3 mol/L酸度时达到最大值。原因同2.2.2节。
2.4 串级实验
2.4.1概念流程的设计 根据C2-BTBP对Am和镧系元素萃取行为的基础数据,拟定了串级实验工艺流程,萃取剂浓度为0.04 mol/L C2-BTBP/CHCl3,水相进料酸度为1.0 mol/L HNO3,组成见表1。1.0 mol/L HNO3作洗涤液,0.01 mol/L HNO3作反萃剂,概念流程示于图7。该流程由6级萃取、4级洗涤、4级反萃组成。流比:AF∶AX∶AS=1∶1∶0.5,BF∶BX=1∶1,实验温度为15 ℃。
2.4.2两相出口浓度变化 按照6级萃取、4级洗涤进行串级实验,做到40排,Am的有机相从第27排开始取瞬时样,水相从第28排开始取瞬时样。Ln的有机相从第31排开始取瞬时样,水相从第30排开始取瞬时样,结果示于图8。从图8可以看出,串级实验进行到30排时,两相出口处的计数(浓度)趋于定值,萃取已经达到了平衡。因此,在30排以后取各级样均达到平衡。

图6 酸度对萃取镧系元素的影响
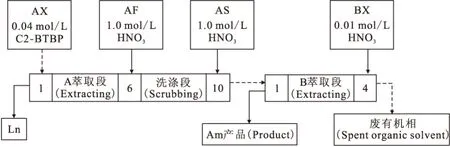
图7 C2-BTBP分离镅和镧系元素的概念流程图
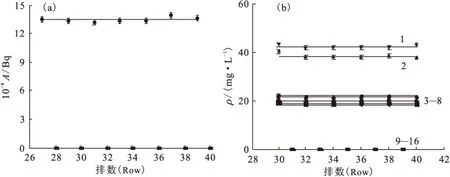
图8 Am(a)和镧系元素(b)各排瞬时样
2.4.3Am和La在萃取洗涤段的各级分布 串级实验在进行到第35排时取平衡样,级数为偶数级。然后再进行5排实验,在第40排时取奇数级的平衡样。图9是Am和La在萃取洗涤段的各级分布。从图9(a)可以看出,基本上所有的Am都萃取到了有机相中,而且经过两级萃取后,即从第四级开始,料液中的Am基本已全部萃入到有机相中,说明C2-BTBP对Am的萃取分配比很高。从图9(b)可以看出,萃取剂对La基本不萃取,所有的La全部留在了水相。因此,通过设计的流程,用C2-BTBP/CHCl3,可很好的实现Am/La的分离。串级实验中Am和Ln的萃取率和物料衡算等数据列于表3。从表3可知,在整个萃取洗涤段,Am的萃取率为99.93%,Ln的萃取率小于0.03%,去污因子(DF)大于103。因此,可通过6级萃取、4级洗涤实现Am/Ln的分离。

图9 Am(a)和La(b)在萃取洗涤段的各级分布
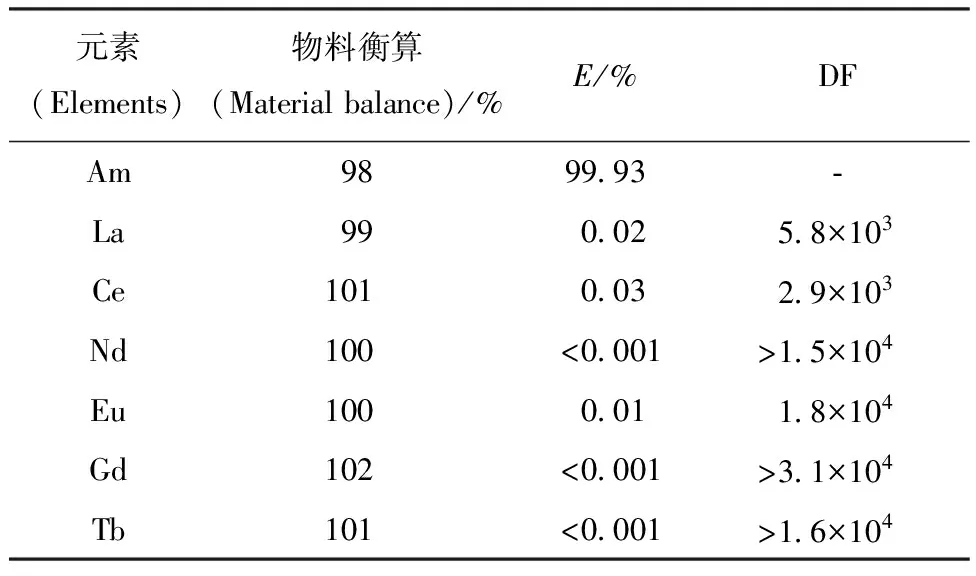
表3 串级实验Am、Ln的萃取率及物料衡算
2.4.4与DiBTP[16]分离三价锕系与镧系元素的性能比较 为比较C2-BTBP与DiBTP[16]分离三价锕系与镧系元素的性能,现将二者的串级实验参数和结果列于表4。从表4可知:C2-BTBP与DiBTP各有优缺点,C2-BTBP的优点是进料酸度高(1.0 mol/L HNO3),工业上易于控制,Am和Ln的净化效果好,单级反萃容易,不需要加入络合剂,缺点是稀释剂的选择有待进一步的研究;DiBTP的优点是用正辛醇和十二烷做为稀释剂,缺点是进料酸度低(0.2 mol/L HNO3),Am中Ln(Eu)的净化效果差,单级反萃实验时发现需要加入络合剂来反萃Am。

表4 C2-BTBP与DiBTP的串级实验参数和结果比较
3 结 论
通过C2-BTBP对镅和镧系元素的萃取行为研究,得出了以下几点结论。
(1)C2-BTBP萃取Am时,10 min达到平衡;D(Am)随酸度增加先增大后减小,因此,可在0.5~2 mol/L硝酸范围内进行萃取实验,在考察的酸度范围内,镧系元素的分配比较小。表明C2-BTBP是一种很好的分离Am和镧系元素的萃取剂,也证实了含软配位原子的萃取剂对三价锕系元素有更高的选择性。
(2)提出了C2-BTBP/CHCl3体系分离三价锕系与镧系元素的概念流程,并经串级实验验证。萃取剂(C2-BTBP/CHCl3)浓度为0.04 mol/L,料液酸度为1.0 mol/L HNO3,洗涤液酸度为1.0 mol/L HNO3,流比为AF∶AX∶AS=1∶1∶0.5,经6级萃取、4级洗涤后,镅的萃取率为99.93%,去污因子大于103,Am中镧系元素的含量小于0.03%,可较好的实现镅和镧系元素的分离。
(3)C2-BTBP可以在c0(HNO3)=1 mol/L时,较好地实现镅和镧系元素的分离;BTBP类作为萃取剂的难点之一是其稀释剂选择问题,本工作以三氯甲烷作为稀释剂在核工业中的进行应用存在一定问题,因此可作为研究C2-BTBP基本性能的稀释剂,以了解此萃取剂的性能,关于稀释剂的选择仍需进一步的研究。
[1]吴华武.核燃料化学工艺学[M].北京:原子能出版社,1989:167-168.
[2]Cecille L,Casarci M,Pietrelli L,et al.New Separation Chemistry Techniques for Radioactive Waste and Other Specific Application[M].London U K: Elsevier,1991: 21.
[3]Kubota M,Yamayucki I,Shirahasi K,et al.Development of a Partitioning Process for the Management of High Level Waste[C]∥Global’93 Proceedings of the International Conference and Technology Exposition on Future Nuclear System: Emerging Fuel Cycles and Waste Disposal Option.Washington: American Nuclear Society,La Grange Park,Ⅲ,1993: 588.
[4]Cuillerdier C,Musikas C,Hoel P,et al.Malonamides as New Extractants for Nuclear Waste Solutions[J].Sep Sci Technol,1991,26: 1 229.
[5]Liljenzin J O,Persson C,Svantesson I,et al.The CTH-Process for HLLW Treatment (Part I General Description and Process Design)[J].Radiochimical Acta,1984,35: 155.
[6]Persson G,Wingertors S,Liljenzin J O,et al.The CTH-Process for HLLW Treatment (Part Ⅱ.Hot Test)[J].Radiochimical Acta,1984,35: 163.
[7]Zhu Y J,Song C L.Recovery of Neptunium,Plutonium and Americium From Highly Active Waste,Trialkyl Phosphine Oxide Extract Ion[M]∥Morss L R,Fuger J,eds.Transuranium Element Symposium.1990.Washington DC: American Chemical Society,1992: 318.
[8]叶国安,何建玉,姜永青,等.酰胺荚醚对Am(Ⅲ)和Eu(Ⅲ)的萃取行为研究Ⅰ.萃取机理研究[J].核化学与放射化学,2000,22(2):65-72.
[9]叶国安,何建玉,罗方祥.酰胺荚醚对Am(Ⅲ)和Eu(Ⅲ)的萃取行为研究Ⅱ.萃取热力学和萃合物光谱研究[J].核化学与放射化学,2000,22(3):136-143.
[10]叶国安,罗方祥,何建玉,等.酰胺荚醚萃取剂从模拟高放废液中分离锕系和镧系元素的研究[J].原子能科学技术,2001,35(增刊):62-69.
[11]王萍.镅等锕系元素与镧系元素分离方法研究进展[J].环境科学导刊,2008,27(5):16-20.
[12]李寿枬.高放废物的嬗变处置与不产生长寿命高放废物的先进核能系统[J].核科学与工程,1996,16(3):269-283.
[13]梁俊福,李旗.二( 2,4,4三甲基戊基)-二硫代膦酸萃取分离Am和Cm的研究[J].核化学与放射化学,2005,27(4):221-224.
[14]Drew M G B,Foreman M R S J,Clement Hill,et al.6,6′-Bis-(5,6-Diethyl-[1,2,4]Triazin-3-yl)-2,2′-Bipyridyl the First Example of a New Class of Quadridentate Heterocyclic Extraction Reagents for the Separation of Americium(Ⅲ)and Europium(Ⅲ)[J].Inorganic Chemistry Communications,2005,8: 239-241.
[15]Retegan T,Ekberg C,Dubois I,et al.Extraction of Actinides With Different 6,6′-Bis(5,6-Dialkyl-[1,2,4]-Triazin-3-yl)-[2,2′]-Bipyridines (BTBPs)[J].Solvent Extr Ion Exch,2007,25: 417-431.
[16]程琦福.双三嗪吡啶的合成及其分离镅和镧系元素的研究[D].北京:中国原子能科学研究院,2006.
