蒿甲醚的纳米包装
2012-01-03洪宗国吴林玉
洪宗国,王 东,吴林玉
(中南民族大学 药学院,武汉 430074)
蒿甲醚是青蒿素的衍生物,为新一代抗疟药,具有比青蒿素更强的抗疟活性[1,2],用于各种疟疾以及抗氯喹恶性疟及脑型疟的急救和治疗,也用于血吸虫病的治疗和高热病人的退热.目前,市场上有片剂[3]、注射剂[4]和胶囊[5]等常规剂型.但蒿甲醚存在着难溶于水的缺点,其口服生物利用度较低,代谢快,体内维持时间短[6], 需开发新剂型以弥补上述不足.
纳米胶囊作为一种特殊的药物载体可解决此类问题.这种载药粒子粒径一般为1~1000 nm,其突出优点为具有可控、缓释和靶向性,以及高的细胞摄取、减少药物副作用等,成为前景广泛的给药系统[7-11].目前,制备纳米胶囊的方法较多,如nanoprecipitation[12,13], layer-by-layer[14], and emulsion-coacervation[15-17]等.然而,这些方法均因涉及多步处理而必定存在二次污染问题[18]. 本文则使用操作简便、处理过程仅一步且可避免二次污染[19]的初生态微晶法[18]完成蒿甲醚的纳米包装;而实验中采用生物相容性好,毒性低,在体内可降解[20]且用药安全性高的明胶作为壁材.
1 实验部分
1.1 试剂和仪器
蒿甲醚(工业级,东京仁成工业株式会社);明胶(B型,化学纯,天津市纵横兴工贸有限公司化工试剂分公司);无水乙醇、冰乙酸、甲醛均分析纯,均购自国药集团化学试剂有限公司;超纯水(电导率18.2 MΩ·cm).
北京赛多利斯公司BS110S型电子天平;金坛市科兴仪器厂85-2型恒温磁力搅拌器;河南省予华仪器有限公司DF-101S型智能集热式恒温加热磁力搅拌器;捷克TECNAI G2 20 S-Twin型透射电子显微镜.
1.2 纳米蒿甲醚胶囊的制备
本实验采用初生态微晶法制备纳米胶囊.将2 g明胶溶于100 mL水中,在室温下搅拌(约600 r/min)溶胀形成透明溶液,真空抽滤器抽滤,除去杂质. 取明胶溶液5 mL置25 mL烧杯中,于42 ℃恒温水浴中搅拌,将3 mL蒿甲醚无水乙醇溶液(2.3 mg/mL)匀速缓慢滴入,使上述混合溶液温度降至20 ℃,滴加适量20 %乙酸溶液,调至pH4.0. 继续降至15 ℃,慢慢滴入0.3 mL甲醛溶液.最后控制温度为5~10 ℃,搅拌30 min,使囊膜固化,得蒿甲醚纳米囊.
2 结果和讨论
2.1 电镜观察
图1为纳米胶囊的TEM图. 由图1可知,胶囊为球形粒子,囊形规则且较为分散.纳米胶囊囊芯部分颜色较深,为蒿甲醚晶体.明胶形成的纳米较薄,颜色较浅,与背景色较为接近,不易分辨. 但由图1中未见中心透明的空囊,说明此方法包封率高,适合对水溶性差的药物包裹,提高水中溶解性能.

图1 纳米蒿甲醚胶囊的透射电镜
2.2 蒿甲醚纳米胶囊形成理论
初生态微晶法制备纳米胶囊可归纳为3个过程,即: 1)囊芯微晶的形成. 将接近饱和的蒿甲醚无水乙醇溶液滴加至明胶溶液中,药物分子析出,形成一定尺寸的微晶; 2)囊材的聚凝. 在微晶体系中加入一定量的20 %冰乙酸溶液调体系pH接近明胶等电点,使其聚凝析出,包围在药物微晶外部.明胶凝聚层的出现阻止微晶继续长大,使之形成分散均匀,大小适宜的纳米粒子; 3)囊壁的交联.适宜温度下用甲醛将不同的明胶分子交联,形成连续的囊壁. 纳米胶囊制备理论阐释见图2.
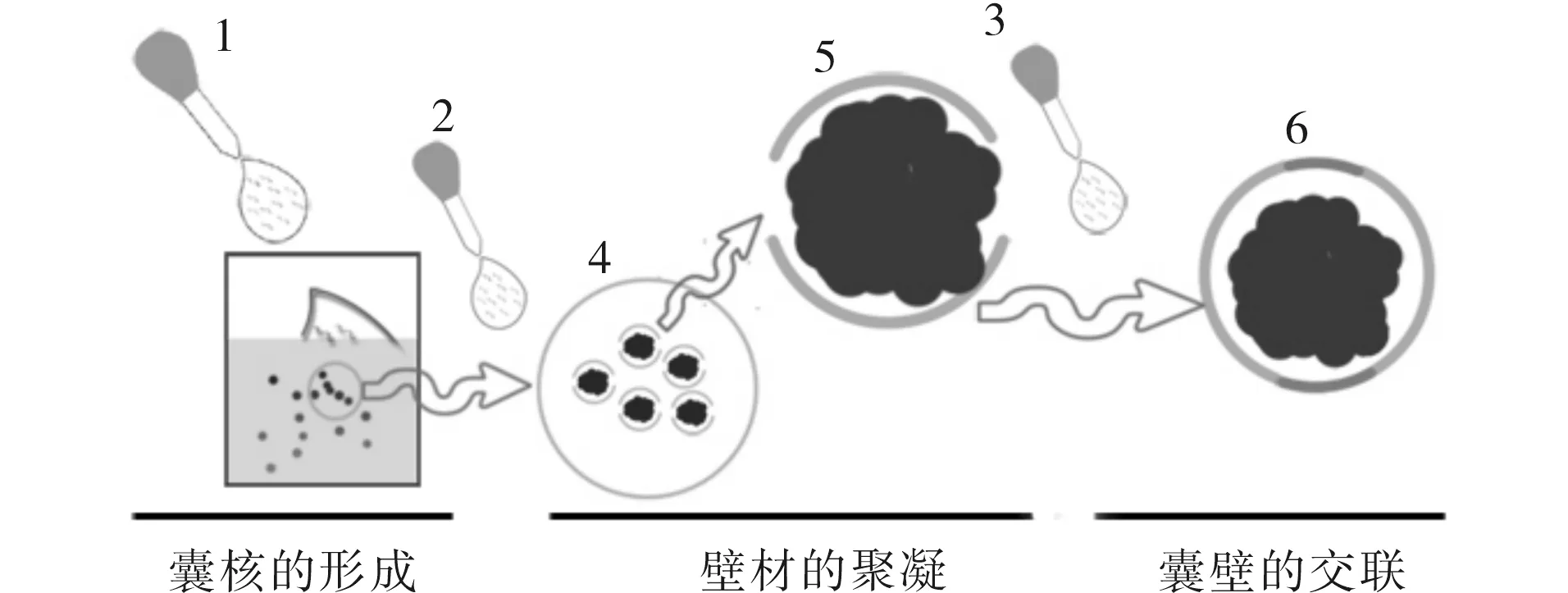
1)蒿甲醚溶液; 2)乙酸溶液;3)甲醛溶液; 4)局部放大;5)单个胶囊的放大; 6)甲醛交联后的胶囊
2.3 药物溶液浓度的影响
以无水乙醇作溶剂,溶解药物,囊材为明胶.由于明胶不溶于乙醇,因而实验中,当蒿甲醚用量相同时,乙醇用量影响体系中明胶分子及蒿甲醚存在的状态. 结果见表1.
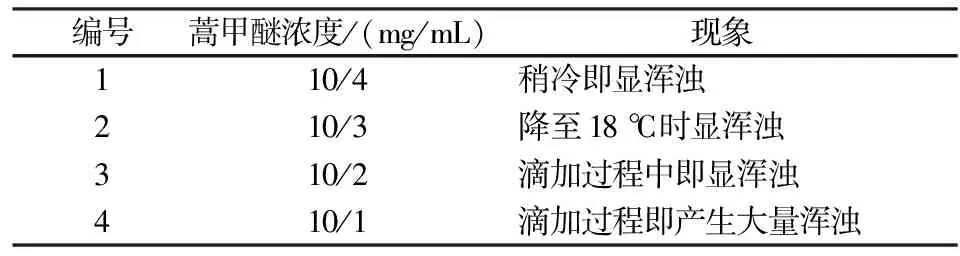
表1 不同药物浓度的影响
由表1可知,无论药品浓度过大或过小,体系均可过早产生浑浊.药品浓度较低时,乙醇用量变大,明胶极易析出;药品浓度高时,会造成局部浓度过大,蒿甲醚极易析出,也会造成浑浊,当蒿甲醚浓度取10 mg/3 mL时,实验结果较好.
2.4 不同pH时温度的确定
随着温度的降低,药物的溶解度将进一步减小.确定合适的温度,再调节体系pH,使壁材及时包围在微晶周围为本实验的关键. 通过一组对比试验(见表2)确定药物微晶析出的温度,基于此确定调节体系pH的温度.

表2 调节pH对温度的确定
由表2可知,在18 ℃时出现的浑浊物应为蒿甲醚晶体,而明胶此时则不会凝聚,因此调pH时所需温度>18 ℃.为保证药物既充分结晶而又不会过大,笔者选择20 ℃时调节体系为pH4.0.
2.5 甲醛用量的影响
甲醛在胶囊制备过程中起交联剂的作用.囊材沉积在微晶周围之后加入甲醛,不同明胶分子被甲醛交联,形成稳定的囊壁.甲醛的量对实验结果影响较大.过量的甲醛易导致胶囊之间交联形成凝胶;相反,可导致部分蒿甲醚胶囊囊材脱落,不利于胶囊的成型.
交联反应温度对实验结果影响重要.温度过高,交联速度快,形成的纳米囊可粘连一起,进而沉淀;温度过低,交联速度慢,体系中过量的明胶易聚沉析出. 实验确定较为理想的反应条件为0.3 mL甲醛于5~10 ℃下反应30 min.
2.6 其它因素的影响
此外,其他因素对实验结果也产生影响,但为次要,如:明胶溶液的初始温度、搅拌速度.考虑药物的稳定性及明胶的溶解度,选择42 ℃为明胶溶液的初始温度. 温度偏高可造成药物分子变性;温度较低,属大分子物质的明胶因此伸展不完全. 结果表明,约600 r/min搅拌速度较为理想.
3 结语
本实验采用初生态微晶法制备了载有蒿甲醚的纳米胶囊.采用该法制备克服了蒿甲醚不溶于水,代谢快及利用率低的缺点,因而可显著提高药效. 纳米蒿甲醚胶囊的出现有可能拓展蒿甲醚在临床上的应用途径,扩大应用范围.
[1]Yang H S,Ye Z G,Liang B W,et al.Studies on pharmaco-kinetics of artemether patch in rats [J].China Journal of Chinese Materia Medica, 2008,33(12):1459-1462.
[2]Ejiofor J I, Kwanashie H O, Anuka J A. Effect of arteme-ther on pentobarbitone sleep and electrical activity in rats [J]. Canadian Journal of Physiology and Pharmacology, 2007, 85(6): 582-587.
[3]Wang M.Determination of artemether in compound arteme-ther bablets by quantitative TLC scanning technique [J]. Chinese Journal of Pharmaceutical Analysis,1996,16(6):380-381.
[4]Yao J,Cheng Q L,Zhang Q M,et al.HPLC determination of artemether injection [J].Chinese Journal of Pharmaceutical Analysis, 2008, 28(1):91-92.
[5]Wang Z Y, Chen Z F. Determination of artemether in artemether capsules by HPLC [J]. Chinese Journal of Pharmaceutical Analysis, 2000, 20(3): 178-179.
[6]Wang J Y. A review of antimalarial Study [J]. Acta Parasitol Med Entomol Sin, 2001, 8 (2): 109-114.
[7]Catarina P R, Ronald J N, Anto′nio J R, et al. Nanoencapsulation I methods for preparation of drug-loaded polymeric nanoparticles [J]. Nanomedicine: Nanotechnology, Biology, and Medicine, 2006, 2(1): 8-21.
[8]Weber C, Kreuter J, Langer K. Desolvation process and surface characteristics of HSA-nanoparticles [J]. International Journal of Pharmaceutics, 2000, 196(2):197-200.
[9]Zillies J C, Zwiorek K, Hoffmann F, et al. Formulation development of freeze-dried oligonucleotide-loaded gelatin nanoparticles [J]. European Journal of Pharmaceutics and Biopharmaceutics, 2008, 70(2):514-521.
[10]Vandervoort J, Ludwig A. Preparation and evaluation of drug-loaded gelatin nanoparticles for topical ophthalmic use [J]. European Journal of Pharmaceutics and Biopharmaceutics, 2004, 57(2):251-261.
[11]Ofokansi K, Winter G, Fricker G, et al. Matrix-loaded biodegradable gelatin nanoparticles as new approach to improve drug loading and delivery [J]. European Journal of Pharmaceutics and Biopharmaceutics, 2010, 76(1):1-9.
[12]Das S, Suresh P K, Desmukh R. Design of eudragit RL 100 nanoparticles by nanoprecipitation method for ocular drug delivery [J]. Nanomedicine, 2010, 6 (2):318-323.
[13]Yordanov G G,Dushkin C D.Preparation of poly (butylc-yanoacrylate)drug carriers by nanoprecipitation using a pre-synthesized polymer and different colloidal stabilizers [J].Colloid and Polymer Science,2010,288 (9):1019-1026.
[14]Thomas P J, Naveen P , Mary D E, et al. Synthetic nanoparticle vaccines produced by layer-by-layer assembly of artificial biofilms induce potent protective T-cell and antibody responses in vivo [J]. Vaccine, 2011, 29 (3): 558-569.
[15]Mora-Huertas C E, Fessi H, Elaissari A. Influence of process and formulation parameters on the formation of submicron particles by solvent displacement and emulsification-diffusion methods: critical comparison [J]. Advances in Colloid and Interface Science,2011,163 (2):90-122.
[16]Rodríguez-Cruz I M, Domínguez-Delgado C L, Escobar-Chávez J J, et al. Nanoparticle infiltration to prepare solvent-free controlled drug delivery systems [J]. International Journal of Pharmaceutics, 2009, 371(1/2), 177-181.
[17]Chang S K, Seok L H, Yeop C, et al. The effect of type of organic phase solvents on the particle size of poly (d,l-lactide-co-glycolide)nanoparticles [J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2006, 276(1-3): 162-167.
[18]Xiao X C, Hong Z G. Firstborn microcrystallization method to prepare nanocapsules containing artesuante [J]. Int J Nanomed, 2010, 5: 1-4.
[19]Zhang T H,Hu X L,Qiao J C,et al.Progress on preparation and performance of nanocapsules [J]. Chemical Industry and Engineering Progress,2006,25(5):502-506.
[20]Cai M J, Zhu Y H, Yang X L. Preparation of gelatin submicron particles with emulsion method [J]. The Chinese Journal of Process Engineering, 2005, 5(6): 617-620.
