二苯胺磺酸钠指示剂终点颜色变化的探讨
2011-12-18陆志发
陆志发,卢 俊
(广西工业职业技术学院,广西 南宁530001)
二苯胺磺酸钠指示剂终点颜色变化的探讨
陆志发,卢 俊
(广西工业职业技术学院,广西 南宁530001)
以二苯胺磺酸钠作指示剂的重铬酸钾测定法是一种常用的容量分析法,主要用来测定样品中铁的含量,但在测定时,有时终点颜色得不到正常的紫色,而是出现墨黑色。文章对此现象进行了探讨并提出了一些解决方案。
二苯胺磺酸钠;重铬酸钾法;终点颜色
在分析化学实验实际生产化验中,重铬酸钾测定法是一种较常用的容量分析方法,主要用来测定亚铁盐、铁矿石或合金中铁的含量[1~3]。如测定铁粉中铁的含量时,先将含铁试样用盐酸溶解,使铁转变为易溶性的[FeCl4]-或[FeCl6]3-,然后用SnCl2将Fe3+还原为Fe2+,用HgCl2除去过量的SnCl2,在硫酸和磷酸的混合酸介质中,以二苯胺磺酸钠作指示剂,用K2Cr2O7标准溶液滴定至紫色,即为终点。在这实验过程中,有时得不到正常的紫色溶液,而是出现墨黑色溶液。这是什么原因导致的?是指示剂被氧化为别的物质了呢,还是终点时氧化还原电位发生了变化?对此现象,我们进行了相关实验。
1 材料与方法
1.1 原理
在硫酸和磷酸的混合酸介质中,亚铁铵矾中的二价铁离子可利用重铬酸钾法测定。
6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
以二苯胺磺酸钠作指示剂,正常情况下,滴定至溶液呈紫色为终点[4]。
1.2 仪器与试剂
ZD-2A型自动电位滴定仪,232型饱和甘汞电极;217型铂电极。
硫磷混合酸(1+1):边搅拌边将150mL硫酸(1.84g·L-1)慢慢注入700mL水中,加150mL磷酸(1.7 g·L-1)混匀。
硫酸亚铁铵溶液c[(NH4)2Fe(SO4)2·6H2O]=0.10mol·L-1: 称取19.70g硫酸亚铁铵溶解于硫酸(5+95)中稀释至1000mL,混匀。
重铬酸钾标准溶液c(1/6K2Cr2O7)=0.05000、0.1000、0.2000mol·L-1:按标准溶液配制方法制备。
二苯胺磺酸钠(C6H5NHC6H4SO3Na)溶液,2g·L-1。
实验用水均为去离子水。
1.3 方法
移取10.00mL硫酸亚铁铵溶液于100mL烧杯中,加入20mL硫磷酸混合酸,加水稀释至50mL左右,滴加4~6滴二苯胺磺酸钠溶液。放入洗净的搅拌子,将烧杯放在电磁搅拌器盘上,插入处理好的甘汞电极与铂电极,把电极线正确连接于测量仪器上。
开启搅拌器,调节转速。将仪器选择开关置“mV”位置上记录溶液的起始电位,然后滴加K2Cr2O7标准溶液,待电位稳定后读取电位值及相应的滴定剂加入体积。在滴定开始时,先加5mL标准滴定溶液记一次电位值,然后每次加入0.5mL或1.0mL标准滴定溶液记一次电位值,直至电位值发生突跃为止[4]。由此可得到终点体积及相应的终点颜色变化。
2 结果与讨论
2.1 重铬酸钾标准溶液浓度大小对终点颜色的
影响
固定待测Fe2+的量,用不同浓度的重铬酸钾标准溶液进行测定,观察电位突跃时溶液终点颜色的变化。从表1可以看出,当被测物铁的量为1.20mmol时,重铬酸钾标准溶液浓度大小对终点颜色没有任何影响。

表1 采用不同浓度的重铬酸钾标准溶液滴定时终点颜色的变化情况
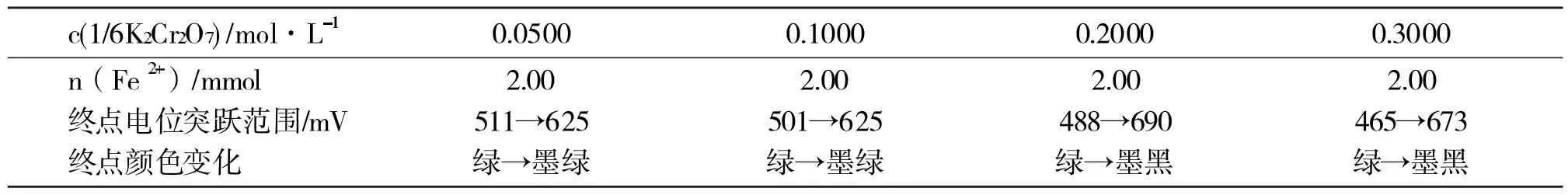
表2 采用不同浓度的重铬酸钾标准溶液滴定时终点颜色的变化情况
从表2可以看出,当被测物铁的量为2.00mmol时,不管采用任何浓度的重铬酸钾标准溶液进行滴定,都得不到正常的颜色变化(即从绿色→紫红色)。
2.2 被测物铁的取样量对终点颜色的影响
固定c(1/6K2Cr2O7)为0.1000mol·L-1,考察被测物铁取量不同时终点颜色的变化情况,结果见表3。
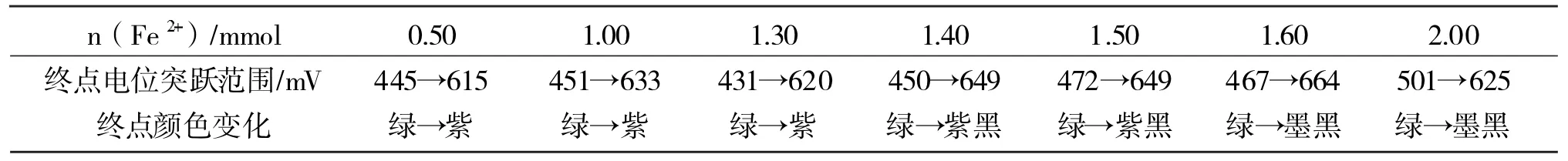
表3 被测物铁取样量不同时终点颜色的变化情况
从表3可以看出,当被测物铁的量n≤1.30mmol时,用c(1/6K2Cr2O7)=0.1000mol·L-1的重铬酸钾标准溶液进行滴定,终点的颜色变化正常 (从绿色→紫红色),当被测物铁的量n>1.30mmol时,终点时都发生异常的颜色变化。进一步的实验证明,不管采用任何浓度的重铬酸钾标准溶液进行滴定,都得到相同的实验结果。
2.3 二苯胺磺酸钠指示剂的加入量对终点颜色的影响
固定c(1/6K2Cr2O7)为0.1000mol·L-1,n(Fe2+)为2.00mmol,考察指示剂加入量对终点颜色的变化影响,结果见表4。
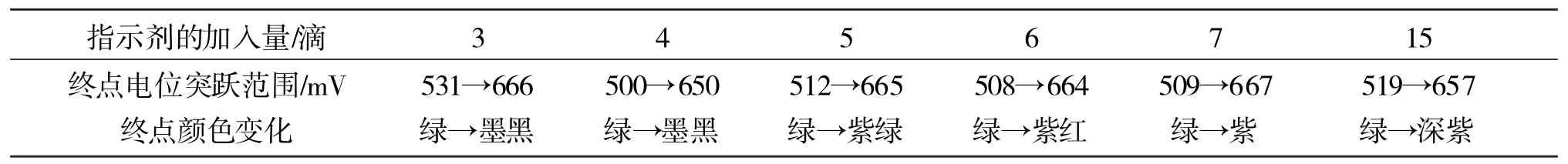
表4 不同的指示剂加入量时终点颜色的变化情况
从表4可以看出,当被测物铁的量为2.00mmol时,采用c(1/6K2Cr2O7)=0.1000mol·L-1重铬酸钾标准溶液进行滴定,指示剂的量<5滴,都得不到正常的颜色变化,但加大指示剂的量,又可以正常的颜色变化(从绿色→紫红色)。
2.4 掩蔽剂磷酸的加入量对终点颜色的影响
固定c(1/6K2Cr2O7)为0.2000mol·L-1,n(Fe2+)为2.00mmol,考察磷酸加入量对终点颜色的变化的影响,结果见表5。

表5 不同的磷酸加入量时终点颜色的变化
从表5可以看出,当被测物铁的量为2.00mmol时,采用c(1/6K2Cr2O7)=0.2000mol·L-1重铬酸钾标准溶液进行滴定,当硫磷混合酸的加入量<20mL,都得不到正常的终点颜色变化,但加大硫磷混合酸的量,滴定终点的颜色变化又恢复正常(从绿色→紫色)。
3 结论
将实验结果及讨论进行分析归纳得到如下结论:一是所有的实验其终点电位值都基本一样,从而排除了由于氧化还原电位发生变化而可能引起的指示剂的颜色异常;二是影响重铬酸钾容量法(以二苯胺磺酸钠作指示剂)终点颜色的因素是取样量、指示剂加入量及掩蔽剂磷酸的加入量。这是因为最后的终点颜色是由Fe3+的颜色(黄色)、二苯胺磺酸钠的氧化色(紫色)及Cr3+的颜色(绿色)共同作用的结果,终点颜色产生异常是由于3种颜色强度不同在终点时发生了光的互补现象而引起。若取样量过大,使得终点时的Fe3+及Cr3+的浓度增大,其色度就增大,从而使二苯胺磺酸钠被氧化时的紫色由于互补作用产生了颜色的偏离,这时如果加入大量的掩蔽剂磷酸,把Fe3+掩蔽起来,或者加入适量的指示剂二苯胺磺酸钠,加强在终点时紫红色的强度,都可以避免终点颜色异常。为此,使用重铬酸钾滴定法测定铁(以二苯胺磺酸钠作指示剂)时,可采用如下措施:
(1)控制称样量。所称样品含铁量在70mg以内或控制测定时消耗c(1/6K2Cr2O7)=0.1000mol·L-1重铬酸钾标准溶液在13mL以内。
(2)若称样量过大,适当加大掩蔽剂磷酸的量和指示剂的量。但指示剂的量不能过大,因为它会消耗重铬酸钾标准溶液体积而使结果偏高,如若采用必须要用标准样进行标定。
(3)为了避免测定终点颜色异常并得到较好的测定结果,建议采用电位滴定法。
[1]GB/T 223.7-2002,铁粉 铁含量测定 重铬酸钾滴定法[S].
[2]GB/T 6730.65-2009,铁矿石 全铁含量的测定 三氯化钛还原重铬酸钾滴定法[S].
[3]GB/T 223.73-1991,钢铁及合金化学分析方法三氯化钛-重铬酸钾容量法测定矿量[S].
[4] 穆华荣,陈志超.仪器分析实验[M].北京:化学工业出版社,2003.156-158.
Study on Endpoint Color Change of Sodium Diphenylamine Sulfonate
LU Zhi-fa,LU Jun
(Department of Petrolchemical Engineering,Guangxi Vocational&Technical Institute of Industry,Nanning 530001,China)
In the determination of iron content,K2Cr2O7methods with sodium diphenylamine sulfonate as indicator was one of the widely used capacity analysis methods in chemical analysis,but sometimes the endpoint color change was black not the normal purple color.This phenomenon was studied and some ideal solutions were provided.
sodium diphenylamine sulfonate;K2Cr2O7;;endpoint color
O 655.2
A
1671-9905(2011)11-0051-03
陆志发(1962-),男,汉族,广西昭平县人,石油与化学工程系教师,大学本科学历,实验师职称,主要从事分析化学仪器分析教学与实践工作,通讯地址:广西南宁市秀灵路37号广西工业职业技术学院石油与化学工程系,联系电话:0771-3828125,E-mail:spw530@163.com
2011-08-08
