含全氟壬烯基单体的合成与聚合
2011-12-08史鸿鑫陈立军武宏科项菊萍
史鸿鑫 黄 磊 陈立军 武宏科 项菊萍
(浙江工业大学,绿色化学合成技术国家重点实验室培育基地,杭州310032)
氟化工
含全氟壬烯基单体的合成与聚合
史鸿鑫 黄 磊 陈立军 武宏科 项菊萍
(浙江工业大学,绿色化学合成技术国家重点实验室培育基地,杭州310032)
制备了1种含有全氟壬烯基的单体,与其他单体聚合得到含氟共聚物乳液。全氟壬烯(I)和烯丙基(p-羟甲基苯基)醚(II),在催化剂存在下得到含氟单体p-全氟壬烯基氧基苯酚烯丙基醚(Ⅲ);以K2S2O8为引发剂,丙烯酸丁酯(BA)、甲基丙烯酸甲酯(MMA)和Ⅲ为共聚单体,采用乳液聚合的方法,制备了带蓝色荧光的含氟乳液。用傅立叶红外(FT-IR)、核磁共振(1H-NMR)、质谱(MASS)、接触角等手段对制备的含氟单体(Ⅲ)和Ⅲ-BA-MMA共聚物结构和性能进行表征。结果表明,当n(I):n(II)=1:1,丙酮作溶剂,吡啶存在下,室温反应6 h,含氟单体Ⅲ的收率为70.4%;引入含氟单体后,聚合物的疏水性有提高。水在含氟共聚物上的接触角随Ⅲ用量的增加而增大,当Ⅲ占单体总质量的25%时,水的接触角为85.6°。
全氟壬烯;含氟单体;氟代共聚物;乳液聚合;接触角
含氟单体是含氟整理剂的重要组成部分,与有机硅类和烃类整理剂相比,含氟整理剂在表面活性、防水、防油、防污、耐热性和耐腐蚀性等方面有着无可比拟的优点,已在纺织、涂料、建筑、光导纤维和国防材料等行业得到了广泛的应用。而含氟单体是合成含氟整理剂最关键的一步,开发含氟单体不仅具有很高的技术和经济价值,而且对我国材料行业的发展,改善材料品种结构都具有积极的意义[1-2]。目前,含氟聚合物单体大多是丙烯酸和甲基丙烯酸类,也有丙烯酰胺类单体和苯乙烯类含氟单体[3-10]。烯丙基类和马来酸酯类单体也有报道[8,11]。
目前含氟聚合物的含氟部分主要是全氟辛基磺酸(PFOS)及其衍生物,由于其在环境中有高持久性和累积性,存在潜在的危险,因而在美国、欧盟等发达国家受到严格限制。PFOS替代品已经成为新的研究热点,其中以六氟丙烯齐聚体作为聚合物的含氟基团是一种有效替代途径,早在1976年就有报道,但近年来报道较少[12-13]。
笔者以全氟壬烯(I)和烯丙基(p-羟甲基苯基)醚(II)为主要原料,合成了含氟单体p-全氟壬烯基氧基苯酚烯丙基醚(III),将其和丙烯酸丁酯(BA)、甲基丙烯酸甲酯(MMA)进行乳液聚合制得一种含氟共聚物乳液,并测试了水在含氟共聚物上的接触角。
1 实验部分
1.1 试剂与仪器
I,质量分数≥99%;II,质量分数≥99%。 MMA,BA,丙酮,吡啶,过硫酸钾(KPS),烷基酚聚氧乙烯醚(OP-10),十二烷基硫酸钠(SDS),碳酸氢钠,氨水,均分析纯。
Waters 515 HPLC Pump/Waters 2487 Dual λ Absorbance Decter液相色谱,AVATAR370 FTIR红外光谱仪,Mercury Plus 400核磁共振仪(400 MHz),DECAX-60000 LCQ Deca XP 质谱仪,Oca-20接触角测量仪。
1.2 III的合成
在带有回流冷凝器的100 mL四口烧瓶中,加入 20 mL 丙酮、1.6 g(0.02 mol)吡啶和 3.48 g(0.02 mol)II, 搅拌 5 min;20 ℃下缓慢滴加 9.00 g(0.02 mol)I,约30 min滴完,滴加完毕后室温搅拌反应6.0 h;将反应混合物注入20 mL质量分数2.5%的盐酸溶液中,分液,下层液体用10 mL质量分数5%盐酸洗1次,3×30 mL水洗,无水硫酸钠干燥。产物溶于六氟丙烯二聚体中,液体分2层,取下层,减压蒸馏除去六氟丙烯二聚体,得到黄色油状液,硅胶柱层析分离(V(环己烷):V(乙酸乙酯)=9:1),得淡黄色澄清油状液体。
反应式如下:

1.3 共聚物乳液的制备
在装有搅拌器、回流冷凝器的50 mL四口烧瓶中,加入去离子水、复配乳化剂和NaHCO3搅拌升温至75~80℃,同时滴加单体混合液和引发剂溶液,约3.0 h滴完,再保温反应2.0 h;冷却至室温,氨水调节pH=8~9,得带蓝色荧光乳液。其中乳化剂为0.2 g OP-10和0.1 g SDS复配,引发剂为0.12 g KPS,单体BA与MMA质量比为3:2,单体总量10 g。
反应式如下:
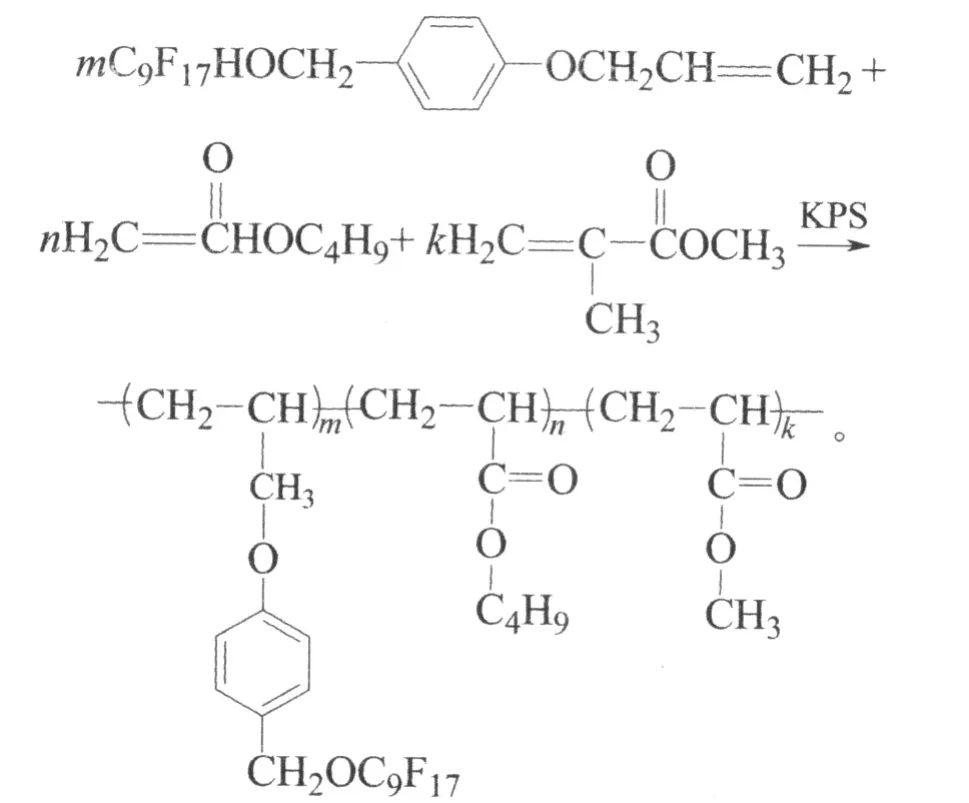
1.4 分析与表征
1.4.1 液相色谱
紫外检测器,ODS2反向填充柱,柱长150 mm,内径4.6 mm,数据处理采用面积归一法进行分析,检测波长226 nm,流动相为甲醇,体积流量为0.7 mL/min,进样量 1.0 μL。
1.4.2 红外光谱
将含氟乳液涂在载玻片上,自然烘干成膜,用红外光谱仪进行表征。
1.4.3 接触角
将含氟乳液均匀地涂在洁净的载玻片上,在空气中放置24 h,自然风干成膜。用接触角测量仪测量水对聚合物薄膜的接触角。
2 结果与讨论
2.1 III的表征
I的红外光谱:1 618.08 cm-1为C=C伸缩振动吸收峰,1 513.79 cm-1为苯环C=C伸缩振动吸收峰,1 192.58 cm-1和754.5 cm-1为C—F的伸缩振动吸收峰。
III的1H-NMR,δ(CD3OD):δa=7.25 (d,2H),δb=6.91(d,2H),δc=6.12~6.05(m,1H),δd=5.40(d,1H),δe=5.25(d,1H),δf,g=4.52~4.54(m,4H),
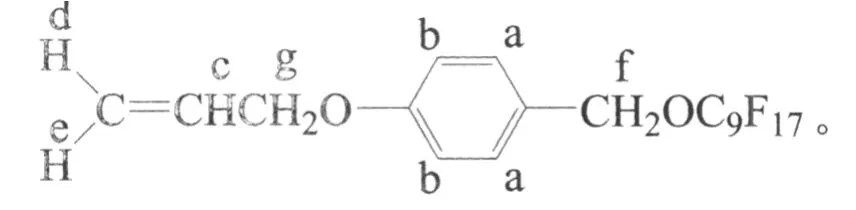
III的 EI-MS 谱,m/z:594.0([M]),147.4([CH2=CHCH2OC6H4CH2]+)。
2.2 III的合成
在极性非质子性溶剂丙酮中,催化剂吡啶存在下,II与I摩尔比为1:1反应合成含氟单体III。盐酸中和吡啶,水洗,无水硫酸钠干燥,得到产物III。为确定最佳反应条件,以产物收率为参考指标,考察反应温度和反应时间对反应的影响,得到较佳工艺条件。2.2.1 反应温度对III收率的影响
反应温度对产物收率的影响如表1所示。
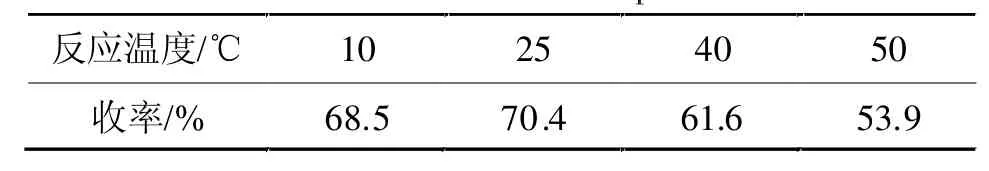
表1 反应温度对III的影响Tab 1 The effect of reaction tempretuie onIII
由表1数据可以看出,反应温度对III的收率有一定影响。反应温度为25℃时,产物收率最高,反应温度继续升高时,收率反而有所下降。这可能因为温度升高后副反应增加,使得III的收率下降。25℃接近室温,容易实现,所以含氟单体III合成的较佳反应温度为室温。
2.2.2 反应时间对III收率的影响
反应时间对产物收率的影响如表2所示。
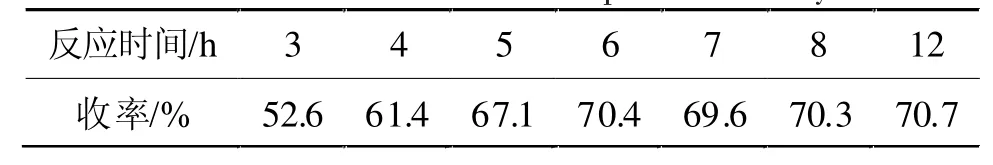
表2 反应时间对III收率的影响Tab 2 The effect of reaction tempretuie onIIIyeild
由表2数据可见,反应时间对III收率的影响较大。当反应时间6 h时,收率达到70.4%;反应时间继续延长,对产物收率的提高作用不大。所以III合成的较佳反应时间为6.0 h。
2.3 含氟共聚物
含氟共聚物III-BA-MMA乳胶膜的FT-IR谱图如图1所示。
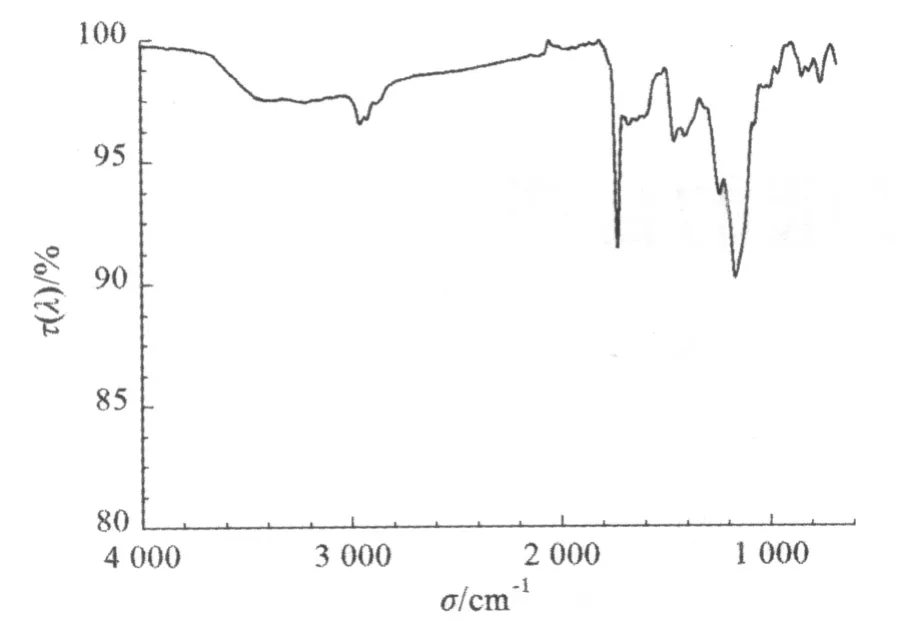
图1 共聚物III-BA-MMA的FT-IR图谱Fig 1 The FT-IR of copdymerIII-BA-NMA
图 1 中,2 956.9、2 916.9 和 2 864.8 cm-1为甲基和亚甲基中C—H键的对称伸缩振动和不对称伸缩振动吸收峰,1 729.9 cm-1为BA和MMA的酯基中C=O键的伸缩振动峰,1 676.8、1 456.1 cm-1为苯环的骨架振动吸收峰,1 239.6 cm-1为MMA和BA中 C—O—C 的伸缩振动峰,1 164.5、752.1 cm-1为C—F键的伸缩振动峰。图1表明,III与BA、MMA共聚制得了含氟聚合物。
2.4 III用量的影响
图2为含氟单体的用量对共聚物III-BA-MMA乳胶膜与水的接触角的影响。

图2 含氟单体用量对膜的接触角的影响Fig 2 Influence of the fluorine content on the contact angle of the film
由图2可以看出,在其他单体不变的情况下,含氟单体的用量越多,乳胶膜与水的接触角越大,当含氟单体质量分数达到25%时,共聚物乳胶膜与水之间接触角为85.6°,与没有含氟单体时涂膜与水的接触角约为35°相比,它具有一定的拒水性,接触角越大,拒水效果越好。这是因为C—F键的结合能大、键长短、键能高,含有大量C—F键的化合物分子间凝聚力小,使其表面能降低。在膜的成型过程中F原子趋向于分布在膜的表面,使得含氟聚合物具有良好的疏水性,而且含氟量越多疏水性越好。
3 结论
以丙酮作为溶剂,在催化剂吡啶存在下,I与II反应生成III,反应的较佳工艺条件为:丙酮20 mL,I 0.02 mol,n(II):n(I)=1:1,室温反应 6.0 h。在此条件下,III的收率为70.41%,
III与BA、MMA非氟单体共聚,采用乳液聚合方法,得到带有蓝色荧光的乳白色乳液聚合物。反应条件如下:m(OP-10):m(SDS)=2:1复配作为乳化剂,乳化剂用量为单体总质量的3%;以K2S2O4为引发剂,用量为单体总质量的0.6%~0.8%;反应温度为70~80℃。含氟乳液的疏水性较普通乳液有明显的提高,当含氟单体质量分数为25%时,与水的接触角为 85.6°。
[1]陈国强.纺织品整理加工用化学品[M].北京:中国纺织出版社,2009.
[2]罗巨涛,姜维利.纺织品有机硅及有机氟整理[M].北京:中国纺织出版社,1999.
[3]川口武行.含弗素不飽和单量体の製造法:JP,50052019[P].1975-05-09.
[4]清水弘明,白崎秀男,根本藤人.2-(ペルフルオロアルケニルオキシ)エチルアクリレートもしくはメタクリレート:JP,61010534[P].1986-01-18.
[5]丸山俊城,横尾秀次郎.フッ素化アルキルアクリレート類の製造方法:JP,61180743[P].1986-08-13.
[6]藤田和男,丹史郎.フルオロ脂肪族基含有高分子化合物:JP,2003221419[P].2003-08-05.
[7]松枝宏尚,小磯彰宏,高野聖史.フッ素系界面活性剤及びそれを用いた感光性組成物:JP,2008269978[P].2007-10-18.
[8]David K Johnson,Patricia M Savu.Acrylic surfactants and compositions containing those surfactants:US,5270378[P].1993-12-14.
[9]Schmidt Donald L,Coburn Charles E,McCrackin Perry J.Fluorocarbon-containing reactive polymeric surfactants and coating compositions therefrom and process for preparing the same:EP,0293963[P].1988-12-07.
[10]Yoshio Hayakawa,Taizo Ono.Facile synthesis of polystyrene bearing highly branched perfluorinated groups[J].European Polymer Journal,2006,42(6):1357-1361.
[11]腾原豊,小松忠名.ヘキサフルオロプロペソオリゴマー残基を有するフルオロオルガノシリコソ化合物およびその用途:JP,53147029[P].1978-12-21.
[12]水野哲也,中村誠一,三上太平,等.高分子撥水撥油剤:JP,51023489[P].1976-02-25.
[13]中村誠一,水野哲也,三上太平,等.撥水撥油剤:JP,52007882[P].1977-01-21.
Preparation and Polymization of a Monomer Containing Perfluorononyleneyl
Shi Hongxin,Huang Lei,Chen Lijun,Wu Hongke,Xiang Juping
(State Key Laboratory Breeding Base of Green Chemistry Synthesis Technology,Zhejiang University of Technology,Hangzhou 310032)
A monomer containing perfluorononyleneyl was synthesized and co-polymerized with other monomers for a copolymer emulsion.p-Perfluorononenoxy-phenoxymethyl allyl ether(Ⅲ)was synthesized from perfluorononene(I)and allyl p-hydroxymethylphenol ether(II)in the presence of a catalyst.The fluorinated-copolymer emulsion with blue-fluorescence was prepared by emulsion polymerization initiated by K2S2O8from butyl acrylate(BA),methyl methacrylate(MMA)andⅢ.The monomerⅢ andⅢ-BA-MMA copolymers were characterized by FT-IR,1H-NMR,MS and/or contact angle measurement respectively.The yield ofⅢis 70.4%when n(I):n(II)=1:1,in the presence of pyridine and acetone as solvent at room temperature for 6 h.The hydrophobicity of the copolymer is improved when the fluorinated monomerⅢ is introduced.The water contact angle is 85.6°when 25% Ⅲ is used in the copolymer.
perfluorononene;fluorinated-monomer fluorinated copolymer;emulsion polymerization;contact angle
TQ325.7
ADOI10.3969/j.issn.1006-6829.2011.03.001
2011-04-12
