超声处理对大豆分离蛋白溶解性和乳化活性的影响
2011-11-28孙燕婷黄国清肖军霞仇宏伟
孙燕婷 黄国清 肖军霞 仇宏伟
超声处理对大豆分离蛋白溶解性和乳化活性的影响
孙燕婷 黄国清 肖军霞 仇宏伟
(青岛农业大学食品科学与工程学院,青岛 266109)
采用超声波处理大豆分离蛋白,观察对其溶解性和乳化活性的影响。结果表明,超声处理时的温度和时间、NaCl浓度以及大豆分离蛋白浓度均会影响其溶解性和乳化活性。0.01 g/mL的大豆分离蛋白溶液调节pH 6.0,在室温(23~25℃)下采用500 W超声功率处理5 min时,其溶解度最大达1 023μg/mL,是未超声处理(805.9 μg/mL)的1.3 倍,乳化活性达18.3 mL/g,是未超声处理(11.9 mL/g)的 1.5 倍。超声处理可以显著提高SPI的溶解性和乳化活性,这为拓宽其在食品工业中的应用提供了理论依据。
大豆分离蛋白 超声处理 溶解性 乳化活性
大豆分离蛋白(Soy protein isolate,SPI)因具有较高的营养价值和功能特性而成为食品加工中的重要原料。但生产过程中采用碱溶酸沉的提取方法,造成部分蛋白质变性而降低或丧失某些功能特性[1-2],如溶解性和乳化性,这在一定程度上限制了它的应用范围。对SPI进行功能特性的改善是目前研究的热点,国内外学者主要是通过物理或化学手段来改善其溶解性和乳化性能,包括加热、酸沉、酶改性、磷酸化和乙酰化等方法[3-6],但这些方法反应激烈、副产物多,效果不太理想,而超声波是一种物理改性方法,通过改变蛋白质的次级结构来改变蛋白质的理化性能,从而达到改善或者加强蛋白质功能的目的。
超声波处理的主要原理是超声波在液体中能产生空化作用,超声空化是指在超声场中液体中的微小气泡随声压变化而产生强烈振荡,膨胀及崩溃的一系列动力学过程,该过程所产生的瞬时强压力和局部温度升高能对溶液中悬浮的粒子产生强烈声化学效果[7]。本研究主要观测超声处理对SPI溶解性及乳化活性的影响,拟找到提高大豆分离蛋白溶解性和乳化活性的方法,从而拓宽其在食品工业中的应用范围。
1 材料与方法
1.1 材料与试剂
SPI(纯度为90%):食品级,青岛天新食品添加剂有限公司;福临门大豆色拉油:食用级,中粮东海粮油工业(张家港)有限公司;牛血清蛋白:天津市巴斯夫化工有限公司;考马斯亮蓝G-250(AR):天津市巴斯夫化工有限公司;十二烷基磺酸钠(AR):烟台市三和化学试剂有限公司;其他试剂均为分析纯。
1.2 仪器与设备
KQ-500B型超声波清洗器(功率为500 W):昆山市超声仪器有限公司;LG10-2.4A高速离心机:北京医用离心机厂;UV-2000分光光度计:上海尤尼科仪器有限公司;DK-98-II型恒温水浴锅:天津市泰斯特仪器有限公司;90-3型双向定时恒温磁力搅拌器:上海泸西分析仪器厂有限公司;迷你多功能漩涡混合振荡器:上海人和科学仪器有限公司;万分之一分析天平:上海方瑞仪器厂。
1.3 试验方法
1.3.1 SPI溶液的超声处理
在超声功率500 W下,配制一定浓度的SPI溶液,设置试验需要的不同超声处理条件包括处理时间,处理温度等,将盛有SPI溶液的锥形瓶放入超声波清洗器中,使SPI溶液面浸入清洗器液面约2~3 cm进行超声处理。
1.3.2 牛血清白蛋白标准曲线的绘制
采用考马斯亮蓝G250染色法[8]。取6支10 mL的带塞试管,分别加入1 000μg/mL的牛血清白蛋白溶液 0、0.1、0.2、0.3、0.4、0.5 mL 后补足蒸馏水到 1 mL,从而得到0~500μg/mL的牛血清白蛋白稀释溶液,取各浓度的稀释液0.1 mL置另外6支带塞试管中,分别加入5 mL 100μg/mL的考马斯亮蓝G250溶液,漩涡振荡混匀,2 min后测定595 nm下各试管的吸光值,并绘制标准曲线。
1.3.3 溶解度的测定
参考1.3.2的方法,测定SPI溶液中可溶性蛋白质的浓度,用每毫升水溶液中溶解的SPI的微克数来表示溶解度[9-10]。将不同条件下得到的SPI溶液摇匀,10 000 r/min离心10 min,取上清液0.1 mL 于10 mL带塞试管中加入5 mL 100μg/mL的考马斯亮蓝G250溶液,漩涡振荡混匀,2 min后以考马斯亮蓝G250溶液调零,在595 nm下测定其吸光值。
1.3.4 乳化活性的测定
SPI的乳化性可用乳化活性EAI来表示,采用Molina[11]及 Tang[12]的方法测定乳化活性(EAI),取一定体积一定质量浓度的SPI溶液,加入1/3体积的大豆色拉油,以10 000 r/min的速度高速搅拌5 min后,取1 mL乳化液加入9 mL蒸馏水稀释,另取1 mL稀释液与9 mL 1 g/kg的十二烷基磺酸钠(SDS)溶液混合均匀,用SDS(1 g/kg)做空白对照在500 nm下测吸光值。按下列公式计算:
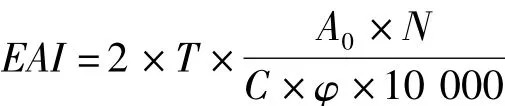
式中,EAI为乳化活性/mL/g;T=2.303;C为乳化液形成前蛋白质水溶液中蛋白浓度/g/mL;φ为乳化液中油的体积分数;N为稀释倍数。
1.4 数据处理
试验平行测定3次,采用SAS8.1对数据进行显著性及相关性分析。
2 结果与分析
2.1 牛血清白蛋白标准曲线
牛血清白蛋白标准曲线如图1所示。该标准曲线的线性方程为:y=0.000 9x+0.014 3,回归系数R2=0.991 6,线性良好,因此可通过该标准曲线计算出SPI溶液中蛋白质的浓度。
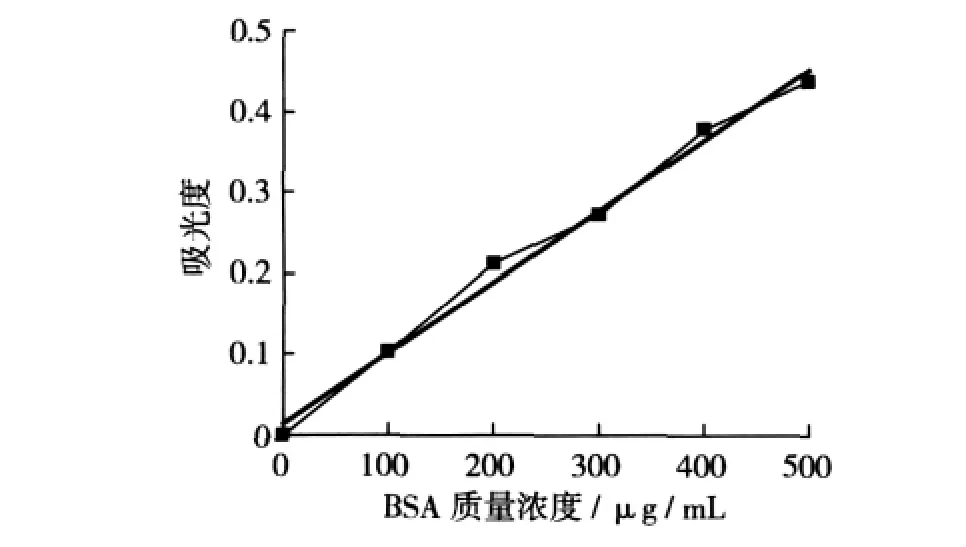
图1 牛血清白蛋白标准曲线
2.2 未经超声处理时pH对SPI溶解性及乳化活性的影响
室温(23~25℃)下配制0.008 g/mL的SPI溶液7份,每份20 mL,分别调节到不同pH,不同pH对SPI溶解度和乳化活性的影响见图2。由图2可知,各pH组之间SPI溶液的溶解度都呈极显著差异(P<0.01),说明pH严重影响到SPI的溶解性。pH 1、pH 3、pH 4.5、pH 5 组之间的 SPI乳化活性呈极显著差异(P<0.01)。SPI在等电点4.5时其溶解性和乳化活性最低,与其他pH组都呈极显著性差异(P<0.01),这主要是因为蛋白质在等电点刚好呈电中性,分子之间缺乏静电推斥力,因疏水相互作用导致蛋白质的聚集和沉淀,降低了此条件下蛋白质的溶解性[13]。在pH 4.5以上,随着 pH 的升高 SPI的溶解度和乳化活性同时增加,SPI在弱酸性环境中的溶解度和乳化活性偏低,限制了在食品工业中的应用范围,提高SPI在弱酸性条件下溶解度和乳化活性是亟待解决的问题,因此以下试验环境选用SPI溶液的pH 为 6.0。
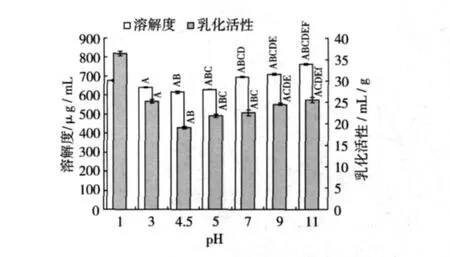
图2 pH对SPI溶解性及乳化活性的影响
2.3 超声处理对SPI溶解性及乳化活性的影响
2.3.1 超声处理时间对SPI溶解性及乳化活性的影响
室温下配制0.008 g/mL的SPI溶液8份,每份20 mL,调节pH 6.0,在功率为500 W下分别超声处理不同时间测定其溶解度及乳化活性,结果如图3所示。当超声处理5 min时SPI的溶解度和乳化活性分别最大达928.9μg/mL和22.3 mL/g,且与其他组比较均具有极显著性差异(P<0.01)。原因可能是超声处理产生强有力的空化和机械作用打断了可溶蛋白成分的四级结构,短时间内释放出的小分子亚基或肽分散到溶剂中,使溶解度出现最大值,当处理时间过长时,超声浸提完全后能量不足以将原有的小分子继续打断,从而溶解度变化不大,而此时乳化能力下降后趋于平稳,这可能是由于溶液经超声处理后,蛋白质三级结构破坏较完全且充分溶解,形成足够的界面来稳定油滴所致[10]。因此以下试验过程选用超声处理时间为5 min。
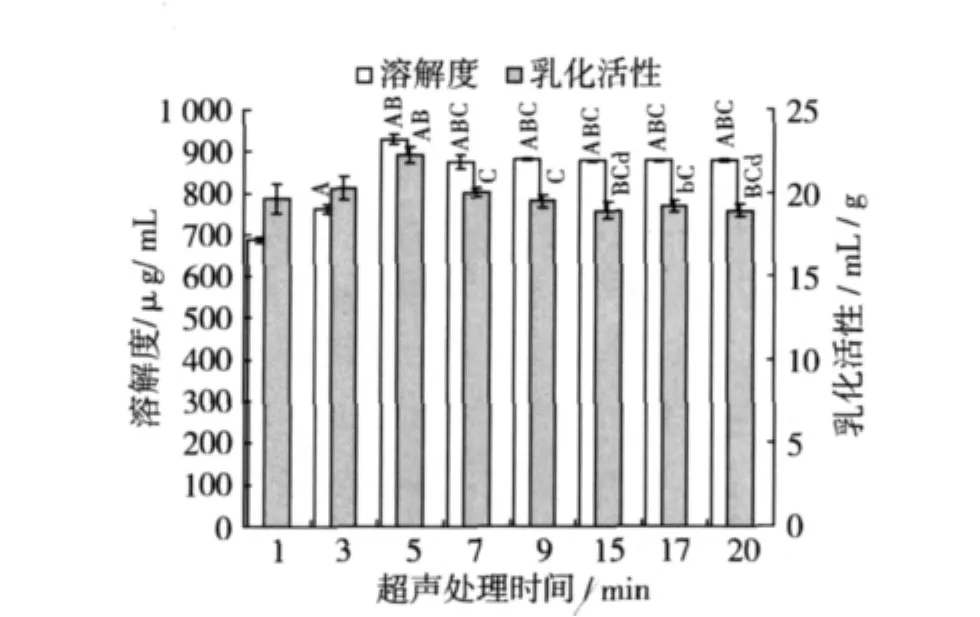
图3 超声处理时间对SPI溶解性及乳化活性的影响
2.3.2 超声处理温度对SPI溶解性及乳化活性的影响
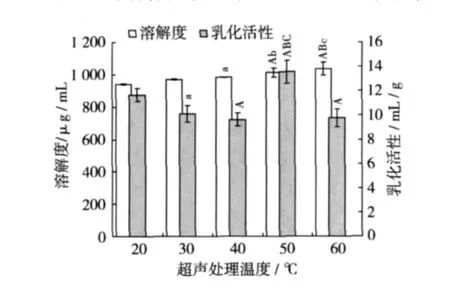
图4 超声处理温度对SPI溶解性及乳化活性的影响
配制0.008 g/mL的SPI溶液5份,每份20 mL,调节pH 6.0,在功率为500 W下以不同温度超声处理5 min,冷却至室温后测定溶解度及乳化活性,结果如图4所示,温度对溶解度和乳化活性的影响程度不一致。SPI的溶解度随着温度升高而不断增加,60℃时SPI的溶解度最大,但与50℃组比较没有显著性差异。当处理温度为50℃时,SPI溶液的溶解度达1 013μg/mL,与20℃、30℃组比较分别呈极显著(P <0.01)、显著(P <0.05)性差异;50 ℃时乳化活性最大达13.6 mL/g,与低温组(20、30、40 ℃)比较呈极显著性差异(P<0.01),但相对于室温下只超声处理5 min的样品来说,乳化活性却明显降低了,考虑到温度太高容易导致SPI的热变性影响其溶解性和乳化活性[14],所以以下试验选用室温。
2.3.3 超声处理下NaCl浓度对SPI溶解度和乳化活性的影响
室温下配制0.008 g/mL的SPI溶液5份,每份10 mL,调节 pH 6.0,分别向其中加入 0.05、0.10、0.15、0.20、0.30 g 的 NaCl,充分溶解,在超声功率500 W的条件下超声处理5 min,并与未经超声处理的样品组进行对照比较,结果如图5,图6所示。超声处理前后SPI的溶解度和乳化活性都随NaCl的变化呈先增加后降低的趋势。经超声处理后,0.015 g/mL NaCl的SPI溶液的溶解度和乳化活性均取得最大值,并与其他各组相比都呈极显著性差异(P <0.01),此时 SPI的溶解度达 587.4 μg/mL,是未超声处理(318.6μg/mL)的1.8倍;而乳化活性达9.1 mL/g,是未超声处理(7.6 mL/g)的 1.2 倍。0.008 g/mL的SPI溶液中不含有NaCl时,在同样条件下,其溶解性和乳化活性分别是928.9μg/mL和22.3 mL/g。由此可知,0.015 g/mL NaCl降低了 SPI的溶解性和乳化活性,而超声处理虽然可以提高其溶解性和乳化活性,但相比不经过NaCl处理的SPI溶液,其溶解性和乳化活性还是偏低。这说明SPI溶液中的NaCl浓度偏高,大部分水分子与NaCl牢固的结合,使之不能满足SPI溶剂化所需水分子的要求,因此,SPI-SPI的相互作用比SPI-水的相互作用更强,这样便导致SPI分子聚集,从而使SPI的溶解度和乳化活性降低[4]。
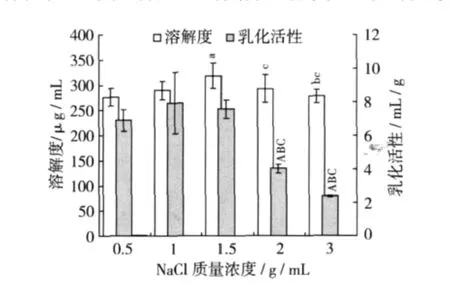
图5 NaCl浓度对SPI溶解性及乳化活性的影响
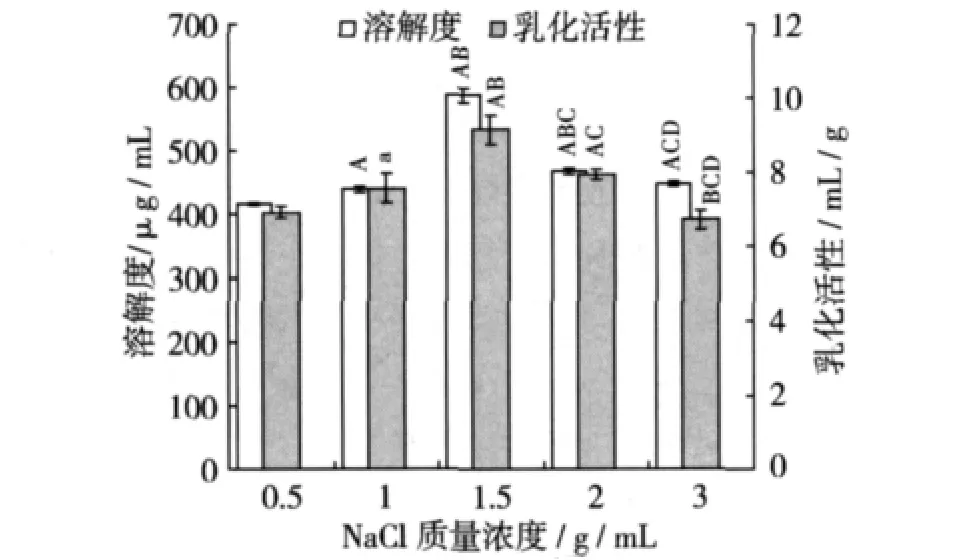
图6 超声处理下NaCl浓度对SPI溶解性及乳化活性的影响
2.3.4 超声处理下SPI浓度对其溶解度和乳化活性的影响
室温下配制不同浓度的SPI溶液6份,每份10 mL,调节pH 6.0,在超声功率500 W的条件下超声处理5 min,与未经超声处理的样品组进行对照比较,结果如图7,图8所示。在试验浓度范围以内,SPI的溶解性都随其浓度的增加而增加,且各组之间都呈极显著性的差异(P<0.01)。未经超声处理的SPI溶液乳化活性在浓度为0.002 g/mL时最大,随着SPI浓度的增加,乳化活性呈下降趋势,这说明低浓度时蛋白质分子彼此靠在一起形成胶束,此时胶束的形成有利于乳化活性的提高,但乳化液达到临界胶束浓度(CMC)时,油水界面上的乳化剂不随浓度增加而增多,以至乳化活性不再升高 。经超声处理的SPI溶液乳化活性随其浓度的变化而变化,0.008 g/mL溶液的乳化活性最大,但与 0.01 g/mL SPI比较没有显著差异。当SPI为0.01 g/mL时,超声处理后的SPI溶解度最大达1 023μg/mL,是未超声处理(805.9 μg/mL)的 1.3 倍,乳化活性达 18.3 mL/g,是未超声处理(11.9 mL/g)的 1.5 倍,这说明超声处理可以显著提高SPI的溶解性和乳化活性。
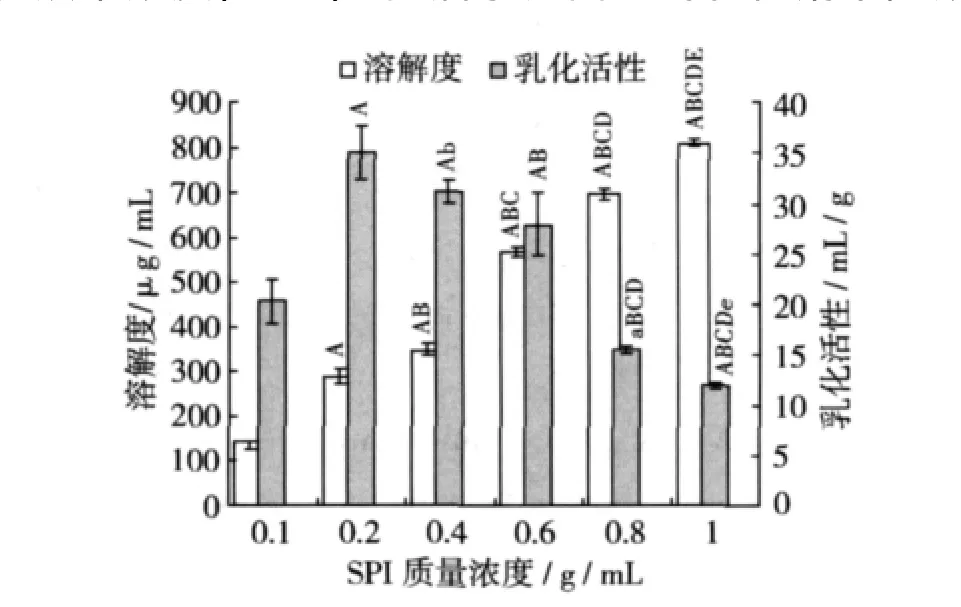
图7 SPI 浓度对其溶解性及乳化活性的影响
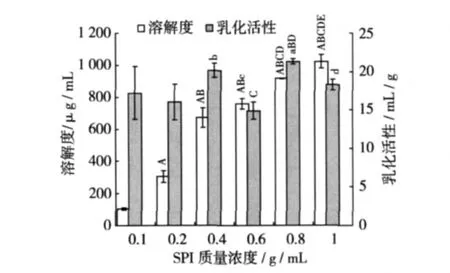
图8 超声处理下SPI浓度对其溶解性及乳化活性的影响
3 结论
SPI在蛋白质等电点时,其溶解度和乳化活性最小。随着pH的升高SPI的溶解度和乳化活性同时增加。为了提高SPI在pH 6.0弱酸性条件下溶解度和乳化活性,采用功率为500 W的超声波处理不同条件下的SPI溶液,观察其溶解度和乳化活性的变化情况。结果表明,在超声处理5 min时,SPI的溶解度和乳化活性取得最大值,且与其他各组均具有极显著性差异(P<0.01),因此确定最佳超声时间为5 min;而当超声处理温度为50℃时,虽然SPI的溶解度和乳化活性相比于低温度组差异显著,但与室温下只经过超声处理5 min的样品相比较,溶解性变化不大,乳化活性却明显降低了,选用室温经超声处理仍然符合试验的要求。
0.008 g/mL的SPI溶液,室温下采用500 W超声功率处理5 min,0.015 g/mL NaCl降低了 SPI的溶解性和乳化活性;当SPI浓度在0.001~0.01 g/mL时,室温下采用500 W超声功率处理5 min时,SPI的溶解性都随其浓度的增加而增加,且各组之间都呈极显著性的差异(P<0.01);而SPI乳化活性随其浓度的变化而变化,0.008 g/mL SPI溶液的乳化活性最大,但与0.01 g/mL SPI比较没有显著差异;SPI在0.01 g/mL时,溶解度和乳化活性分别达1 023μg/mL和18.3 mL/g,分别是未超声处理的1.3倍和1.5倍,这说明超声处理可以显著提高SPI的溶解性和乳化活性,该研究为SPI在酸性食品中的应用提供了理论基础。
[1]Delia A S,Jorge R W.Comparative study of foaming properties of whey and isolate soybean protein[J].Food research international,2002,35:721 -729
[2]谢良,王璋,蔡宝玉.大豆分离蛋白的组成与功能性质[J].中国粮油学报,2000,12(6):6 -10
[3]周瑞宝,周兵.蛋白质的生物和化学改性[J].中国油脂,2000,25(6):181 -185
[4]李秀川,迟玉杰.大豆分离蛋白溶解性能与水解度相关的研究[J].中国粮油学报,2009,24(7):38-40
[5]海日罕,迟玉杰.微波辅助磷酸化改性提高大豆分离蛋白乳化性的研究[J].中国粮油学报,2009,24(6):37 -39
[6]Liu C,Wang X S,Mah,et al.Functional properties of protein isolates from soybeans stored under various conditions[J].Food Chem,2008,111(1):29 -37
[7]郑家丰.大豆蛋白的功能特性研究[J].中国粮油学报,1996(4):21-24
[8]张水华.食品分析[M].北京:中国轻工业出版社,2004:164
[9]朱建华,杨晓泉,邹文中,等.超声处理对大豆分离蛋白功能特性的影响[J].食品科学,2004,25(7):58
[10]袁道强,杨丽.超声波改性提高大豆分离蛋白酸性条件下溶解性的研究[J].粮食与饲料工业,2008,1:28
[11]Molina E,Papadopoulou A,Ledward D A.Emulsifying properties of high pressure treated soy protein isolate and 7Sand 11Sglobulins[J].Food Hydrocolloids,2001(15):263-269
[12]Tang Chuanhe,Yang Xiaoquan,Chen Zhong,et al.Physicochemical and structural characteristics of sodium caseinate biopolymers induced by microbial transglutaminase[J].Journal of Food Biochemistry,2005,29(4):402 -421
[13]杨帆,童正明,戴杏云.大豆分离蛋白的性质分析与改性研究[J].食品研究与开发,2006,27(7):87-89
[14]郭凤仙,熊幼翎,何志勇,等.热处理对大豆分离蛋白功能特性的影响[J].食品与机械,2009,25(6):55-57
[15]张根生,岳晓霞,李继光,等.大豆分离蛋白乳化性影响因素的研究[J].食品科学,2006,27(7):49.
Effects of Ultrasonic Exposure on the Solubility and Emulsifying Properties of Soy Protein Isolate
Sun Yanting Huang Guoqing Xiao Junxia Qiu Hongwei
(College of Food Science and Engineering,Qingdao Agricultural University,Qingdao 266109)
The objective of this paper is to explore the effect of ultrasonic exposure on the solubility and emulsifying properties of soy protein isolate(SPI).The results showed that ultrasonic treatment temperature,duration,and NaCl and SPIconcentration significantly influenced the solubility and emulsifying properties of SPI.The maximum solubility was obtained in the SPI concentration 0.01 g/mL,pH 6.0,ultrasonic power 500 W,and exposure duration 5 min in room temperature(23 ~25 ℃),which reached up to 1 023 μg/mL,1.3 times higher than untreated SPI(805.9 μg/mL).Under these conditions,the emulsion capacity reached 18.3 mL/g,1.5 times higher than untreated SPI(11.9 mL/g).Hence,ultrasonic exposure can significantly improve the solubility and emulsifying properties of SPI.This paper has provided a theoretical basis for the application of ultrasonic treatment in the food processing industry.
soy protein isolate,ultrasonic Tech-nology,solubility,emulsifying property
TS201
A
1003-0174(2011)07-0022-05
山东省自然科学基金(6210a7)
2010-08-13
孙燕婷,女,1986年出生,硕士,食品科学
肖军霞,女,1977年出生,副教授,硕士生导师,功能性成分与微囊化
