用季铵盐从模拟钨矿苏打浸出液中直接萃取钨
2011-11-24关文娟张贵清
关文娟, 张贵清
用季铵盐从模拟钨矿苏打浸出液中直接萃取钨
关文娟, 张贵清
(中南大学 冶金科学与工程学院, 长沙 410083)
针对从钨矿碱性浸出液中直接萃取钨制取仲钨酸铵(APT)工艺萃取分相慢、反萃液中WO3浓度偏低的问题,采用季铵盐三辛基甲基氯化铵(Tri-n-octylmethyl-ammonium chloride,TOMAC)为萃取剂,对从钨矿苏打浸出模拟料液中直接萃取钨进行研究,分别考察钨矿浸出液中 Na2CO3浓度、反萃剂组成及浓度对萃取和反萃取过程的影响;分别绘制萃取等温线和反萃取等温线,并结合Kremser方程选择合适的反萃流比以及逆流反萃级数,用离心萃取器模拟逆流串级萃取与反萃取实验。结果表明:料液中Na2CO3浓度对WO3萃取率影响不大,但对萃取过程分相性能影响较大;当萃取剂浓度为50%(体积分数)时,有机相饱和萃钨容量(以WO3计)为91.49g/L;向反萃剂NH4HCO3中加入NH3·H2O,不仅能提高反萃液(钨酸铵溶液)的稳定性,而且有利于提高反萃液中WO3的浓度。实验条件下分相良好,反萃液中WO3浓度达到160 g/L左右,杂质含量完全可以满足生产0级APT的需要。
钨;溶剂萃取;季铵盐;Na2CO3体系
在钨冶金过程中,钨矿物大多采用碱法(苏打或苛性钠)工艺分解,分解得到的浸出液中含有大量游离的NaOH或Na2CO3以及少量的P、As和Si等杂质,从该碱性浸出液中提取钨制取仲钨酸铵(APT)的主要工艺有离子交换法和溶剂萃取法[1−3]。
目前,工业上广泛采用的是强碱性阴离子交换法,该法能在转型的同时除去P、As和Si等杂质,具有流程短、钨损少的优点,因而在我国获得了广泛的应用。但是,该工艺要求控制较低的吸附原液(WO3)浓度(15~25 g/L),需将钨矿碱分解液(100~200 g/L WO3)加水高倍稀释,因而耗水量和废水排出量巨大,每生产1 t 仲钨酸铵约排放53 m3废水,且废水中P和As含量大大超过国家废水排放标准,必须经过处理才能排放,使得处理成本增加。另外,钨矿碱分解液中的游离碱随交换废水排出,不仅无法利用,而且需要消耗无机酸中和;离子交换工艺中的APT结晶母液因含有Cl−而不能返回主流程,需设专门工序处理,也给整个工艺增加了负担[4−5]。鉴于日益严重的水资源紧缺问题和日益严格的环保要求,离子交换工艺的发展受到了极大的限制[6]。
目前,工业上使用的溶剂萃取工艺在酸性介质(pH=2~3)中进行,与离子交换法相比,酸性萃取法中钨矿碱分解液不需稀释,耗水量少,且结晶母液能直接返回主流程处理,不需辅助作业,萃取级数少且过程连续。但是,该工艺需要消耗大量的酸以中和钨矿碱分解液中的残余碱,使得有价酸及存在于浸出液中的游离碱变成外排萃余液中的无机盐。随着日益严格的环保要求,处理这种含盐量很高的萃余液成为一个紧迫的问题[7−8]。此外,酸性萃取仅起转型作用而不能除去P、As及Si等阴离子杂质,流程中仍需保留单独除杂作业,P、As及Si渣需设较复杂辅助流程处理,流程长且伴随着钨的损失。
鉴于此,各国科技工作者试图开发从钨矿碱分解液中生产APT的新方法,其中,以季铵盐从碱性介质中直接萃取钨的新方法最具吸引力。早在20世纪60年代,美国学者DROBNICK和LEWIS就研究了用季铵盐从含有CO32−的钨酸钠溶液中萃取钨的规律[9];我国科技工作者也为此进行了不懈的努力[10]。但鉴于该方法在技术上的困难,直至20世纪80年代,前苏联学者创造性的研究工作才获得了具有工业前景的研究结果,他们选择以 CO32−季铵盐为萃取剂、NH4HCO3为反萃剂、NaOH为再生剂的萃取体系,从钨矿苏打高压浸出液中直接萃取钨制取钨酸铵溶液[11]。20世纪90年代以来,张贵清等[12−14]在此基础上对季铵盐从钨矿苛性钠浸出液中直接萃取钨进行研究,在实验室实现了在转型的同时除杂制取纯钨酸铵溶液。随后,廖春发等[15−17]进一步对稀释剂的筛选和杂质 Sn在萃取过程中的行为进行了研究。上述研究表明:季铵盐碱性萃取工艺能在转型的同时除去P、As和Si等杂质,钨矿碱浸出液萃取前不需稀释,且萃余液可以返回钨矿浸出使用,萃取工序能与浸出工序形成水的闭路循环,具有流程短、碱耗低、水耗少及无大量含钠废水产生等优点,是一种极具工业应用前景的钨湿法冶金清洁工艺[18]。
上述研究为碱性介质直接萃取钨的工业化应用打下了坚实基础,但同时也暴露出所选萃取体系存在不足[12],主要体现在:1) 萃取体系的分相性能较差,重力分相速度较慢;2) 反萃液中 WO3浓度偏低,只能达到100 g/L左右,后续蒸发结晶蒸发量大、能耗高。上述不足严重阻碍了从碱性介质中直接萃钨新工艺的工业化进程,导致从碱性介质中直接萃钨新工艺在国内外均没有实现工业化。
近10年来,国外未见从碱性介质中直接萃钨的报道。张贵清等[19−20]在碱性介质萃取钨的研究基础上,针对该工艺工业化的瓶颈,采用季铵盐从钨矿苏打高压浸出液中直接萃取钨,取得了突破性进展。通过采用离心萃取器以及合理选择有机相和反萃剂的组成,解决了萃取体系分相速度慢和反萃液 WO3浓度低的问题,并在此基础上对该萃取体系进行了长时间的运转考察,研究结果为该新工艺的产业化排除了障碍。其中,连续运转试验结果已经在文献[20]中进行了报道,本文作者主要报道以TOMAC为萃取剂,从钨矿苏打浸出模拟料液中直接萃取钨的基础实验研究结果。
1 原理
用季铵盐直接萃取钨制备钨酸铵溶液的过程包括萃取、反萃和再生等步骤,萃取剂为季铵碳酸盐,反萃剂为碳酸氢铵与碳酸铵的混合溶液,再生剂为氢氧化钠和碳酸钠的混合溶液。过程的主要反应方程式为
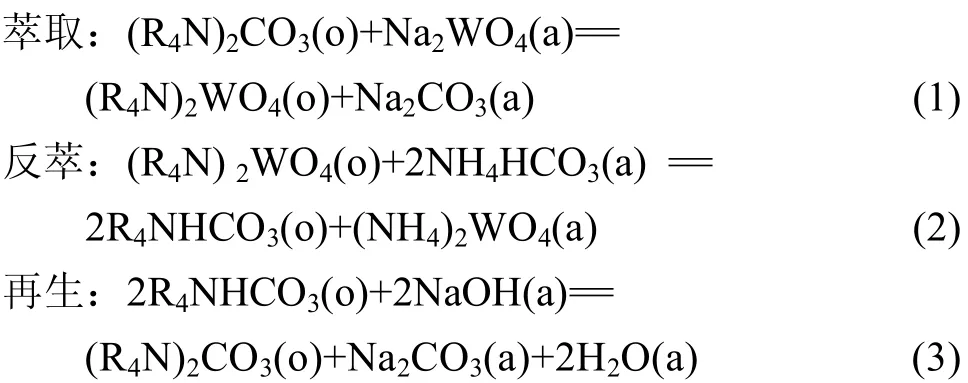
季铵盐萃取 WO42−的能力比 PO43−、AsO43−和SiO44−的强,因而可以优先萃取钨而将杂质 P、As和Si留在萃余液中,从而实现 WO42−与 PO43−、AsO43−和SiO44−等杂质阴离子的分离。
在萃取过程中,杂质可能发生的反应有

2 实验
2.1 原料及试剂
选用三辛基甲基氯化铵(TOMAC)为萃取剂、仲辛醇为极性改善剂、磺化煤油为稀释剂,有机相的组成为50%(体积分数) TOMAC、30%(体积分数)仲辛醇和20%(体积分数)磺化煤油。其中,TOMAC为工业级产品,纯度90%;仲辛醇为化学纯。萃取前将有机相中的Cl−型季铵盐转化成CO32−型。
料液用化学纯试剂模拟工业钨矿苏打浸出液的成分配制而成。反萃剂及再生剂均用化学纯试剂配制。
2.2 方法及设备
萃取与反萃取试验在分液漏斗中于气浴恒温振荡器上进行;串级逆流萃取−反萃取−再生试验在 20级环隙式离心萃取系统中进行,环隙式离心萃取器为清华大学研制,型号为HL−20,转鼓直径为20 mm。
水相中 WO3浓度采用硫氰酸盐比色法测定;As和 Si的浓度分别采用二乙胺硫代酸根比色法和硅钼蓝比色法测定;P的浓度采用离子色谱法测定。
有机相中各元素的浓度根据萃取前、后水相的浓度和体积变化按差减法计算。
3 结果与讨论
3.1 萃取
3.1.1 料液中Na2CO3浓度对萃取过程的影响
钨矿苏打高压浸出液中含有大量 CO32−,而Na2CO3浓度对萃取过程的影响尚未见报道。据文献[12],钨的萃取率随着萃取剂N263浓度的升高而升高,但当浓度高于400 g/L后,分相性能明显变差,在文献[12]中选择有机相组成为 350g/L N263+20%仲辛醇(体积分数)+航空煤油。可见,分相性能是制约萃取剂浓度提高的重要因素。
本研究选用TOMAC为萃取剂,将萃取剂浓度提高至50%(体积分数,约450 g/L TOMAC),有机相组成为50% TOMAC +30%仲辛醇+20%磺化煤油,进一步考察浸出液中 Na2CO3浓度对萃钨率和萃取体系分相性能的影响。料液中WO3浓度为97.41 g/L,萃取相比V(O)/V(A)=2/1,温度20 ℃,振荡时间5 min。图1所示为料液Na2CO3浓度对WO3萃取率和体系分相性能的影响。

图1 料液中Na2CO3浓度对萃取过程分相时间和WO3萃取率的影响Fig.1 Influence of concentration of Na2CO3 in feed solution on phase-separation time and extraction rate of WO3 in extraction process
由图 1可见,料液中 Na2CO3浓度对钨的萃取率影响很小,实验条件下,WO3单级萃取率最低为89.94%,最高为94.01%。当Na2CO3浓度为0时,钨的单级萃取率最高;随后,WO3的单级萃取率随Na2CO3浓度的升高而降低,这是CO32−与WO42−竞争萃取的结果;当 Na2CO3浓度高于 110 g/L后,WO3的单级萃取率随 Na2CO3浓度的升高变化不大。实验条件下,钨的单级萃取率最低也在89%左右,这说明,该萃取体系完全能满足从 Na2CO3体系中深度提取钨的需要。
料液中 Na2CO3浓度对萃取分相性能影响很大。从图1可知,Na2CO3浓度升高,分相速度加快,分相时间缩短;当Na2CO3浓度高于120 g/L后,分相时间变化不大。实验条件下,分相时间最短也在8 min以上,最长为13 min。总体来说,该体系的分相性能仍不理想,重力分相速度较慢,难以满足普通混合澄清槽的要求。
3.1.2 饱和萃取容量的测定和萃取等温线的绘制
在文献[12]中,有机相组成为350g/L N263+20%(体积分数)仲辛醇+航空煤油,其饱和萃钨容量为 59.14 g/L WO3。体系的分相性能限制了有机相中萃取剂浓度的提高,从而限制了有机相饱和萃钨容量的进一步提高,而有机相较低的萃钨容量又是造成反萃液中WO3浓度偏低的重要原因之一。因此,提高有机相的饱和萃钨容量是提高反萃液中 WO3浓度的有效途径之一。
本研究采用组成为 50%TOMAC+30%仲辛醇+20%磺化煤油的有机相,料液中含99.37 g/L WO3、100 g/L Na2CO3、不含其他杂质,用等相比法绘制的萃取等温线如图2所示。实验中相比V(O)/V(A)=5/1,温度为25 ℃,振荡时间为5 min。

图2 WO3的萃取等温线Fig.2 Extraction isotherm of WO3
由图 2可知,组成为 50%TOMAC+30%仲辛醇+20%磺化煤油的有机相的饱和萃钨容量(以WO3计)为91.49 g/L左右。与文献[12]中的结果相比,提高了近55%。
3.2 反萃
3.2.1 反萃剂浓度对反萃过程的影响
在文献[11−18]中,均采用 NH4HCO3溶液作为反萃剂,钨的反萃效果随着 NH4HCO3浓度的升高而增强。但 NH4HCO3在水溶液中溶解度不大,且随温度变化影响很大,温度越高,溶解度越大,而NH4HCO3溶液在高温下不稳定,高于30 ℃即开始分解,产生大量气泡,妨碍分相。因此,通过提高 NH4HCO3溶液浓度来提高钨的反萃效果十分困难。另外,由于NH4HCO3溶液的pH值在8.2左右,随着WO3浓度的提高,反萃液中会出现APT沉淀,这也限制了反萃液中WO3浓度的继续提高。
而在实际操作中,总希望反萃液中WO3浓度高一些,以减少APT的蒸发量、降低能耗,而且也易于控制APT的粒度。为很好地解决以上问题,本文作者在NH4HCO3溶液中加入 NH3·H2O,采用 NH4HCO3+NH3·H2O混合溶液作为反萃剂。
有机相组成为50%TOMAC+30%仲辛醇+20% 磺化煤油,有机相负载WO3浓度为89.655 g/L。考察不同反萃剂浓度对 WO3反萃率的影响,反萃相比V(O)/V(A)=2/1、温度为25 ℃、振荡时间为5 min,结果如图3和4所示。

图3 WO3反萃率与NH4HCO3浓度的关系Fig.3 Relationship between stripping rate of WO3 and concentration of NH4HCO3

图4 WO3反萃率与NH3·H2O浓度的关系Fig.4 Relationship between stripping rate of WO3 and concentration of NH3·H2O
从图3和4可以看出:当NH3·H2O浓度一定时,WO3的反萃率随着 NH4HCO3浓度的升高而升高;当NH4HCO3浓度一定时,WO3的反萃率随着 NH3·H2O的升高而降低;当总 NH4+浓度一定时,NH4HCO3浓度越高,反萃率越高。这是因为HCO3−与季铵盐的结合能力明显强于 CO32−的,即 HCO3−反萃钨的能力强于 CO32−的[13]。反萃剂中 NH3·H2O 浓度越高,HCO3−与 OH−中和生成的 CO32−越多,溶液中实际的 HCO3−浓度越低,从而造成WO3反萃率下降。从这一点来看,加入 NH3·H2O 似乎对反萃不利,但是 NH3·H2O 的加入,一方面可以通过生成(NH4)2CO3来加大NH4HCO3在常温下水中的溶解,减少因 NH4HCO3分解形成的气泡,有利于分相;另一方面也使得反萃体系平衡pH值升高,有利于维持钨在反萃液中的WO42−形态,防止当反萃液中WO3浓度过高时,钨酸根向仲钨酸根形态转化以溶解度较低的仲钨酸铵结晶析出,从而大大提高反萃液的稳定性。因此,在维持一定单级 WO3反萃率的基础上,向反萃剂中加入NH3·H2O对提高反萃液中WO3浓度极为有利。
综上所述,选择 3 mol/L NH4HCO3+1 mol/L NH3·H2O的混合溶液为反萃剂,在本实验条件下,WO3单级反萃率可以达到55.69%。但在实验中发现,反萃取过程的分相性能比萃取过程的差,实验条件下分相时间均在15 min以上,同样存在重力分相速度慢、普通混合澄清槽难以满足要求的问题。
3.2.2 反萃等温线的绘制及相比对反萃过程的影响
为了选择最佳的反萃相比和理论级数,本研究用相变化法绘制了反萃取等温线(见图5)。实验中反萃剂为3 mol/L NH4HCO3+1 mol/L NH3·H2O混合溶液,温度为 20 ℃。图 6所示为 WO3反萃率与反萃相比的关系。
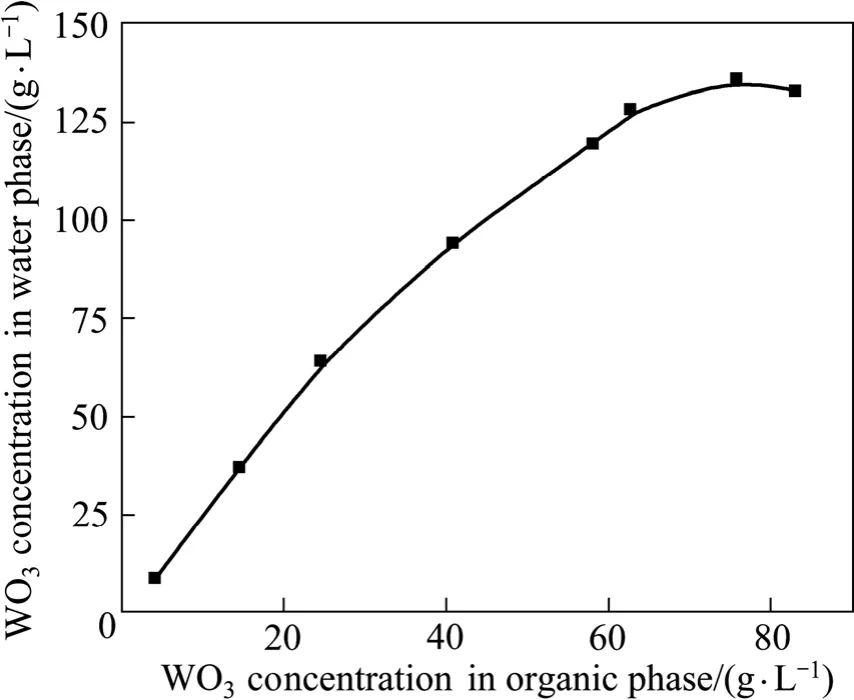
图5 WO3的反萃等温线Fig.5 Stripping isotherm of WO3

图6 WO3反萃率与相比V(O)/V(A)的关系Fig.6 Relationship between stripping rate of WO3 and phase ratio V(O)/V(A)
由图 5可知,以 3 mol/L NH4HCO3+1 mol/L NH3·H2O为反萃剂,反萃液中WO3的最高浓度不低于135 g/L。
结合反萃取等温线(见图5)、反萃率和相比之间的关系(见图6),通过McCabe-Thiele图解法和Kremser方程联合求解,得到本反萃体系在不同反萃相比下,经12级反萃后有机相中WO3反萃率和反萃液中WO3浓度的理论值,结果如表1所列。表1中的计算结果已考虑有机相和水相体积在反萃前、后的变化。

表1 不同反萃相比经12级反萃后WO3反萃率及反萃液中WO3浓度的理论计算值Table 1 Calculated values of stripping rate of WO3 and its concentration in stripping liquor after 12-stage stripping with different phase ratios
由表1可知, 经12级反萃取后,基本可以满足要求。综合考虑,反萃相比选择2/1~2.5/1较为合适。此时,WO3的理论反萃率大于 92%,反萃液中 WO3浓度为166~190 g/L。
3.3 离心萃取器模拟串级逆流萃取与反萃取试验
前已述及,本研究中萃取与反萃取均存在重力分相速度慢的问题,普通混合澄清槽难以满足分相要求。而离心萃取器以离心力取代重力作用,可加速两相的分离,特别适应于化学稳定性差、接触时间短、易于乳化、分离困难等体系的萃取[21],已经在萃取工艺实验中得到了越来越多的应用[22−23]。因次,本研究采用直径为 20 mm环隙式离心萃取系统进行串级逆流萃取与反萃取实验模拟,其流程如图7所示。
实验中,有机相组成为 50%TOMAC+30%仲辛醇+20%磺化煤油,料液含 98.32 g/L WO3、100g/L Na2CO3及较高浓度的杂质 P、As和 Si。有机相的操作容量按 86 g/L WO3计算。反萃剂为 3 mol/LNH4HCO3+1.0 mol/L NH3·H2O,再生剂为 37.5 g/L Na2CO3+45 g/L NaOH。有机相的流量为12 mL/min、料液流量为10.5 mL/min、反萃流比为2/1、再生流比为1.5/1。有机相经2级再生、6级萃取、12级反萃,实验连续进行12 h,系统运行稳定,分相性能良好,两相夹带量低于0.5%。结果如表2所列。
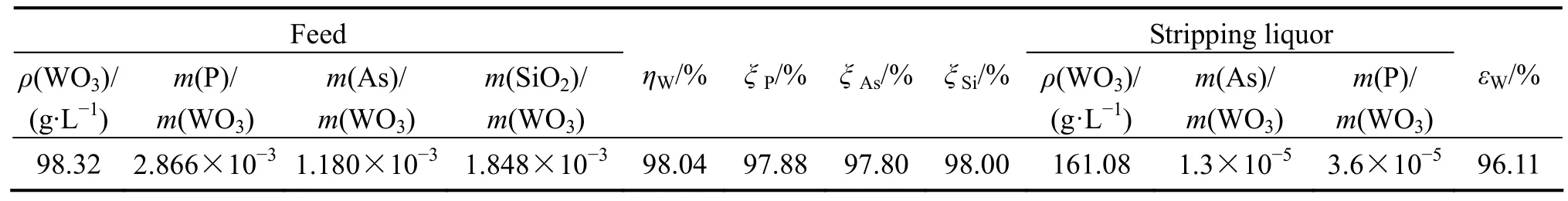
表2 离心萃取器模拟串级逆流萃取与反萃取实验结果Table 2 Experiment results of simulated counter current extraction and stripping using centrifugal extractor

图7 离心萃取器模拟串级逆流萃取与反萃取实验流程Fig.7 Flowchart of simulated counter current extraction and stripping using centrifugal extractor
由表2可知,工艺中钨的萃取率为98.04%;萃取阶段,P、As和Si的除去率不低于97.80%,说明碱性萃钨工艺具有良好的除杂效果。反萃液中WO3浓度可达161.08 g/L,杂钨比完全符合生产国家标准规定的0级APT的要求。
4 结论
1) 料液中Na2CO3浓度对WO3萃取率影响不大,但对萃取过程分相性能影响较大,以TOMAC为萃取剂的萃取体系完全能满足从高浓度 Na2CO3体系中深度提取钨的要求。当有机相组成为50%TOMAC+ 30%仲辛醇+20%磺化煤油时,其饱和萃钨容量可达91.49/L WO3。
2) 用NH4HCO3+NH3·H2O混合溶液作反萃剂,不仅能减少因 NH4HCO3分解产生的气泡,从而改善反萃分相,还能显著提高反萃液的稳定性,为提高反萃液中WO3浓度创造有利的条件。
3) 通过绘制反萃等温线,选择了合适的反萃流比及级数,采用环隙式离心萃取器进行串级逆流萃取和反萃取模拟实验。 控制有机相操作容量为 86 g/L WO3,反萃流比为2/1,有机相经2级再生、6级萃取、12级反萃,连续运行12 h,体系分相性能良好,两相夹带量低于 0.5%。实验条件下,钨的萃取率高于98.3%,萃取阶段P、As和Si等杂质的除去率不低于97.80%。钨的反萃率达96.11%,反萃液中WO3浓度高于160 g/L,杂质含量完全可以满足生产国家标准规定的0级APT的要求。
REFERENCES
[1] 张启修, 赵秦生. 钨钼冶金学[M]. 北京: 冶金工业出版社,2005: 76−141.ZHANG Qi-xiu, ZHAO Qin-sheng. Tungsten and molybdenum metallurgy[M]. Beijing: Metallurgical Industry Press, 2005:76−141.
[2] 李洪桂. 稀有金属冶金学[M]. 北京: 冶金工业出版社, 1990:75−98.LI Hong-gui. Rare metal metallurgy[M]. Beijing: Metallurgical Industry Press, 1990: 75−98.
[3] 朱 屯. 溶剂萃取与离子交换[M]. 北京: 冶金工业出版社,2005: 56−58.ZHU Tun. Solvent extraction and ion exchange[M]. Beijing:Metallurgical Industry Press, 2005: 56−58.
[4] 何立新, 李洪桂, 任鸿九. 离子交换法处理钨矿物原料苏打压煮母液的研究[J]. 中南工业大学学报: 自然科学版, 1995,26(6): 761−765.HE Li-xin, LI Hong-gui, REN Hong-jiu. A Study on the treatment of soda digestion solution of tungsten concentrate by ion-exchange process[J]. Journal of Central South University of Technology: Natural Science, 1995, 26(6): 761−765.
[5] 黄成通. 钨的离子交换新工艺的发展[J]. 稀有金属与硬质合金, 2003, 31(3): 37−41.HUANG Cheng-tong. Development of W ion-exchange new technology[J]. Rare Metals and Cemented Carbides, 2003, 31(3):37−41.
[6] 李洪桂, 李 波, 赵中伟. 钨冶金离子交换新工艺研究[J]. 稀有金属和硬质合金, 2007, 35(1): 1−4.LI Hong-gui, LI Bo, ZHAO Zhong-wei. Development of new ion-exchange process in tungsten metallurgy[J]. Rare Metal and Cemented Carbides, 2007, 35(1): 1−4.
[7] 张子岩, 简椿林. 溶剂萃取法在钨湿法冶金中的应用[J]. 湿法冶金, 2006, 25(1): 1−9.ZHANG Zi-yan, JIAN Chun-lin. Application of solvent extraction in tungsten hydrometallurgy[J]. Hydrometallurgy of China, 2006, 25(1): 1−9.
[8] 张邦胜, 蒋开喜, 王海北, 施友富. 萃取法分离钨钼的研究进展[J]. 有色金属, 2004, 56(4): 89−91.ZHANG Bang-sheng, JIANG Kai-xi, WANG Hai-bei, SHI You-fu. Progress in W/Mo separation by solvent extraction[J].Nonferrous Metals, 2004, 56(4): 89−91.
[9] DROBNICK J L, LEWIS C J. Recovery and Purification of tungsten by liquid ion exchange process[C]//Unit Processes in Hydrometallurgy. London: Gordon and Breach Science Publishers, 1964: 504−514.
[10] 李大任, 苏元复. N263萃取分离W, P[J]. 稀有金属, 1991(1):6−9.LI Da-ren, SU Yuan-fu. Extraction separation of W and P with N263[J]. Chinese Journal of Rare Metals, 1991(1): 6−9.
[11] ZAITSEV V P, IVANOV I M, KALISH N K, US T V. Scientific foundations of a new extraction technology for the processing of tungsten containing solutions[C]//Proceedings of the Second International Conference on Hydrometallurgy(ICHM). Changsha:International Academic Publishers, 1992: 768−772.
[12] 张贵清. 从碱性介质中萃取钨制取纯钨酸铵溶液的研究[D].长沙: 中南大学, 1994: 26−48.ZHANG Gui-qing. The study of tungsten extraction from alkaline media to produce ammonium tungsten solution[D].Changsha: Central South University, 1994: 26−48.
[13] 张贵清, 张启修. 从钨矿苛性钠浸出液中直接萃取钨制取纯钨酸铵溶液的研究(Ⅰ)[J]. 中南矿冶学院学报, 1994, 24(钨专辑): 97−101.ZHANG Gui-qing, ZHANG Qi-xiu. The study of tungsten extraction from caustic soda leach liquor to produce ammonium tungsten solution(Ⅰ) [J]. Journal of Central-South Institute of Mining and Metallurgy, 1994, 24(W Special): 97−101.
[14] 张贵清, 张启修. 从钨矿苛性钠浸出液中直接萃取钨制取纯钨酸铵溶液的研究(Ⅱ)[J]. 中南矿冶学院学报, 1994, 24(钨专辑): 102−105.ZHANG Gui-qing, ZHANG Qi-xiu. The study of tungsten extraction from caustic soda leach liquor to produce ammonium tungsten solution(Ⅱ) [J]. Journal of Central-South Institute of Mining and Metallurgy, 1994, 24(W Special): 102−105.
[15] 廖春发. 从钨矿苛性钠浸出液中直接萃取钨分离杂质的研究[D]. 长沙: 中南大学, 1995: 26−48.LIAO Chun-fa. The study of tungsten extraction of from caustic soda leach liquor[D]. Changsha: Central South University, 1995:26−48.
[16] 廖春发, 张启修. 从碱浸液中萃取钨稀释剂的筛选及其对萃取性能的影响[J]. 中国钨业, 2000, 15(2): 29−31.LIAO Chun-fa, ZHANG Qi-xiu. The influence of diluents on tungsten solvent extraction in alkaline leach liquor and their extraction character[J]. China Tungsten Industry, 2000, 15(2):29−31.
[17] 廖春发, 张启修. 从钨矿苛性钠浸出液直接萃取钨时杂质锡行为的考察[J]. 南方冶金学院学报, 2001, 22(4): 239−242.LIAO Chun-fa, ZHANG Qi-xiu. On the behavior of impurity Sn in tungsten extraction from caustic soda leach liquor[J]. Journal of Southern Institute of Metallurgy, 2001, 22(4): 239−242.
[18] 张贵清, 张启修. 一种钨湿法冶金清洁生产工艺[J]. 稀有金属, 2003, 27(2): 254−257.ZHANG Gui-qing, ZHANG Qi-xiu. A new production technology for tungsten hydrometallurgy[J]. Chinese Journal of Rare Metals, 2003, 27(2): 254−257.
[19] 张贵清, 张启修, 张 斌, 肖连生, 张宏伟, 关文娟.从含钨物料苏打浸出液中离心萃取制取钨酸铵溶液的方法: 中国,CN200810143290.X[P]. 2008−09−25.ZHANG Gui-qing, ZHANG Qi-xiu, ZHANG Bin, XIAO Lian-sheng, ZHANG Hong-wei, GUAN Wen-juan. Methods of preparing solution of ammonium tungstate from autoclave-soda leaching liquor of materials containing tungsten:CN200810143290.X[P]. 2008−09−25.
[20] 张贵清, 关文娟, 张启修, 肖连生, 李青刚, 曹佐英. 从钨矿苏打浸出液中直接萃取钨的连续运转试验[J]. 中国钨业,2009, 24(5): 49−52.ZHANG Gui-qing, GUAN Wen-juan, ZHANG Qi-xiu, XIAO Lian-sheng, LI Qing-gang, CAO Zuo-ying. Continuous-running experiment for direct solvent extraction of tungsten from autoclave-soda leaching liquor of scheelite[J]. China Tungsten Industry, 2009, 24(5): 49−52.
[21] 叶春林. 圆筒式离心萃取器[M]. 北京: 原子能出版社, 2007:8−23.YE Chun-lin. Tube type centrifugal extractor[M]. Beijing:Atomic Energy Press, 2007: 8−23.
[22] 段五华, 周秀珠, 周嘉贞. 微型离心萃取器在萃取工艺实验研究中的应用[J]. 现代化工, 2004, 24(7): 63−65.DUAN Wu-hua, ZHOU Xiu-zhu, ZHOU Jia-zhen. Application of a miniature centrifugal extractor in experiments for extractive process[J]. Modern Chemical Industry, 2004, 24(7): 63−65.
[23] 段五华, 周秀珠, 周嘉贞. 离心萃取器在有色冶金中的应用[J]. 有色金属, 2006, 58(3): 54−58.DUAN Wu-hua, ZHOU Xiu-zhu, ZHOU Jia-zhen. Application of centrifugal extractor in non-ferrous metallurgy[J]. Nonferrous Metals, 2006, 58(3): 54−58.
Extraction of tungsten from simulated autoclave-soda leaching liquor of scheelite with quaternary ammonium salt
GUAN Wen-juan, ZHANG Gui-qing
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
The direct solvent extraction of tungsten from autoclave-soda leach solution of scheelite using quaternary ammonium salt (tri-n-octylmethy-lammonium chloride, TOMAC) was investigated to solve the problems of slow phase separation and low WO3concentration in strip liquor which are main disadvantages in the process of direct solvent extraction of tungsten from alkaline medium. The effects of Na2CO3concentration in leaching solution, composition and concentration of stripping reagent on the extraction and stripping were investigated. The isotherms of the extraction and stripping were plotted, and the optimum flow ratio and stripping stage were determined through Kremser formula. Based on these, the centrifugal extractor was used to simulate the counter current extraction. The results indicate that the concentration of Na2CO3in feed solution has little influence on the extraction of WO3but great influence on the phase separation in the extraction, the saturated loading capacity (for WO3) of organic reaches 91.49 g/L when the concentration of extractant is 50%( volume fraction), the addition of NH3·H2O into NH4HCO3as the mixed stripping reagent not only improves the stability of stripping liquor, but also increases the WO3concentration in stripping liquor. The phase separation is good during the extraction and stripping, and the concentration of WO3in stripping liquor reaches about 160 g/L. The stripping liquor can be used to produce APT of 0 grade of national standards of China.
tungsten; solvent extraction; quaternary ammonium salt; Na2CO3system
TF841.1
A
1004-0609(2011)07-1756-07
2010-08-09;
2010-12-27
张贵清,副教授,博士;电话:0731-88830472;E-mail: gq_zhang@163.com
(编辑 陈卫萍)
