间歇性高容量血液滤过对肾替代治疗病人血清莫西沙星药物浓度的影响
2011-11-20陈铁锋刘双信
李 莉, 史 伟, 陈铁锋, 刘双信
(1南方医科大学研究生学院,广东 广州 510515;2粤北人民医院重症医学科,广东 韶关 512026; 3广东省人民医院肾内科,医学研究中心,广东 广州 510080)
间歇性高容量血液滤过对肾替代治疗病人血清莫西沙星药物浓度的影响
李 莉1,2, 史 伟3△, 陈铁锋3, 刘双信3
(1南方医科大学研究生学院,广东 广州 510515;2粤北人民医院重症医学科,广东 韶关 512026;3广东省人民医院肾内科,医学研究中心,广东 广州 510080)
目的: 研究间歇性高容量血液滤过(PHVHF)治疗时莫西沙星的血清药物浓度变化,为临床用药提供依据。方法8名行PHVHF治疗患者在治疗开始60 min内匀速静滴莫西沙星400 mg,给药后不同时间收集滤器前、后血样和置换液,采用高效液相色谱法(HPLC)测定血清及置换液中莫西沙星浓度。用DAS 2.1.1软件计算药代动力学参数。结果PHVHF治疗前后血尿素氮(BUN)及肌酐(SCr)、血清钾(K+)水平显著下降(Plt;0.05),血清钠(Na+)氯(Cl-)维持稳定。HPLC分析方法测定血滤患者血清及置换液中莫西沙星浓度,线性关系良好,准确度及精密度高。静滴莫西沙星400 mg后在该患者体内的药代动力学符合开放型二室模型。主要药代参数:峰浓度(Cmax)=(4.843±1.854) mg/L,半衰期(T1/2)=(4.822±2.126) h,达峰时间(Tmax)=(1.31±0.59) h,总体分布容积 (Vd)=(82.63±24.69) L,总体清除率(CLtot)=(14.36±8.43) L/h ,AUC/MIC90在MIC90值分别为0.25 mg/L、0.12 mg/L、0.03 mg/L时均大于100,Cmax/ MIC90在MIC90值分别为0.25 mg/L、0.12 mg/L、0.03 mg/L时均大于10。结论PHVHF治疗可明显改善肾功能,稳定内环境,部分清除血清中莫西沙星,但PHVHF治疗后血清药物浓度仍可达到针对病原菌的有效治疗浓度。
间歇性高容量血液滤过; 莫西沙星; 肾替代治疗
莫西沙星是新一代具有广谱抗菌活性的8-甲氧基氟喹诺酮类抗菌药,因其无明显肾毒性,任何程度肾功受损的病人均可使用,故该药在危重患者中的应用未受限制。连续性肾替代治疗(continuous renal replacement therapy,CRRT)常应用于ICU血流动力学不稳定的急性肾功能衰竭(acute renal failure,ARF)及多器官衰竭(multiple organ failure,MOF)等危重患者的抢救[1]。目前缺乏莫西沙星在CRRT病人的药代动力学数据。研究及了解该药在CRRT患者体内的分布、代谢以及从滤液中析出的状况,有助于确保CRRT患者准确合理应用抗生素。由于CRRT模式不断改进,本研究选用置换量为50-70 mL·h-1·kg-1、夜间暂停治疗的12 h间歇性高容量血液滤过治疗(pulse high-volume hemofiltration,PHVHF)方式,探讨莫西沙星药物浓度测定方法及在PHVHF时莫西沙星药物浓度的变化,以指导临床在进行PHVHF时准确使用莫西沙星,同时为临床测定药物浓度提供方法学依据。
材 料 和 方 法
1研究对象和样本采集方法
1.1研究对象 ICU病房临床怀疑或证实对莫西沙星敏感的8名行PHVHF治疗的感染患者人选。试验前签署知情同意书,经医院伦理委员会通过,患者资料见表1。
1.2PHVHF设备与方法 PHVHF采用Braun Diapact CRRT机器,置换液以生理盐水2 000 mL、注射用水500 mL、50%的葡萄糖20 mL、10%葡萄糖酸钙20 mL、25%硫酸镁3 mL、10%氯化钾5 mL配制匀速输入。5%碳酸氢盐125 mL不混入输液袋中,但同时并入同一通路输入以避免离子沉淀。根据患者生化结果调整电解质配方。常规抗生素、液体复苏、机械通气、营养支持等基础上采用PHVHF治疗12 h·d-1,血流量200-250 mL·min-1;置换液前稀释法输入,置换液流量50-70 mL·h-1·kg-1。采用Gambro聚丙脪腈膜(AN69膜,面积0.9 m2),血路为CRRT管路,主要通过股静脉以Seldinger 法置入单针双腔导管建立临时血管通路,根据患者凝血功能采用低分子量肝素(LMWH)、普通肝素或无肝素抗凝。
1.3给药方法 盐酸莫西沙星400 mg,每天1次, 经中心静脉导管(非血滤导管)恒速输注,60 min滴完。
1.4标本采集与检测方法 静滴药后0.5、1、2、3、4、5、6、8、10、12 h分别于滤器前(动脉端)、后(静脉端)采集血样3 mL置普通试管,静置离心(4 000 r/min离心10 min)取上层血清2 mL,-70 ℃冰冻保存备测,相同时点取置换液同法保存备测,采用高效液相色谱法(high performance liquid chromatography ,HPLC)测定莫西沙星浓度。
2药品、试剂与仪器
2.1药品与试剂、仪器 标准品盐酸莫西沙星(商品名拜复乐,德国拜耳公司,批号为BXR2DWF,规格:每瓶400 mg)。惠普1050型高效液相色谱仪,1046荧光检测器;XW-80A 旋涡混合器;YH-3000 数据处理工作站。采用HPLC法测定纯度gt;99.0%;内标盐酸特拉唑嗪;四丁基硫酸氢胺(分析纯);甲醇、乙腈(色谱纯);二氯甲烷(分析纯)。
2.2血清标本的预处理 取0.1 mL血清样品于5 mL玻璃离心管,每管分别加入10 μg的内标,旋涡振荡约10 s,然后加500 μg二氯甲烷,旋涡振荡约1 min后,2 000 r/min离心5 min后,吸弃上水相,收集有机相至另2 mL玻璃离心管内,40 ℃氮气吹干,加入流动相300 μg定容,吸取10 μg进样分析。
3统计学处理
应用DAS 2.1.1药代动力学程序将所测的莫西沙星浓度-时间数值进行房室模型拟合,并计算主要的药代动力学参数。使用SPSS 13.0统计软件包对所得数据进行配对t检验。
结 果
1临床指标检测结果
患者临床资料见表1。结果显示,2例微生物培养结果为肺炎克雷伯杆菌,2例为革兰氏阴性菌,3例未检出病原菌,1例未做,治疗结果存活5例,存活率62.5%,死亡3例。
2PHVHF治疗前后血生化及肾功能
结果见表2。PHVHF治疗后的K+、BUN、SCr较治疗前降低,治疗前后对比,差异显著(Plt;0.05)。PHVHF有效降低毒素水平,纠正高钾血症及电解质紊乱。
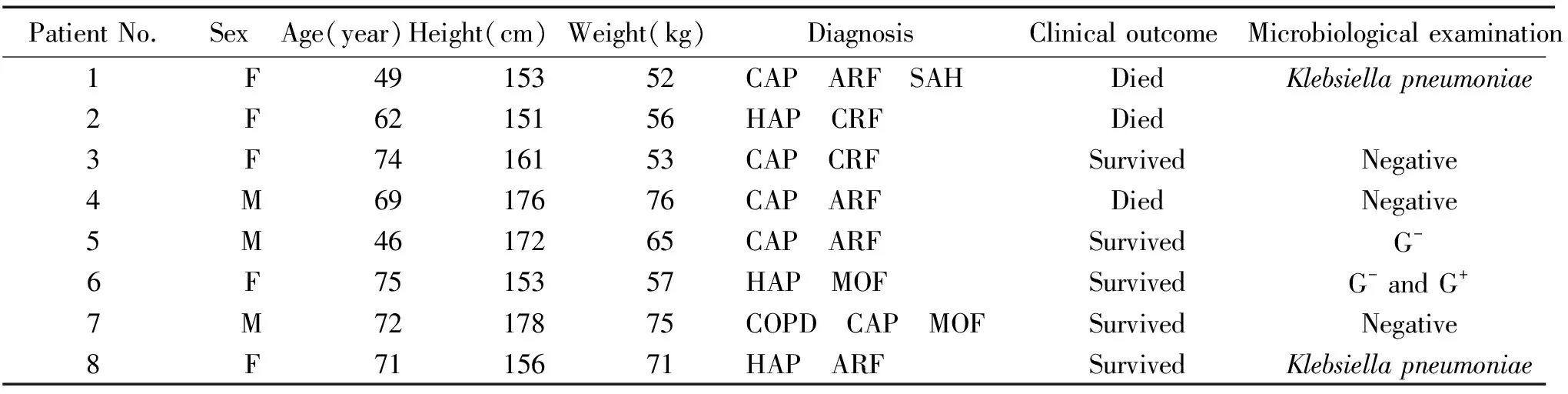
表1 患者临床特征
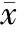
表2 PHVHF治疗前后肾功能变化
3试验样品中分析的色谱图
色谱图见图1。结果显示,莫西沙星保留时间2.7 min,两色谱峰分离好,没有杂质峰干扰。
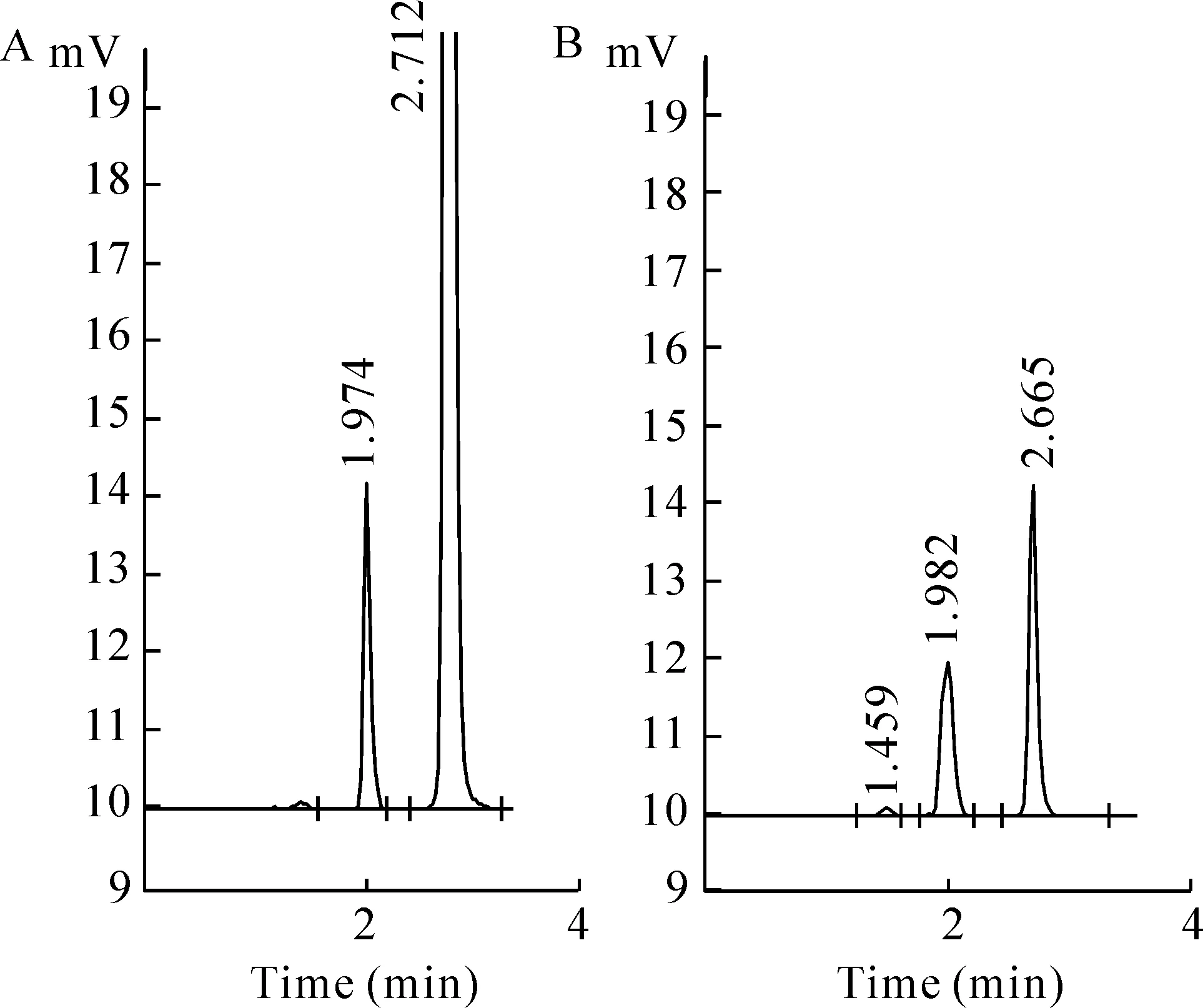
Figure 1.HPLC of moxifloxacin in serum(A) and displacement liquid(B).tR=2.7 min.
4药代动力学结果
4.1血清中莫西沙星的浓度结果 8例行PHVHF治疗患者静脉滴注莫西沙星后,血药浓度见图2。结果显示:静滴莫西沙星后主要药代动力学参数为峰浓度(4.843±1.854)mg/L,达峰时间(1.31±0.59)h。药物浓度随时间变化逐渐衰减,经12 h血滤治疗后,血药浓度降至(1.171±0.725)mg/L。
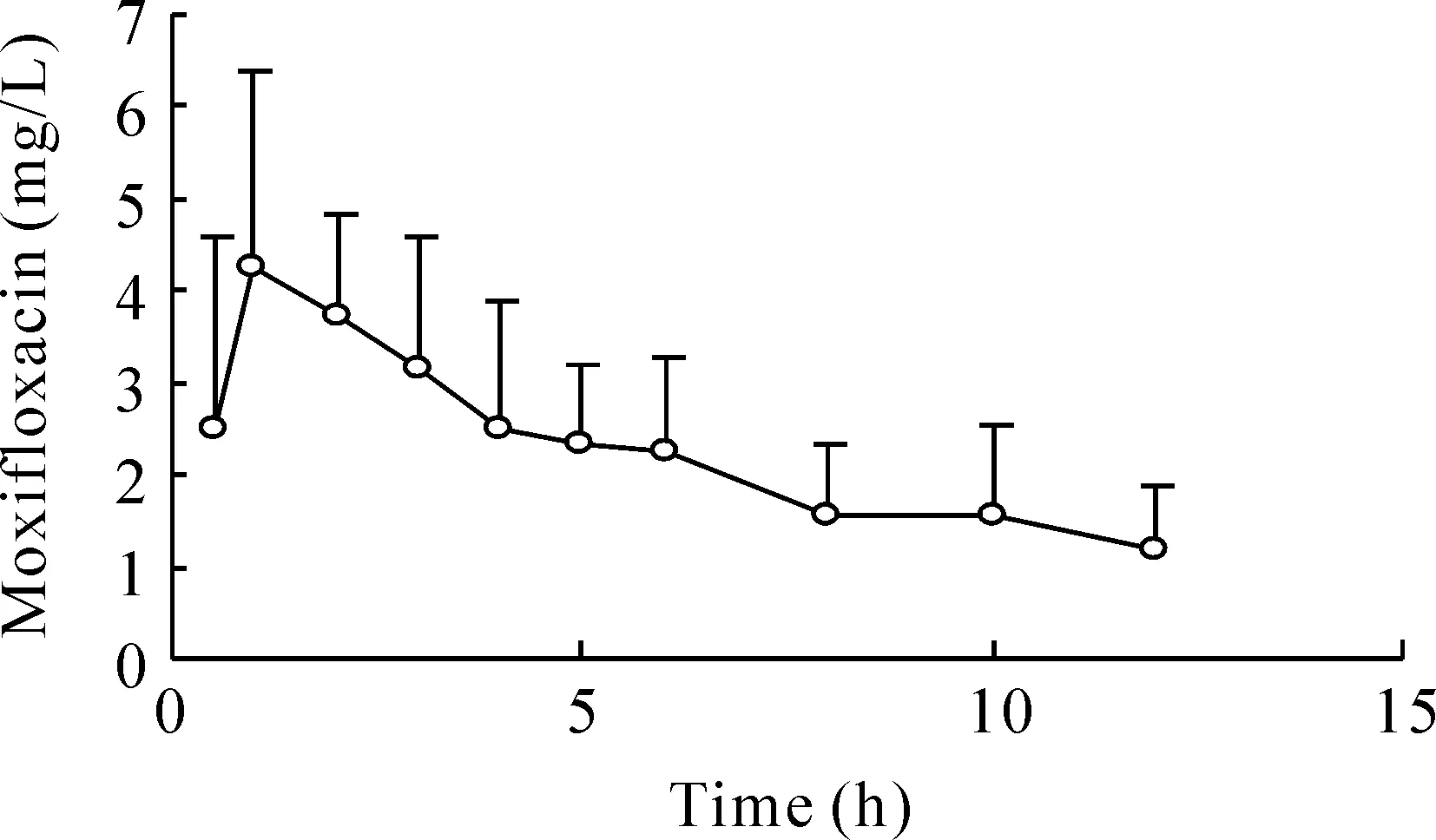
Figure 2.The serum concentration-time curves of moxifloxacin
4.2药代动力学及药效学参数 8例行PHVHF治疗患者静滴莫西沙星60 min后,其时间-血药浓度数据以二室模型拟合最佳,主要药代动力学及药效学参数见表3、4。表3结果显示,PHVHF患者静滴莫西沙星后主要药代动力学参数:峰浓度=(4.843±1.854)mg/L,半衰期(T1/2)=(4.822±2.126)h,药时曲线下面积(AUCO-12 h)(26.908±10.957)mg· h-1·L-1,总体分布面积(Vd)=(82.63±24.69)L。清除率(14.36±8.43)L/h。
表4结果显示,MIC90值分别为0.25 mg/L、0.12 mg/L、0.03 mg/L时AUC/MIC90分别为100.5±44.93、209.38±93.60、837.51±374.40、AUC/MIC90均大于100:MIC90值分别为0.25 mg/L、0.12 mg/L、0.03 mg/L时Cmax/MIC90分别为15.44±6.12、32.17±12.76、128.67±51.03,Cmax/MIC90均大于10;此两道标均超过了治疗相关细菌感染的治疗阈值。

表3 8例行PHVHF治疗患者静滴莫西沙星后主要药代动力学参数

表4 8例行PHVHF治疗患者静滴莫西沙星后主要药效学参数
讨 论
抗生素治疗的药代动力学/药效学(PK/PD)理论,整合了药物的体外活性和体内代谢过程及对微生物和人体的作用,用以预测临床疗效。药物浓度与抗菌效果的关系是目前PK/KD研究热点[2]。莫西沙星在体外显示对革兰阳性、阴性菌及厌氧菌、抗酸菌、支原体、衣原体、军团菌有广谱抗菌活性,是ICU病房重症感染的重要治疗措施。莫西沙星独特的药代动力学特征使其成为治疗呼吸道感染的一线选择[3],与加替沙星、吉米沙星、左氧氟沙星一起被称为“呼吸喹诺酮”。
血液滤过主要依靠对流、超滤的方式清除溶质,药物的清除与超滤率及滤过分数有关,血滤可能清除部分莫西沙星,目前对莫西沙星在血液滤过中的药代学研究极少,给临床合理用药带来困难。血滤患者药物浓度变化受到三方面影响:药物方面:药物理化特性(分子量、蛋白结合力、电荷、水溶性);CRRT方面:CRRT模式、剂量(置换液流速、稀释方式)、滤膜性质(如孔径大小、滤器表面积、吸附作用、静电负荷以及滤器材料)等的影响;患者方面:年龄、残存肾功能、病理生理改变(如血浆蛋白水平等)的影响。
血液净化模式、剂量不断改进,近年提出高容量血液滤过(high volume hemofiltration,HVHF)的概念[4]。HVHF是在标准CRRT的基础上通过增加置换液量提高对大中分子溶质的清除。2001年Ronco等[5]提出超滤率为20-35 mL·h-1·kg-1相当于传统剂量,超过42.8 mL·h-1·kg-1可认为是大剂量。我们选用置换量为50-70 mL·h-1·kg-1的大剂量、夜间暂停、每日12 h的PHVHF方式。目前尚无莫西沙星在HVHF治疗的药代动力学资料。本研究结果提示PHVHF治疗可明显改善肾功,稳定内环境,差异显著(Plt;0.05)。
本实验建立了以二氯甲烷提取、盐酸特拉唑嗪为内标、乙腈∶(10 mmol/L磷酸二氢钾+1.5 mmol/L四丁基硫酸氢胺)=25∶75为流动相的高效液相色谱(HPLC)分析方法,测定血滤患者血清及置换液中药物浓度,结果莫西沙星峰形良好,分离完全,标准曲线拟合好,精密度及准确度高,HPLC法测定莫西沙星浓度适用于血滤患者。
莫西沙星单剂量静脉给药400 mg,1 h后血药浓度达峰值4.1 mg/L,蛋白结合率约为45%。以往的研究[6,7]表明,氟喹诺酮为浓度依赖性抗生素,AUC/MIC及Cmax/ MIC90是决定喹诺酮抗菌效果及减少耐药的PK/PD参数。AUC24/ MIC90比值在100-125范围内或Cmax/ MIC90gt;10时,细菌清除率最大且能有效减少耐药。Waqner等[8]研究盐酸莫西沙星体外抗菌活性结果可见,莫西沙星在呼吸道常见病原菌肺炎球菌、卡他莫拉菌、流感嗜血杆菌、肺炎衣原体、肺炎支原体的90%最低抑菌浓度(MIC90)分别为0.25、0.12、0.03、0.12及0.12 mg/L。我们的研究表明,AUC/ MIC90在MIC90值分别为0.25 mg/L、0.12 mg/L、0.03 mg/L均大于100,Cmax/MIC90在MIC90值分别为0.25 mg/L、0.12 mg/L、0.03 mg/L均大于10;提示临床应用莫西沙星400 mg/d治疗重症感染PHVHF患者具有优良的PK/PD特性。
本研究结果显示,所有行PHVHF治疗患者均可良好耐受莫西沙星治疗,血药浓度-时间数据以二室模型拟合最佳。给药1 h达峰浓度,滤器前血药峰浓度为(4.843±1.854)mg/L,滤器后(3.274±1.491)mg/L,与文献[9]报道相似。12 h后滤器前血药浓度降至(1.171±0.725)mg/L,滤器后(1.200±0.671)mg/L。提示药物最低浓度(1.171±0.725)mg/L至(1.200±0.671)mg/L,高于大多数革兰阴性菌、重要革兰阳性菌、厌氧菌及肺炎衣原体、支原体的MIC90。主要药代参数:T1/2为(4.822±2.216)h, Vd为(82.63±24.69)L,CL为(14.36±8.43)L/h,提示莫西沙星用于行PHVHF治疗危重病患者,半衰期缩短,清除率增加,容积分布Vd增加,表明血滤可部分清除莫西沙星,但血药浓度仍可达病原菌有效浓度,因此可以认为血滤患者莫西沙星每天400 mg的给药剂量合理。
[1]季大玺,谢红浪,黎磊石.连续性血液净化与非肾脏疾病[J].中国危重病急救医学,2001,13(1):5-9.
[2]Mouton JW,Dudley MN,Cars O,et al.Standardization of pharmacokinetic pharmacodynamic (PK/PD) terminology for anti-infective drugs: an update[J].J Antimicrob Chemother,2005,55(5): 601-607.
[3]Krasemann C,Meyer J,Tillotson G,et al.Evaluation of the clinical microbiology profile of moxifloxacin[J].Clin Infect Dis,2001,32(3): S51-S63.
[4]Romero CM,Downey P,Hernandez G.High volume hemofiltration in septic shock[J].Med Intensiva,2010,34(5):345-352
[5]Renco C,Bellomo R,Homel P,et al .Effect of different doses in continuous veno-venous hemofiltration on outcoms of acute renal failure: a prospective randomised trial[J].Lancet,2000,356(9223):26-30.
[6]Nightingale CH.Moxifloxacin,a new antibiotic designed to treat community-acquired respiratory tract infections: a review of microbiologic and pharmacokinetic pharmacodynamic characteristics[J].Pharmacotherapy,2000,20(3): 245-256.
[7]Aminimanizani A,Beringer P,Jelliffe R.Comparative pharmacokinetics and pharmacodynamics of the newer fluoroquinolone antibacterials[J].Clin Pharmacokinet,2001,40(3):169-187.
[8]Waqner RS,Granet DB,Lichtenstein SJ,et al.Kinetics of kill of bacterial conjunctivitis isolates with moxifloxacin,a fluoroquinolone,compared with the aminoglycosides tobramycin and gentamicin[J].Clin Ophthalmol,2010,4:41-45.
[9]Deshpande D,Srivastava S,Meek C,et al.Moxifloxacin pharmacokinetics/pharmacodynamics and optimal dose and susceptibility breakpoint identification for treatment of disseminatedMycobacteriumaviuminfection[J].Antimicrob Aqents Chemother,2010,54(6):2534-2539.
Effectsofpulsehigh-volumehemofiltrationonserumconcentrationofmoxifloxacininpatientswithcontinuousrenalreplacementtherapy
LI Li1,2,SHI Wei3,CHEN Tie-feng3,LIU Shuang-xin3
(1GraduateSchool,SouthernMedicalUniversity,Guangzhou510515,China;2DepartmentofCriticalCareMedicine,YuebeiPeople’sHospital,Shaoguan512026,China;3DepartmentofNephrology,GuangdongGeneralHospital,Guangzhou510080,China.E-mail:weishi_gz@126.com)
AIM: To study the changes of the serum moxifloxacin concentration in the patients with continuous renal replacement therapy when applied for pulse high-volume hemofiltration (PHVHF).METHODSThe patients applied for PHVHF were intravenously given moxifloxacin at the dose of 400 mg in 60 min.Blood samples were collected from the arterial (input) and venous (output) lines of the extracorporeal circuit immediately at different time points after the beginning of infusion,and replacement fluid was taken at the corresponding time points.The serum concentration of moxifloxacin was measured by high-performance liquid chromatography (HPLC).The pharmacokinetics parameters were determined using DAS 2.1.1 software.RESULTSTwo-compartment model was used to achieve the best concentration-time relation of moxifloxacin.The levels of blood urea nitrogen (BUN),serum creatinine (SCr) and serum K+were obviously decreased after application of PHVHF (Plt;0.05).The peak serum concentration (Cmax) of moxifloxacin was (4.843±1.854) mg/L.The half-life (T1/2) was (4.822±2.126) h and the peak time (Tmax) was (1.31±0.59) h.The total volume of distribution (Vd) was (82.63±24.69) L.The total clearance (CLtot) was (14.36±8.43) L/h.All the ratios of area under the concentration-time curve (AUC) to 90% minimal inhibitory concentration (MIC90) were more than 100 when the values of MIC90were 0.25 mg/L,0.12 mg/L and 0.03 mg/L.All the values of Cmax/MIC90were more than 10 when the values of MIC90were 0.25 mg/L,0.12 mg/L and 0.03 mg/L.CONCLUSIONApplication of PHVHF obviously improves the renal functions and eliminates a part of moxifloxacin in the serum.However,the serum concentration of moxifloxacin remains at the effective level for controlling the pathogenic bacteria.
Pulse high-volume hemofiltration; Moxifloxacin; Renal replacement therapy
1000-4718(2011)05-1008-04
R363
A
10.3969/j.issn.1000-4718.2011.05.034
2010-11-22
2011-03-29
△通讯作者 Tel:020-83827812-62027;E-mail weishi_gz@126.com
